Trắc nghiệm Tổng hợp bài tập cacbon - silic hay và khó (phần 1) - Hóa 11Đề bài
Câu 1 :
Trộn 100 ml dung dịch A gồm KHCO3 1M và K2CO3 1M vào 100 ml dung dịch B gồm NaHCO3 1M và Na2CO3 1M thu được dung dịch C. Nhỏ từ từ 100 ml dung dịch D gồm H2SO4 1M và HCl 1M vào dung dịch C thu được V lít CO2 (đktc) và dung dịch E. Cho dung dịch Ba(OH)2 tới dư vào dung dịch E thì thu được m gam kết tủa.Giá trị của m và V lần lượt là :
Câu 2 :
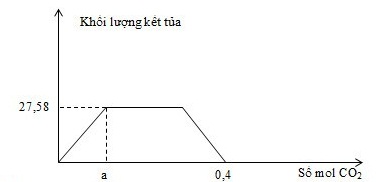
Cho m gam hỗn hợp gồm Na, Na2O, Ba, BaO vào lượng nước dư, thu được dung dịch X và a mol khí H2. Sục khí CO2 đến dư vào dung dịch X, phản ứng được biểu diễn theo đồ thị sau:
Giá trị của m là
Câu 3 :
Hấp thụ hoàn toàn V lít CO2 (đktc) vào dung dịch chứa đồng thời 0,1 mol Ba(OH)2; 0,255 mol KOH và 0,2 mol NaOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và kết tủa Y. Nhỏ từ từ đến hết dung dịch X vào dung dịch chứa 0,35 mol HCl, sinh ra 0,25 mol CO2. Giá trị của V là
Câu 4 :
Dung dịch Z gồm Na2CO3 0,4M, KHCO3 xM. Thêm từ từ 0,5 lít dung dịch Z vào 500 ml dung dịch HCl 1M sau phản ứng hoàn toàn thu được khí và dung dịch Y. Cho dung dịch Ba(OH)2 dư vào dung dịch Y sau phản ứng hoàn toàn thu được 78,8 gam kết tủa. Giá trị x là
Câu 5 :
Hấp thụ hết 4,480 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Cho từ từ 100 ml X vào 300 ml dung dịch HCl 0,5M thu được 2,688 lít khí (đktc). Mặt khác, 100 ml X tác dụng với dung dịch Ba(OH)2 dư, thu được 39,4 gam kết tủa. Giá trị của x là
Câu 6 :
Sục CO2 vào dung dịch chứa Ca(OH)2 và NaOH ta thu được kết quả biểu diễn theo hình bên. Giá trị của x bằng bao nhiêu?
Câu 7 :
Hấp thụ hết 4,48 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Cho từ từ đến hết 100 ml dung dịch X vào 300 ml dung dịch HCl 0,5M, thu được 2,688 lít khí (đktc). Mặt khác, cho 100 ml dung dịch X tác dụng với đung dịch Ba(OH)2 dư, thu được 39,4 gam kết tủa. Giá trị của x là
Câu 8 :
Cho một luồng khí CO đi qua ống sứ đựng m gam Fe2O3 nung nóng. Sau một thời gian thu được 44,46 gam hỗn hợp X gồm Fe3O4, FeO, Fe, Fe2O3 dư. Cho X tác dụng hết với dung dịch HNO3 loãng thu được 3,136 lít NO (đktc) duy nhất. Thể tích khí CO (đktc) và m gam Fe2O3 đã dùng là:
Câu 9 :
Hòa tan hết 34,6 gam hỗn hợp gồm Na, Na2O, Ba, BaO vào nước dư, thu được dung dịch X và a mol khí H2. Sục khí CO2 dư vào dung dịch X, phản ứng được biểu diễn theo sơ đồ sau:
Nếu cho 34,6 gam X tác dụng với 300 ml dung dịch H2SO4 0,4M và HCl 0,6M. Kết thúc phản ứng, thu được dung dịch Y có khối lượng tăng x gam so với dung dịch ban đầu. Giá trị của x là
Câu 10 :
Cho từ từ dung dịch HCl 1M đến dư vào 200 ml dung dịch X chứa Na2CO3 và NaHCO3. Phản ứng được biểu diễn theo đồ thị sau:
Nếu cho từ từ 200 ml dung dịch X vào 175 ml dung dịch HCl 1M, thu được V lít khí CO2 (đktc). Giá trị của V là
Lời giải và đáp án
Câu 1 :
Trộn 100 ml dung dịch A gồm KHCO3 1M và K2CO3 1M vào 100 ml dung dịch B gồm NaHCO3 1M và Na2CO3 1M thu được dung dịch C. Nhỏ từ từ 100 ml dung dịch D gồm H2SO4 1M và HCl 1M vào dung dịch C thu được V lít CO2 (đktc) và dung dịch E. Cho dung dịch Ba(OH)2 tới dư vào dung dịch E thì thu được m gam kết tủa.Giá trị của m và V lần lượt là :
Đáp án : A Phương pháp giải :
Khi cho từ từ dd HCl vào dung dịch X thì ta có \(\begin{array}{l}{H^ + } + C{O_3}^{2 - } \to HC{O_3}^ - \\HC{O_3}^ - + {H^ + } \to {H_2}O + C{O_2}{\rm{ }}\end{array}\) +) Tính theo PTHH => V +) Tính số mol ion HCO3- và SO42- trong E => số mol kết tủa Lời giải chi tiết :
Dd C có: \({{n}_{HCO_{3}^{-}}}=0,2\text{ }mol;\text{ }{{n}_{CO_{3}^{2-}}}=0,2\text{ }mol\) và Na+ , K+ Dd D: ${{n}_{{{H}^{+}}}}=0,3\,mol;\,{{n}_{SO_{4}^{2-}}}=0,1\,mol$và Cl- Nhỏ từ từ D vào C CO32- + H+ → HCO3- 0,2 → 0,2 → 0,2 H+ + HCO3- → CO2 + H2O 0,1 → 0,1 → 0,1 => V = 0,1.22,4 = 2,24 lít E chứa HCO3- (0,3 mol); SO42- (0,1 mol) và các ion khác Cho Ba(OH)2 dư vào E Ba2+ + HCO3- + OH- → BaCO3 + H2O 0,3 → 0,3 Ba2+ + SO42- → BaSO4 0,1 → 0,1 => m = 0,3.197 + 0,1.233 = 82,4 gam
Câu 2 :
Cho m gam hỗn hợp gồm Na, Na2O, Ba, BaO vào lượng nước dư, thu được dung dịch X và a mol khí H2. Sục khí CO2 đến dư vào dung dịch X, phản ứng được biểu diễn theo đồ thị sau:
Giá trị của m là
Đáp án : B Phương pháp giải :
+ Tại thời điểm ${{n}_{C{{O}_{2}}}}~=a$ thì: ${{n}_{B{{a}^{2+}}}}~=\text{ }{{n}_{\downarrow \text{ }max}}~={{n}_{C{{O}_{2}}}}$ + Tại thời điểm ${{n}_{C{{O}_{2}}}}~=0,4\text{ }mol$ thì ${{n}_{HC{{O}_{3}}^{-}}}~={{n}_{C{{O}_{2}}}}~=0,4\text{ }mol$ BTĐT => ${{n}_{N{{a}^{+}}}}~={{n}_{HC{{O}_{3}}^{-}~}}-2{{n}_{B{{a}^{2+}}}}$ BT e: 2nBa + nNa = 2nO + 2nH2 => nO => m = mBa + mNa + mO Lời giải chi tiết :
${{n}_{B{{a}^{2+}}~}}={{n}_{\downarrow max}}~=\frac{27,58}{197}=0,14\text{ }mol$ (tại thời điểm ${{n}_{C{{O}_{2}}~}}=a=0,14$) Khi ${{n}_{C{{O}_{2}}}}~=0,4\text{ }mol$ : dung dịch thu được gồm: Ba2+ (0,14 mol), HCO3- (0,4 mol) và Na+ BTĐT => ${{n}_{N{{a}^{+}}}}~={{n}_{HC{{O}_{3}}^{-}~}}-2{{n}_{B{{a}^{2+}}}}$ = 0,12 mol BT e: 2nBa + nNa = 2nO + 2nH2 => nO = 0,06 mol m = mBa + mNa + mO = 22,9 gam
Câu 3 :
Hấp thụ hoàn toàn V lít CO2 (đktc) vào dung dịch chứa đồng thời 0,1 mol Ba(OH)2; 0,255 mol KOH và 0,2 mol NaOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và kết tủa Y. Nhỏ từ từ đến hết dung dịch X vào dung dịch chứa 0,35 mol HCl, sinh ra 0,25 mol CO2. Giá trị của V là
Đáp án : A Phương pháp giải :
Tính nOH- Do nH+ > nCO2 nên X có cả CO32- => X không có Ba2+ => ${{n}_{BaC{{O}_{3}}}}~={{n}_{Ba{{\left( OH \right)}_{2}}}}$ Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+ x + y = ${{n}_{C{{O}_{2}}}}$ 2x + y = ${{n}_{{{H}^{+}}}}$ => x và y Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (xk mol), HCO3- (yk mol) BTĐT => k BTNT C: ${{n}_{C{{O}_{2}}}}$ban đầu $={{n}_{BaC{{O}_{3}}}}+{{n}_{CO_{3}^{2-}}}~+\text{ }{{n}_{HCO_{3}^{-}}}$ => V Lời giải chi tiết :
${{n}_{O{{H}^{-}}}}=0,1.2+0,225+0,2=0,625\text{ }mol$ Do ${{n}_{{{H}^{+}}}}>{{n}_{C{{O}_{2}}}}$ nên X có cả CO32- => X không có Ba2+ => ${{n}_{BaC{{O}_{3}}}}~={{n}_{Ba{{\left( OH \right)}_{2}}}}$= 0,1 mol Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+ x + y = ${{n}_{C{{O}_{2}}}}$ = 0,25 2x + y = ${{n}_{{{H}^{+}}}}$ = 0,35 => x = 0,1; y = 0,15 Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol) BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3 BTNT C: ${{n}_{C{{O}_{2}}}}$ban đầu $={{n}_{BaC{{O}_{3}}}}+{{n}_{CO_{3}^{2-}}}~+\text{ }{{n}_{HCO_{3}^{-}}}$ = 0,1 + 0,13 + 0,195 = 0,425 mol => V = 9,52 lít
Câu 4 :
Dung dịch Z gồm Na2CO3 0,4M, KHCO3 xM. Thêm từ từ 0,5 lít dung dịch Z vào 500 ml dung dịch HCl 1M sau phản ứng hoàn toàn thu được khí và dung dịch Y. Cho dung dịch Ba(OH)2 dư vào dung dịch Y sau phản ứng hoàn toàn thu được 78,8 gam kết tủa. Giá trị x là
Đáp án : D Phương pháp giải :
Khi sục từ từ CO32- và HCO3- vào H+ thì phản ứng xảy ra đồng thời và theo đúng tỉ lệ mol $\left\{ {\begin{array}{*{20}{l}}{CO_3^{2 - }:0,2}\\{HCO_3^ - :a}\end{array}} \right. \to \frac{{HCO_3^ - }}{{CO_3^{2 - }}} = 5{\rm{a}}$ CO32- + 2H+ → CO2 + H2O y → 2y HCO3- + H+ → CO2 + H2O 5ay 5ay +) Từ số mol H+ => PT (1) ẩn y và ay +) tính được nBaCO3 +) BTNT C => PT (2) ẩn y và ay => a và y +) $x=\frac{n}{V}$ Lời giải chi tiết :
Câu 5 :
Hấp thụ hết 4,480 lít CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Cho từ từ 100 ml X vào 300 ml dung dịch HCl 0,5M thu được 2,688 lít khí (đktc). Mặt khác, 100 ml X tác dụng với dung dịch Ba(OH)2 dư, thu được 39,4 gam kết tủa. Giá trị của x là
Đáp án : C Phương pháp giải :
Xét trong 100 ml dung dịch X BTNT: C => nBaCO3 = PT (1) Gọi u và v lần lượt là số mol HCO3- và CO32- tác dụng với HCl với tỉ lệ u/v = a/b HCO3- + H+ → CO2 + H2O CO32- + 2H+ → CO2 + H2O +) Từ 2 PT => hệ u và v $=>\frac{a}{b}=\frac{u}{v}=?(2)$ Từ (1) và (2) => a = ? và b = ? (mol) Xét trong 200 ml dd X chứa: CO32-: 2b ; HCO3-: 2a; K+ : ? (mol) ( Bảo toàn điện tích ra được số mol của K+) BTNT K, C => x, y = ? Lời giải chi tiết :
Xét trong 100 ml dung dịch X BTNT: C => nBaCO3 = a + b = 0,2 (1) Gọi u và v lần lượt là số mol HCO3- và CO32- tác dụng với HCl với tỉ lệ u/v = a/b HCO3- + H+ → CO2 + H2O u → u → u (mol) CO32- + 2H+ → CO2 + H2O v → 2v → v (mol) Ta có hệ phương trình $\begin{array}{*{20}{l}}{\left\{ {\begin{array}{*{20}{l}}{\sum {{n_{{H^ + }}} = u + 2v = 0,15} }\\{\sum {{n_{C{O_2}}} = u + v = 0,12} }\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{l}}{u = 0,09(mol)}\\{v = 0,03(mol)}\end{array}} \right.}\\{ =>\frac{a}{b} = \frac{u}{v} = \frac{1}{3}\Rightarrow 3a - b = 0,2{\mkern 1mu} {\mkern 1mu} (2)}\end{array}$ Từ (1) và (2) => a = 0,05 và b = 0,15 (mol) Xét trong 200 ml dd X chứa: CO32-: 0,1 ; HCO3-: 0,3; K+ : 0,5 (mol) (Bảo toàn điện tích ra được số mol của K+)
Câu 6 :
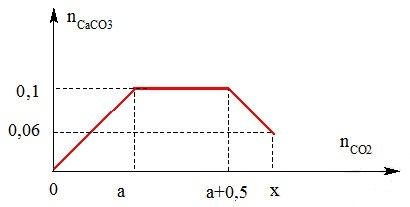
Sục CO2 vào dung dịch chứa Ca(OH)2 và NaOH ta thu được kết quả biểu diễn theo hình bên. Giá trị của x bằng bao nhiêu?
Đáp án : A Phương pháp giải :
+ Tại nCO2 = a mol: CO2 + Ca(OH)2 → CaCO3 + H2O => a = ? + Từ nCO2 = a+0,5 đến nCO2 = x có thêm giai đoạn: CO2 + CaCO3 + H2O → Ca(HCO3)2 => x = ? Lời giải chi tiết :
+ Tại nCO2 = a mol: CO2 + Ca(OH)2 → CaCO3 + H2O 0,1 ← 0,1 a = 0,1 mol + Từ nCO2 = a+0,5 đến nCO2 = x có thêm giai đoạn: CO2 + CaCO3 + H2O → Ca(HCO3)2 0,04←0,04 => x = 0,04 + a + 0,5 = 0,04 + 0,1 + 0,5 = 0,64 mol
Câu 7 :
Hấp thụ hết 4,48 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Cho từ từ đến hết 100 ml dung dịch X vào 300 ml dung dịch HCl 0,5M, thu được 2,688 lít khí (đktc). Mặt khác, cho 100 ml dung dịch X tác dụng với đung dịch Ba(OH)2 dư, thu được 39,4 gam kết tủa. Giá trị của x là
Đáp án : B Phương pháp giải :
Khi cho từ từ dd chứa HCO3- và CO32- vào dd HCl sẽ xảy ra phản ứng: HCO3- + H+ → CO2 + H2O CO32- + 2H+ → CO2 + H2O Gọi x và y là số mol khi tham gia phản ứng với HCl với tỉ lệ này trùng với tỉ lệ HCO3- và CO32- ban đầu. Bảo toàn nguyên tố C Bảo toàn điện tích Bảo toàn nguyên tố K Lời giải chi tiết :
TH1: Nếu trong dd X có OH- dư => dd X chứa OH- dư, CO32-, K+ Khi cho từ từ 100 ml dd X vào 0,15 mol HCl OH- + H+ → H2O CO32- + 2H+ → CO2 ↑+ H2O => ${{n}_{{{H}^{+}}}}~={{n}_{O{{H}^{-}}}}+2{{n}_{C{{O}_{2}}}}~>0,12.2=0,24\text{ }\left( mol \right)$ => loại vì ${{n}_{{{H}^{+}}}}=0,15\left( mol \right)$ Vậy dd X không chứa OH- dư TH2: dd X không chứa OH- dư ta có sơ đồ bài toán như trên Khi cho từ từ 100ml dd X vào 0,15 mol HCl có phản ứng: HCO3- + H+ → CO2 + H2O x → x → x (mol) CO32- + 2H+ → CO2 + H2O y → 2y → y (mol) Gọi x và y là số mol khi tham gia phản ứng với HCl với tỉ lệ $\frac{x}{y}=\frac{a}{b}$ Ta có: $\left\{ {\begin{array}{*{20}{l}}{\sum {{n_{C{O_2}}} = x + y = 0,12} }\\{\sum {{n_{HCl}} = x + 2y = 0,15} }\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{l}}{x = 0,09\left( {mol} \right)}\\{y = 0,03\left( {mol} \right)}\end{array}} \right. \Rightarrow \frac{a}{b} = \frac{x}{y} = \frac{3}{1} = > a = 3b{\mkern 1mu} {\mkern 1mu} (1)$ BTNT C: ${{n}_{BaC{{O}_{3}}}}$ = a + b = 0,2 (2) Từ (1) và (2) => a = 0,15 và b = 0,05 (mol) Trong 200 ml dd X: ${{n}_{HCO_{3}^{-}}}~=0,3\left( mol \right);\,{{n}_{CO_{3}^{2-}}}~=0,1\left( mol \right)$ Bảo toàn điện tích đối với dd X : nK+ = 0,3 + 0,1.2 = 0,5 (mol) BTNT C: ${{n}_{CO2(b)}}+{{n}_{{{K}_{2}}C{{O}_{3}}}}={{n}_{HCO_{3}^{-}}}+{{n}_{CO_{3}^{2-}}}~$=> 0,2 + y = 0,3 + 0,1 => y = 0,2 (mol) BTNT K: ${{n}_{K+}}={{n}_{KOH}}+2{{n}_{{{K}_{2}}C{{O}_{3}}}}=>{{n}_{KOH}}=0,52.0,2=0,1\left( mol \right)$ => x = 0,1 (mol)
Câu 8 :
Cho một luồng khí CO đi qua ống sứ đựng m gam Fe2O3 nung nóng. Sau một thời gian thu được 44,46 gam hỗn hợp X gồm Fe3O4, FeO, Fe, Fe2O3 dư. Cho X tác dụng hết với dung dịch HNO3 loãng thu được 3,136 lít NO (đktc) duy nhất. Thể tích khí CO (đktc) và m gam Fe2O3 đã dùng là:
Đáp án : D Phương pháp giải :
Coi hỗn hợp các oxit sắt chỉ gồm Fe (x mol) và O (y mol) +) Bảo toàn e cho cả quá trình: ne (CO) nhường = n e (HNO3) nhận +) Bảo toàn e và bảo toàn khối lượng => x và y Lời giải chi tiết :
Bảo toàn e cho cả quá trình => ne (CO) nhường = n e (HNO3) nhận => ${{n}_{~CO}}~=\frac{0,14.3}{2}=0,21\left( \text{ }mol \right)$ => VCO = 4,704 (lít) Coi X gồm Fe : x (mol) và O : y (mol) Dùng bảo toàn e và bảo toàn khối lượng $ \to \left\{ {\begin{array}{*{20}{l}}{56{\rm{x}} + 16y = 44,46}\\{3{\rm{x}} - 2y = 0,14.3}\end{array}} \right. \to \left\{ {\begin{array}{*{20}{l}}{x = 0,59775 = {n_{F{\rm{e}}}} \Rightarrow {n_{F{{\rm{e}}_2}{O_3}}} = 0,298875}\\{y = 0,686625 = {n_O}}\end{array}} \right.$ => mFe2O3 = 0,298875.160 = 47,82 (gam)
Câu 9 :
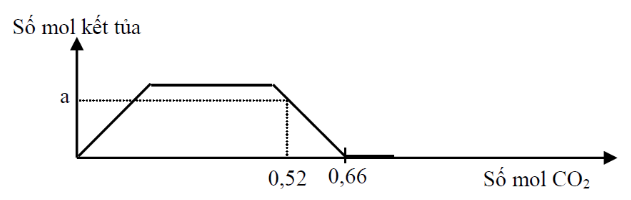
Hòa tan hết 34,6 gam hỗn hợp gồm Na, Na2O, Ba, BaO vào nước dư, thu được dung dịch X và a mol khí H2. Sục khí CO2 dư vào dung dịch X, phản ứng được biểu diễn theo sơ đồ sau:
Nếu cho 34,6 gam X tác dụng với 300 ml dung dịch H2SO4 0,4M và HCl 0,6M. Kết thúc phản ứng, thu được dung dịch Y có khối lượng tăng x gam so với dung dịch ban đầu. Giá trị của x là
Đáp án : B Phương pháp giải :
Hỗn hợp ban đầu chứa Na (x mol); Ba (y mol) và O (z mol) +) Khối lượng hỗn hợp => PT (1) +) Bảo toàn electron => PT (2) Trên đồ thị, khi CO2 = 0,66 thì kết tủa bị hòa tan hết => ${{n}_{HCO_{3}^{-}}}$ +) Bảo toàn điện tích => Pt (3) Tại nCO2 = 0,53 thì kết tủa bị hòa tan 1 phần ${{n}_{BaC{{O}_{3}}}}=a\Rightarrow {{n}_{Ba{{\left( HC{{O}_{3}} \right)}_{2}}}}=y-a$ và ${{n}_{NaHC{{O}_{3}}}}=x$ +) Bảo toàn C => Pt (4) Từ (1), (2), (3), (4) => x; y; z; a +) $\Delta m=34,6{-{m}_{BaS{{O}_{4}}}}-{{m}_{{{H}_{2}}}}$ Lời giải chi tiết :
Hỗn hợp ban đầu chứa Na (x mol); Ba (y mol) và O (z mol) => 23x + 137y + 16z = 34,6 (1) Bảo toàn electron: x + 2y = 2z + 2a (2) Trên đồ thị, khi CO2 = 0,66 thì kết tủa bị hòa tan hết => ${{n}_{HCO_{3}^{-}}}=0,66$ Bảo toàn điện tích => x + 2y = 0,66 (3) Tại nCO2 = 0,53 thì kết tủa bị hòa tan 1 phần ${{n}_{BaC{{O}_{3}}}}=a\Rightarrow {{n}_{Ba{{\left( HC{{O}_{3}} \right)}_{2}}}}=y-a$ và ${{n}_{NaHC{{O}_{3}}}}=x$ Bảo toàn C => a + 2.(y – a) + x = 0,52 (4) Từ (1), (2), (3), (4) => x = 0,3; y = 0,18; z = 0,19; a = 0,14 ${{n}_{{{H}_{2}}S{{O}_{4}}}}=0,12\Rightarrow {{n}_{BaS{{O}_{4}}}}=0,12$ $\Delta m=34,6{-{m}_{BaS{{O}_{4}}}}-{{m}_{{{H}_{2}}}}=6,36$ => tăng 6,36 gam
Câu 10 :
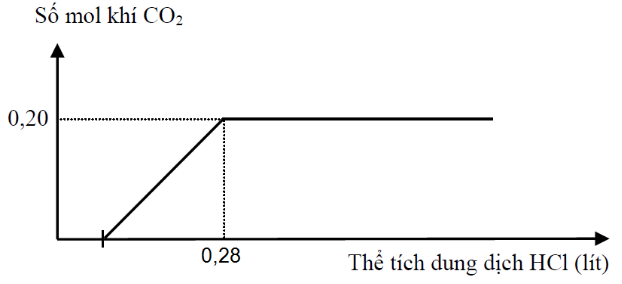
Cho từ từ dung dịch HCl 1M đến dư vào 200 ml dung dịch X chứa Na2CO3 và NaHCO3. Phản ứng được biểu diễn theo đồ thị sau:
Nếu cho từ từ 200 ml dung dịch X vào 175 ml dung dịch HCl 1M, thu được V lít khí CO2 (đktc). Giá trị của V là
Đáp án : C Phương pháp giải :
X chứa ${{n}_{CO_{3}^{2-}}}=a\text{ }v\grave{a}\text{ }{{n}_{HCO_{3}^{-}}}=b$ => nCO2 max => Pt (1) +) nHCl => Pt (2) => a và b => a / b Khi cho từ từ X vào HCl, đặt 2x và 3x là số mol CO32- và HCO3- phản ứng +) Từ nH+ => x => nCO2 Lời giải chi tiết :
X chứa ${{n}_{CO_{3}^{2-}}}=a\text{ }v\grave{a}\text{ }{{n}_{HCO_{3}^{-}}}=b$ => nCO2 max = a + b = 0,2 nHCl = 2a + b = 0,28 => a = 0,08 và b = 0,12 => a/b = 2/3 Khi cho từ từ X vào HCl, đặt 2x và 3x là số mol CO32- và HCO3- phản ứng => nH+ = 2x.2 + 3x = 0,175 => x = 0,025 => nCO2 = 5x = 0,125 => V = 2,8 lít
|














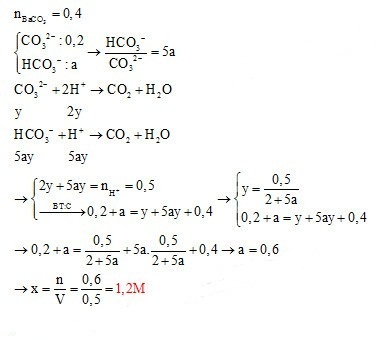
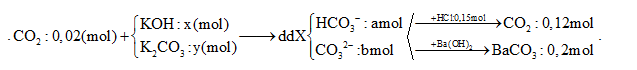
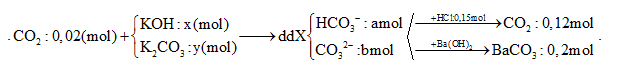
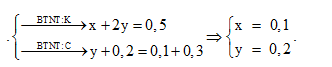
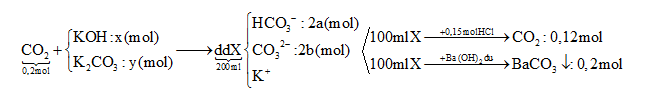
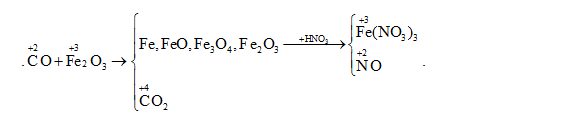





Danh sách bình luận