Trắc nghiệm Bài 7. Nitơ - Hóa 11Đề bài
Câu 1 :
Cấu hình electron lớp ngoài cùng của nguyên tố nitơ là
Câu 2 :
Nhóm nitơ gồm những nguyên tố nào ?
Câu 3 :
Các nguyên tố thuộc nhóm nitơ đều thuộc các nguyên tố họ
Câu 4 :
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là
Câu 5 :
Ở điều kiện thường, nitơ khá trơ về mặt hóa học là do
Câu 6 :
Nitơ thể hiện tính khử khi phản ứng với
Câu 7 :
Nhận xét nào đúng về tính oxi hóa khử của N2 ?
Câu 8 :
Nitơ phản ứng với chất nào sau đây ở điều kiện thường ?
Câu 9 :
Trong công nghiệp thì Nitơ được điều chế bằng phương pháp :
Câu 10 :
Điều chế khí N2 trong phòng thí nghiệm bằng phương trình sau :
Câu 11 :
Điểm giống nhau giữa N2 và CO2 là
Câu 12 :
Cặp công thức của liti nitrua và nhôm nitrua là
Câu 13 :
Mệnh đề nào dưới đây không đúng?
Câu 14 :
Mệnh đề nào dưới đây là không đúng?
Câu 15 :
Mệnh đề nào dưới đây đúng?
Câu 16 :
Trong các hợp chất, nitơ có cộng hóa trị tối đa là
Câu 17 :
Trong các hợp chất, nitơ có thể có các số oxi hóa là
Câu 18 :
Ở điều kiện thường, nitơ phản ứng được với
Câu 19 :
Cho hỗn hợp khí X gồm N2, Cl2, SO2, CO2, H2 qua dung dịch NaOH dư, người ta thu được các khí thoát ra gồm
Câu 20 :
Trong phòng thí nghiệm, người ta thu khí nitơ bằng phương pháp dời nước vì
Câu 21 :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là
Câu 22 :
Một số người lạm dụng bóng cười làm ảnh hưởng xấu đến sức khỏe và hệ thần kinh, khí trong bóng cười là
Câu 23 :
Dãy nào dưới đây gồm các chất mà nguyên tố nitơ có khả năng vừa thể hiện tính khử vừa thể hiện tính oxi hóa khi tham gia phản ứng ?
Câu 24 :
Khối lượng NaNO2 cần dùng trong phòng thí nghiệm để thu được 6,72 lít N2 (đktc) là
Câu 25 :
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm Nitơ là
Câu 26 :
Cây không sử dụng được nitơ phân tử N2 trong không khí vì:
Lời giải và đáp án
Câu 1 :
Cấu hình electron lớp ngoài cùng của nguyên tố nitơ là
Đáp án : B Lời giải chi tiết :
Cấu hình electron lớp ngoài cùng của nguyên tố nitơ là : 2s22p3
Câu 2 :
Nhóm nitơ gồm những nguyên tố nào ?
Đáp án : B Phương pháp giải :
Xem lại lí thuyết nitơ Lời giải chi tiết :
Nhóm nitơ gồm N, P, As, Sb, Bi.
Câu 3 :
Các nguyên tố thuộc nhóm nitơ đều thuộc các nguyên tố họ
Đáp án : B Lời giải chi tiết :
Các nguyên tố thuộc nhóm nitơ đều thuộc các nguyên tố họ p
Câu 4 :
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là
Đáp án : C Lời giải chi tiết :
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là: N2 < O2 < F2.
Câu 5 :
Ở điều kiện thường, nitơ khá trơ về mặt hóa học là do
Đáp án : C Lời giải chi tiết :
Ở điều kiện thường, nitơ khá trơ về mặt hóa học là do phân tử nitơ có liên kết ba khá bền.
Câu 6 :
Nitơ thể hiện tính khử khi phản ứng với
Đáp án : B Lời giải chi tiết :
Nitơ thể hiện tính khử khi phản ứng với chất có tính oxi hóa => O2 ${{N}_{2}}+{{O}_{2}}\overset{{{t}^{o}},xt}{\leftrightarrows}2NO$
Câu 7 :
Nhận xét nào đúng về tính oxi hóa khử của N2 ?
Đáp án : D Lời giải chi tiết :
N2 thể hiện tính khử khi tác dụng với O2 và thể hiện tính oxi hóa khi tác dụng với kim loại (Mg, Li)
Câu 8 :
Nitơ phản ứng với chất nào sau đây ở điều kiện thường ?
Đáp án : D Lời giải chi tiết :
Ở nhiệt độ thường nitơ chỉ tác dụng với liti tạo liti nitrua. 6Li + N2 $\to $ 2Li3N
Câu 9 :
Trong công nghiệp thì Nitơ được điều chế bằng phương pháp :
Đáp án : A Lời giải chi tiết :
Trong công nghiệp thì Nitơ được điều chế bằng phương pháp chưng cất phân đoạn không khí lỏng
Câu 10 :
Điều chế khí N2 trong phòng thí nghiệm bằng phương trình sau :
Đáp án : C Lời giải chi tiết :
Điều chế khí N2 trong phòng thí nghiệm bằng phương trình sau : NH4Cl + NaNO2 $\xrightarrow{{{t}^{o}}}$ N2 + NaCl + 2H2O
Câu 11 :
Điểm giống nhau giữa N2 và CO2 là
Đáp án : C Phương pháp giải :
Cần nắm được tính chất vật lí và tính chất hóa học của N2 và CO2, từ đó suy ra đặc điểm chung. Lời giải chi tiết :
Điểm giống nhau giữa N2 và CO2 là: đều không duy trì sự cháy và sự sống. A sai vì N2 ít tan trong nước B sai vì CO2 chỉ có tính oxi hóa, không có tính khử vì C có số oxi hóa +4 là số oxi hóa cao nhất, còn O có số oxi hóa -2 nhưng không có phản ứng nào để O tạo thành O2 nên O không có tính khử.
Câu 12 :
Cặp công thức của liti nitrua và nhôm nitrua là
Đáp án : B Phương pháp giải :
N2 tác dụng với kim loại thể hiện số oxi hóa -3 => N có hóa trị III Lời giải chi tiết :
Liti nitrua: Li3N Nhôm nitrua: AlN
Câu 13 :
Mệnh đề nào dưới đây không đúng?
Đáp án : C Phương pháp giải :
Nắm được quy luật biến đổi tuần hoàn về tính chất của các nguyên tố hóa học trong cùng 1 nhóm Lời giải chi tiết :
Mệnh đề không đúng là: Tính phi kim của các nguyên tố nhóm VA tăng theo chiều tăng của điện tích hạt nhân. Vì trong cùng một nhóm, theo chiều tăng của điện tích hạt nhân thì độ âm điện giảm => tính phi kim giảm. A đúng vì các nguyên tử của các nguyên tố thuộc nhóm VA có cấu hình e lớp ngoài là ns2np3 B đúng vì nitơ có số hiệu nguyên tử nhỏ nhất D đúng.
Câu 14 :
Mệnh đề nào dưới đây là không đúng?
Đáp án : C Phương pháp giải :
Áp dụng quy luật biến đổi về tính chất của các chất trong cùng 1 nhóm và tính chất riêng của nitơ Lời giải chi tiết :
Mệnh đề không đúng là: So với các nguyên tố cùng nhóm VA, nitơ có tính kim loại mạnh nhất. Vì nitơ có độ âm điện lớn nhất trong nhóm VA => nitơ có tính phi kim mạnh nhất. A đúng B đúng vì độ âm điện của nitơ mạnh nhất => khả năng hút e mạnh nhất => bán kính nhỏ nhất D đúng
Câu 15 :
Mệnh đề nào dưới đây đúng?
Đáp án : B Phương pháp giải :
Xem lại tính chất vật lí và tính chất hóa học của khí nitơ Lời giải chi tiết :
A sai, nitơ không duy trì sự hô hấp vì nitơ là khí trơ, không phải là khí độc. B đúng C sai vì trong phản ứng của nitơ với kim loại thì nitơ thể hiện tính oxi hóa, kim loại thể hiện tính khử D sai vì trong N2O4 nguyên tử N có số oxi hóa +4 \(\overset{+3}{\mathop{Al}}\,\overset{-3}{\mathop{N}}\,,\text{ }{{\overset{+4}{\mathop{N}}\,}_{2}}{{\overset{-2}{\mathop{O}}\,}_{4}},\text{ }\overset{-3}{\mathop{N}}\,{{\overset{+1}{\mathop{H}}\,}_{4}}^{+},\text{ }\overset{+5}{\mathop{N}}\,{{\overset{-2}{\mathop{O}}\,}_{3}}^{-},\text{ }\overset{+4}{\mathop{N}}\,{{\overset{-2}{\mathop{O}}\,}_{2}}\)
Câu 16 :
Trong các hợp chất, nitơ có cộng hóa trị tối đa là
Đáp án : C Phương pháp giải :
Dựa vào cấu hình e nguyên tử của N không có obitan d Lời giải chi tiết :
Trong các hợp chất, nitơ có cộng hóa trị tối đa là: 4 Nguyên tử nitơ không có obitan d trống, nên ở trạng thái kích thích không xuất hiện 5 electron độc thân để tạo thành 5 liên kết cộng hóa trị. Ngoài khả năng tạo 3 liên kết cộng hóa trị bằng sự góp chung electron, nitơ còn có khả năng tạo thêm 1 liên kết cho – nhận. Các nguyên tố còn lại của nhóm VA khi ở trạng thái kích thích nguyên tử của chúng xuất hiện 5 electron độc thân nên có khả năng tạo 5 liên kết cộng hóa trị.
Câu 17 :
Trong các hợp chất, nitơ có thể có các số oxi hóa là
Đáp án : D Phương pháp giải :
Dựa vào cấu hình e của nguyên tử N để giải thích số oxi hóa Lời giải chi tiết :
Trong các hợp chất, nitơ có thể có các số oxi hóa là: -3; +1; +2; +3; +4; +5 Cấu hình e của nguyên tử N:
=> ở trang thái kích thích, nguyên tử N có thể cho từ 1 đến 5e để tạo liên kết => có số oxi hóa từ +1 đến +5 N có thể nhận 3e để tạo liên kết => có số oxi hóa -3
Câu 18 :
Ở điều kiện thường, nitơ phản ứng được với
Đáp án : C Lời giải chi tiết :
Ở nhiệt độ thường nitơ chỉ tác dụng với liti tạo liti nitrua. 6Li + N2 → 2Li3N
Câu 19 :
Cho hỗn hợp khí X gồm N2, Cl2, SO2, CO2, H2 qua dung dịch NaOH dư, người ta thu được các khí thoát ra gồm
Đáp án : D Phương pháp giải :
Các khí bị giữ lại trong dd là các khí có khả năng phản ứng với NaOH Lời giải chi tiết :
Các khí bị giữ lại trong dung dịch NaOH là: Cl2, SO2, CO2 2NaOH + Cl2 → NaCl + NaClO + H2O 2NaOH + SO2 → Na2SO3 + H2O 2NaOH + CO2 → Na2CO3 + H2O => 2 khí thoát ra là N2 và H2
Câu 20 :
Trong phòng thí nghiệm, người ta thu khí nitơ bằng phương pháp dời nước vì
Đáp án : B Lời giải chi tiết :
Trong phòng thí nghiệm, người ta thu khí nitơ bằng phương pháp dời nước vì N2 rất ít tan trong nước.
Câu 21 :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là
Đáp án : C Lời giải chi tiết :
Nitơ có nhiều trong khoáng vật diêm tiêu, diêm tiêu có thành phần chính là: NaNO3
Câu 22 :
Một số người lạm dụng bóng cười làm ảnh hưởng xấu đến sức khỏe và hệ thần kinh, khí trong bóng cười là
Đáp án : B Lời giải chi tiết :
Bóng cười chứa khí N2O.
Câu 23 :
Dãy nào dưới đây gồm các chất mà nguyên tố nitơ có khả năng vừa thể hiện tính khử vừa thể hiện tính oxi hóa khi tham gia phản ứng ?
Đáp án : D Lời giải chi tiết :
Nguyên tố N có các số oxi hóa: -3, 0, +1, + 2, +3, +4, +5 Những nguyên tố N mang số oxi hóa trung gian có khả năng vừa thể hiện tính oxi hóa, vừa thể hiện tính khử khi tham gia phản ứng Trong NH3, Nitơ có số oxi hóa -3, là số oxi hóa thấp nhất nên chỉ thể hiện tính khử. Trong HNO3 và N2O5, N có số oxi hóa +5, là số oxi hóa cao nhất nên chỉ thể hiện tính oxi hóa.
Câu 24 :
Khối lượng NaNO2 cần dùng trong phòng thí nghiệm để thu được 6,72 lít N2 (đktc) là
Đáp án : D Phương pháp giải :
Trong phòng thí nghiệm người ta điều chế N2 bằng phản ứng: NH4Cl + NaNO2 \(\xrightarrow{{{t}^{o}}}\) N2 + NaCl + 2H2O - Tính toán theo PTHH. Lời giải chi tiết :
NH4Cl + NaNO2 \(\xrightarrow{{{t}^{o}}}\) N2 + NaCl + 2H2O Theo PTHH: nNaNO2 = nN2 = 6,72:22,4 = 0,3 mol => mNaNO2 = 0,3.69 = 20,7 gam
Câu 25 :
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm Nitơ là
Đáp án : A Lời giải chi tiết :
N thuộc nhóm VA nên cấu hình có dạng là ns2np3
Câu 26 :
Cây không sử dụng được nitơ phân tử N2 trong không khí vì:
Đáp án : A Phương pháp giải :
Dựa vào đặc điểm liên kết của Nitơ. Lời giải chi tiết :
Cây không sử dụng được nitơ phân tử N2 trong không khí vì phân tử N2 có liên kết ba bền vững cần phải đủ điều kiện mới bẻ gãy được.
|














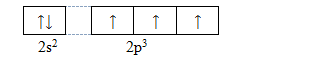





Danh sách bình luận