Trắc nghiệm Bài 4. Nguyên tử - Hóa học 8Đề bài
Câu 1 :
Nguyên tử được tạo bởi các loại hạt
Câu 2 :
Chọn đán án đúng nhất
Câu 3 :
Chọn đáp án sai
Câu 4 :
Đường kính của nguyên tử là
Câu 5 :
Vì sao nguyên tử có khả năng liên kết với nhau?
Câu 6 :
Vì sao khối lượng nguyên tử được coi bằng khối lượng hạt nhân?
Câu 7 :
Trong khoảng không gian giữa hạt nhân và lớp vỏ electron của nguyên tử có những gì?
Câu 8 :
Hạt nhân được cấu tạo bởi:
Câu 9 :
Nguyên tử Cacbon có điện tích hạt nhân là 6+. Số electron lớp ngoài cùng của Cacbon là:
Câu 10 :
Để biểu thị khối lượng của một nguyên tử, người ta dùng đơn vị
Câu 11 :
Nguyên tử nguyên tố A có 3 hạt proton trong hạt nhân. Vậy số hạt electron trong nguyên tử nguyên tố A là
Câu 12 :
Nguyên tử trung hòa về điện vì
Câu 13 :
Một nguyên tử có 17 electron, cấu tạo của nguyên tử đó có bao nhiêu lớp electron?
Câu 14 :
Trong nguyên tử, hạt mang điện là
Câu 15 :
Hạt nhân nguyên tử có cấu tạo bởi các loại hạt:
Câu 16 :
Số proton trong hạt nhân của nguyên tử Fe là:
Câu 17 :
Khẳng định nào sau đây đúng?
Câu 18 :
Số……..là số đặc trưng của một nguyên tố hóa học
Câu 19 :
Nguyên tử oxi có 8 electron. Nguyên tử oxi có :
Câu 20 :
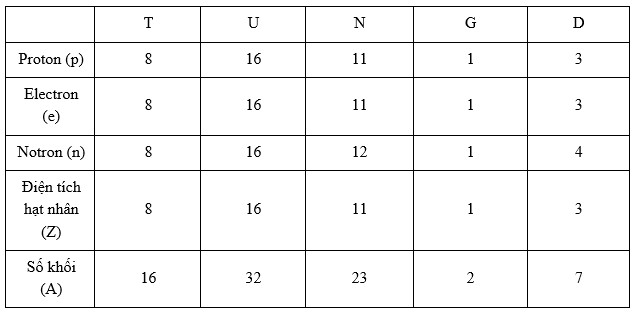
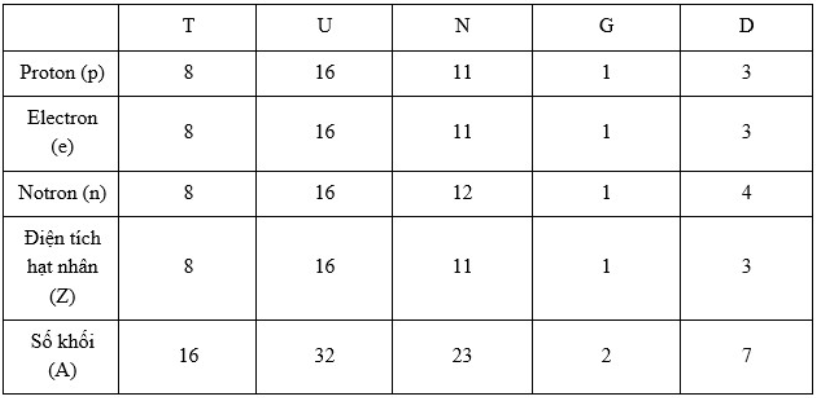
Hoàn thành bảng sau và cho biết nhận định nào không chính xác trong các nhận định sau: 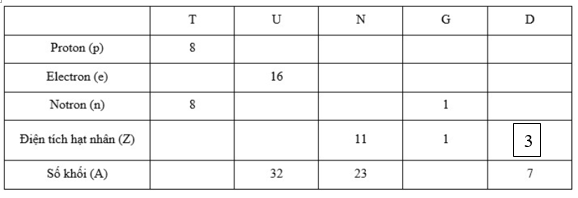
Câu 21 :
Tổng số hạt p,n,e trong 2 nguyên tử kim loại A và B là 177. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 8. Số proton của A là:
Câu 22 :
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Điện tích hạt nhân của X là:
Câu 23 :
Ngtử của nguyên tố Y được cấu tạo bởi 36 hạt .Trong hạt nhân, hạt mang điện dương bằng số hạt không mang điện. Số proton có trong hạt nhân nguyên tử A là?
Câu 24 :
Nguyên tử của một nguyên tố A có tổng số hạt proton, nơtron, electron là 48, trong đó số hạt mang điện gấp hai lần số hạt không mang điện. Số hạt mỗi loại là:
Câu 25 :
Tổng số hạt trong nguyên tử là 36, trong đó số hạt không mang điện chiếm xấp xỉ 50%. Số proton có trong nguyên tử là:
Câu 26 :
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. Tổng số hạt p và n có trong nguyên tử M là:
Câu 27 :
Nguyên tử Nhôm có điện tích hạt nhân là 13+. Trong nguyên tử nhôm, số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Số hạt notron của nhôm là?
Câu 28 :
Nguyên tử B có tổng số hạt là 28. Số hạt không mang điện chiếm 35,7%. Số proton, notron trong B lần lượt là:
Câu 29 :
Mệnh đề nào sau đây không đúng ? (1) Số điện tích hạt nhân đặc trưng cho 1 nguyên tố. (2) Chỉ có hạt nhân nguyên tử oxi mới có 8 proton. (3) Chỉ có hạt nhân nguyên tử oxi mới có 8 nơtron. (4) Chỉ có trong nguyên tử oxi mới có 8 electron.
Lời giải và đáp án
Câu 1 :
Nguyên tử được tạo bởi các loại hạt
Đáp án : B Lời giải chi tiết :
Nguyên tử được tạo bởi các loại hạt electron, proton, nơtron.
Câu 2 :
Chọn đán án đúng nhất
Đáp án : A Lời giải chi tiết :
Đáp án đúng là A. Trong nguyên tử có số p = số e B sai vì hạt nhân tạo bởi proton và nơtron C sai vì các e chuyển động rất nhanh và sắp xếp thành từng lớp từ trong ra ngoài, có một số electron nhất định. D sai.
Câu 3 :
Chọn đáp án sai
Đáp án : D Lời giải chi tiết :
Đáp án sai là: oxi có số p khác số e
Câu 4 :
Đường kính của nguyên tử là
Đáp án : A Lời giải chi tiết :
Đường kính của nguyên tử là 10-8 cm
Câu 5 :
Vì sao nguyên tử có khả năng liên kết với nhau?
Đáp án : A Lời giải chi tiết :
Nguyên tử có khả năng liên kết với nhau do các lớp electron chuyển động xung quanh hạt nhân
Câu 6 :
Vì sao khối lượng nguyên tử được coi bằng khối lượng hạt nhân?
Đáp án : A Lời giải chi tiết :
Khối lượng của hạt: \({{m}_{p}}={{m}_{n}}=1,{{6726.10}^{-27}}kg\) , \({{m}_{e}}=9,{{1094.10}^{-31}}kg\) Như vậy, khối lượng của electron nhỏ hơn nhiều khối lượng proton và notron. Nên khi tính khối lượng tương đối của nguyên tử có thể bỏ qua khối lượng của electron.
Câu 7 :
Trong khoảng không gian giữa hạt nhân và lớp vỏ electron của nguyên tử có những gì?
Đáp án : D Lời giải chi tiết :
Nguyên tử có cấu tạo rỗng => có khoảng không gian trống giữa hạt nhân và lớp vỏ electron của nguyên tử
Câu 8 :
Hạt nhân được cấu tạo bởi:
Đáp án : C Lời giải chi tiết :
Hạt nhân được cấu tạo bởi: Proton và notron
Câu 9 :
Nguyên tử Cacbon có điện tích hạt nhân là 6+. Số electron lớp ngoài cùng của Cacbon là:
Đáp án : B Lời giải chi tiết :
C có 6+ e hạt nhân \( \to\) lớp vỏ ngoài cùng có 4 electron
Câu 10 :
Để biểu thị khối lượng của một nguyên tử, người ta dùng đơn vị
Đáp án : D Phương pháp giải :
Khối lượng của một nguyên tử thường được sử dụng đơn vị là đvC Lời giải chi tiết :
Để biểu thị khối lượng của một nguyên tử, người ta thường dùng đơn vị đvC
Câu 11 :
Nguyên tử nguyên tố A có 3 hạt proton trong hạt nhân. Vậy số hạt electron trong nguyên tử nguyên tố A là
Đáp án : C Phương pháp giải :
Vì nguyên tử trung hòa về điện nên số proton bằng số electron Lời giải chi tiết :
Vì nguyên tử trung hòa về điện nên số electron bằng số hạt proton và bằng 3
Câu 12 :
Nguyên tử trung hòa về điện vì
Đáp án : D Lời giải chi tiết :
Vì trong nguyên tử, số proton = số electron. Mà proton mang điện tích dương, electron mang điện tích âm => Nguyên tử trung hòa về điện
Câu 13 :
Một nguyên tử có 17 electron, cấu tạo của nguyên tử đó có bao nhiêu lớp electron?
Đáp án : B Phương pháp giải :
Trong nguyên tử, các electron chuyển động rất nhanh và sắp xếp thhành từng lớp từ trong ra ngoài, có một số electron nhất định + Lớp 1 có tối đa 2e + Lớp 2, 3, 4… có tối đa 8e Lời giải chi tiết :
Vì nguyên tử có 17e nên sẽ phân bố vào các lớp như sau + Lớp 1: 2e (1s2) + Lớp 2: 8e (2s22p6) + Lớp 3: 7e (3s23p5) Vậy nguyên tử có 3 lớp electron
Câu 14 :
Trong nguyên tử, hạt mang điện là
Đáp án : B Lời giải chi tiết :
Trong nguyên tử, hạt mang điện là hạt proton và hạt electron
Câu 15 :
Hạt nhân nguyên tử có cấu tạo bởi các loại hạt:
Đáp án : B Phương pháp giải :
Đọc lại cấu tạo hạt nhân nguyên tử Lời giải chi tiết :
Hạt nhân cấu tạo bởi: Proton, Nơtron. Chú ý
Học sinh có thể nhầm lẫn cấu tạo nguyên tử mà chọn đáp án 3 loại hạt Electron, Proton, Nơtron.
Câu 16 :
Số proton trong hạt nhân của nguyên tử Fe là:
Đáp án : B Lời giải chi tiết :
Từ hình vẽ cho thấy Fe có tổng 26 e → hạt nhân của Fe có 26 hạt proton
Câu 17 :
Khẳng định nào sau đây đúng?
Đáp án : B Lời giải chi tiết :
A. chưa rõ ràng và đầy đủ B. đúng C. sai vì hạt nhân nguyên tử gồm các hạt proton, notron D. sai vì trong mỗi nguyên tử số proton bằng số electron
Câu 18 :
Số……..là số đặc trưng của một nguyên tố hóa học
Đáp án : A Lời giải chi tiết :
Số Proton là số đặc trưng của một nguyên tố hóa học
Câu 19 :
Nguyên tử oxi có 8 electron. Nguyên tử oxi có :
Đáp án : A Phương pháp giải :
Dựa vào kiến thức về nguyên tử SGK Hóa 8 trang 15 Lời giải chi tiết :
Nguyên tử oxi có 8 proton Nguyên tử oxi có 2 lớp e trong đó có 6 e ở lớp ngoài cùng
Câu 20 :
Hoàn thành bảng sau và cho biết nhận định nào không chính xác trong các nhận định sau: 
Đáp án : C Phương pháp giải :
Số proton(p) = số electron (e) Điên tích hạt nhân (Z) = số proton Số khối (A) = số proton(p) + số notron (n) Dựa vào mối quan hệ trên, các đại lượng nào chưa biết thì đi tìm dựa vào đại lượng đã Lời giải chi tiết :
=> A, B, D đúng còn C sai
Câu 21 :
Tổng số hạt p,n,e trong 2 nguyên tử kim loại A và B là 177. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 8. Số proton của A là:
Đáp án : B Phương pháp giải :
Đặt số proton, notron của A lần lượt là pA, nA Đặt số proton, notron của A lần lượt là pB, nB Nguyên tử trung hòa về điện nên số proton = số notron → eA = pA ; eB = pB Lập phương trình với dữ kiện 177; 47; 8. Sử dụng kiến thức toán học kết hợp 2 phương trình sẽ giải được tổng (pA + pB) và (nA + nB). Sau đó giải ra được riêng pA; pB = ? Lời giải chi tiết :
Đặt số proton, notron của A lần lượt là pA, nA Đặt số proton, notron của A lần lượt là pB, nB Nguyên tử trung hòa về điện nên số proton = số notron → eA = pA ; eB = pB Tổng số hạt p,n,e trong 2 nguyên tử A, B là 142 nên ta có phương trình: (pA + eA + nA) + (pB + eB + nB) = 177 → 2pA + nA + 2pB + nB = 177 → 2pA + 2pB + nA + nB = 177 (1) Trong A, B số hạt mang điện nhiều hơn số hạt không mang điện là 47 nên ta có phương trình (pA + eA + pB + eB) – (nA + nB) = 47 → (2pA + 2pB) – (nA + nB) = 47 (2) Số hạt mang điện của B nhiều hơn A là 8 nên ta có phương trình (pB + eB) – (pA + eA) = 8 → 2pB – 2pA = 8 → pB – pA = 4 (3) Từ (1) và (2) ta có hệ phương trình: \(\left\{ \begin{array}{l}(2{p_A} + 2{p_B}) + ({n_A} + {n_B}) = 177\\(2{p_A} + 2{p_B}) - ({n_A} + {n_B}) = 47\end{array} \right. \Rightarrow \left\{ \begin{array}{l}2{p_A} + 2{p_B} = 112\,(4)\\{n_A} + {n_B} = 65\end{array} \right.\) Từ (3) và (4) kết hợp ta có hệ phương trình: \(\left\{ \begin{array}{l} - {p_A} + {p_B} = 4\,(3)\\2{p_A} + 2{p_B} = 112\,(4)\end{array} \right. \Rightarrow \left\{ \begin{array}{l}{p_A} = 26\\{p_B} = 30\end{array} \right.\)
Câu 22 :
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Điện tích hạt nhân của X là:
Đáp án : D Phương pháp giải :
Bước 1: Lập pt tổng số hạt = p + n + e = 2p + n (do p = e) (1) Bước 2: Lập pt mỗi liên hệ giữa số hạt mang điện (p+e) và không mang điện (n) n =53,125% (p+e) (2) Bước 3: Giải hệ pt (1) (2) tìm p, n Lời giải chi tiết :
Bước 1: Lập pt số hạt cơ bản Tổng số hạt cơ bản trong X là 49 nên ta có: p + e + n = 49 => 2p + n = 49 (do p = e) (1) Bước 2: Lập pt mỗi liên hệ giữa số hạt mang điện (p+e) và không mang điện (n) Số hạt không mang điện bằng 53,125% số hạt mang điện => \(n = \frac{{53,125\% }}{{100\% }}(p + e)\,hay\,n = \frac{{53,125\% }}{{100\% }}.2p\,(2)\) Bước 3: Giải hệ pt (1) (2) tìm p, n Từ (1) và (2) ta có hệ phương trình: \(\left\{ \begin{array}{l}2p + n = 49\\0,53125.2p - n = 0\end{array} \right. \Rightarrow \left\{ \begin{array}{l}p = 16\\n = 17\end{array} \right.\) Số điện tích hạt nhân: Z = số p = 16
Câu 23 :
Ngtử của nguyên tố Y được cấu tạo bởi 36 hạt .Trong hạt nhân, hạt mang điện dương bằng số hạt không mang điện. Số proton có trong hạt nhân nguyên tử A là?
Đáp án : A Phương pháp giải :
Tổng số hạt của nguyên tử là p, n, e → lập phương trình với dữ kiện 36 Trong hạt nhân, hạt không mang điện là n; hạt mang điện là p → lập được phương trình hóa học hai hạt bằng nhau. giải ra được p và n. Từ đó tính được: Z = số p ; số khối A = p + n =? Lời giải chi tiết :
Đặt số proton, notron của nguyên tử Y lần lượt là p và n Nguyên tử trung hòa về điện nên số e = số p = p (hạt) Tổng số hạt trong Y là 36 → p + e + n = 36 hay 2p + n = 36 (1) Trong hạt nhân, hạt mang điện dương bằng hạt không mang điện nên: p = n (2) Từ (1) và (2) ta có hệ phương trình: \(\left\{ \begin{array}{l}2p + n = 36\\p = n\end{array} \right. \Rightarrow p = n = \frac{{36}}{3} = 12\) (hạt)
Câu 24 :
Nguyên tử của một nguyên tố A có tổng số hạt proton, nơtron, electron là 48, trong đó số hạt mang điện gấp hai lần số hạt không mang điện. Số hạt mỗi loại là:
Đáp án : D Phương pháp giải :
Trong A, tổng số hạt là 48 → p + e + n = 48 Số hạt mang điện gấp hai số hạt không mang điện → (p+e) = 2n Nguyên tử trung hòa về điện nên số e = số p. Thế vào 2 PTHH trên giải được ra p, n = ? Lời giải chi tiết :
Đặt số proton, notron lần lượt là p và n (hạt) Nguyên tử trung hòa về điện nên số electron = số proton = p (hạt) Trong A, tổng số hạt là 48 → p + e + n = 48 hay 2p + n = 48 (1) Số hạt mang điện gấp hai số hạt không mang điện → (p+e) = 2n hay 2p =2n → p = n (2) Từ (1) và (2) ta có hệ phương trình:\(\left\{ \begin{array}{l}2p + n = 48\\p - n = 0\end{array} \right. \Rightarrow p = n = 16\) Vậy số hạt proton, electron, notron đều là 16 hạt
Câu 25 :
Tổng số hạt trong nguyên tử là 36, trong đó số hạt không mang điện chiếm xấp xỉ 50%. Số proton có trong nguyên tử là:
Đáp án : A Phương pháp giải :
Hạt không mang điện là notron, chiếm 50% → n = ? Dựa vào dữ kiện tổng số hạt là 36 tìm được nốt p = e = (36-n)/2 =? Lời giải chi tiết :
Hạt không mang điện là notron, chiếm 50% \( \Rightarrow n = 36 \times \frac{{50\% }}{{100\% }} = 18\)(hạt) Tổng số hạt proton và electron còn lại là: 36 – 18 = 18 (hạt) Nguyên tử trung hòa về điện nên số proton = số electron = 18/2 = 9 (hạt)
Câu 26 :
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. Tổng số hạt p và n có trong nguyên tử M là:
Đáp án : D Phương pháp giải :
Lập phương trình với dữ kiện 1 Lập phương trình với dữ kiện 10 giải hệ được p, n =? Từ đó tìm được số khối: A = p+n Lời giải chi tiết :
Đặt số proton, notron lần lượt là p và n (hạt) Nguyên tử trung hòa về điện nên số electron = số proton = p (hạt) Trong M, số notron nhiều hơn số proton là 1 → n – p = 1 (1) Số hạt mang điện nhiều hơn số hạt không mang điện là 10 → p + e – n = 10 hay 2p – n = 10 (2) Từ (1) và (2) ta có hệ phương trình:\(\left\{ \begin{array}{l}n - p = 1\,\\ - n + 2p = 10\end{array} \right. \Rightarrow \left\{ \begin{array}{l}n = 12\\p = 11\end{array} \right.\) Tổng số hạt p và n có trong nguyên tử M là: p + n = 11 + 12 = 23
Câu 27 :
Nguyên tử Nhôm có điện tích hạt nhân là 13+. Trong nguyên tử nhôm, số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Số hạt notron của nhôm là?
Đáp án : B Phương pháp giải :
Bước 1: Tính số p, e của nhôm Số p = số e = ZAl Bước 2: Lập pt mối quan hệ giữa số hạt mang điện (p + e) và không mang điện (n) Bước 3: Tìm n Lời giải chi tiết :
Bước 1: Tính số p, e của nhôm Số p = số e = ZAl = 13 Bước 2: Số hạt mang điện (p+e) nhiều hơn số hạt không mang điện (n) 12 hạt => (p+e) - n = 12 => 26 - n = 12 => n = 14
Câu 28 :
Nguyên tử B có tổng số hạt là 28. Số hạt không mang điện chiếm 35,7%. Số proton, notron trong B lần lượt là:
Đáp án : A Phương pháp giải :
Hạt không mang điện là notron, chiếm 35,7% → n = ? Dựa vào dữ kiện tổng số hạt là 36 tìm được nốt p = e = (28-n)/2 =? Lời giải chi tiết :
Hạt không mang điện là notron, chiếm 35,7% \( \Rightarrow n = 28 \times \frac{{35,7\% }}{{100\% }} = 10\,\)(hạt) Tổng số hạt proton và electron còn lại là: 28 – 10 = 18 (hạt) Nguyên tử trung hòa về điện nên số proton = số electron = 18/2 = 9 (hạt)
Câu 29 :
Mệnh đề nào sau đây không đúng ? (1) Số điện tích hạt nhân đặc trưng cho 1 nguyên tố. (2) Chỉ có hạt nhân nguyên tử oxi mới có 8 proton. (3) Chỉ có hạt nhân nguyên tử oxi mới có 8 nơtron. (4) Chỉ có trong nguyên tử oxi mới có 8 electron.
Đáp án : A Phương pháp giải :
Dựa vào kiến thức học về nguyên tử. Lời giải chi tiết :
(1) đúng (2) đúng (3) sai vì có thể đồng vị của nitơ cũng có 8 nơtron (4) sai
|



















Danh sách bình luận