Trắc nghiệm Bài 14. Dòng điện trong chất điện phân - Vật Lí 11Đề bài
Câu 1 :
Hạt mang tải điện trong chất điện phân là:
Câu 2 :
Bản chất dòng điện trong chất điện phân là
Câu 3 :
Trong các dung dịch điện phân , các ion mang điện tích âm là
Câu 4 :
Chọn phát biểu đúng?
Câu 5 :
Bản chất của hiện tượng dương cực tan là
Câu 6 :
Hiện tượng điện phân không ứng dụng để
Câu 7 :
Công thức nào sau đây là công thức đúng của định luật Fa-ra-đây?
Câu 8 :
Phát biểu nào sau đây là đúng?
Câu 9 :
Phát biểu nào sau đây không đúng khi khi nói về cách mạ một huy chương bạc:
Câu 10 :
Khi điện phân dương cực tan, nếu tăng cường độ dòng điện và thời gian điện phân lên 2 lần thì khối lượng chất giải phóng ra ở điện cực.
Câu 11 :
Khi điện phân dung dịch AgNO3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 1 h để có 27 gam Ag bám ở cực âm là
Câu 12 :
Điện phân cực dương tan một dung dịch trong 20 phút thì khối lượng cực âm tăng thêm 4 gam. Nếu điện phân trong một giờ với cùng cường độ dòng điện như trước thì khối lượng cực âm tăng thêm là
Câu 13 :
Hai bình điện phân: (FeCl3/Fe và CuSO4/Cu) mắc nối tiếp. Sau một khoảng thời gian, bình thứ nhất giải phóng một lượng sắt là 1,4 g. Lượng đồng giải phóng ở bình thứ hai trong cùng khoảng thời gian đó là bao nhiêu ? Biết nguyên tử lượng của đồng và sắt là 64 và 56, hóa trị của đồng và sắt là 2 và 3.
Câu 14 :
Một bộ nguồn điện gồm $30$ pin mắc thành $3$ nhóm nối tiếp, mỗi nhóm có $10$ pin mắc song song, mỗi pin có suất điện động $0,9V$ và điện trở trong \(0,6\Omega\). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega\) được mắc vào hai cực của bộ nguồn nói trên. Anốt của bình điện phân bằng đồng. Khối lượng đồng bám vào catốt của bình trong thời gian $50$ phút là? Biết đồng có $A = 64, n = 2$
Câu 15 :
Muốn mạ đồng một tấm sắt có diện tích tổng cộng $200cm^2$, người ta dùng tấm sắt làm catốt của một bình điện phân đựng dung dịch $CuSO_4$ và anốt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ $I = 10A$ chạy qua trong thời gian $2$ giờ $40$ phút $50$ giây. Bề dày lớp đồng bám trên mặt tấm sắt là bao nhiêu? Biết đồng có $A = 64$, $n = 2$ và có khối lượng riêng $ρ = 8,9.10^3 kg/m^3$
Câu 16 :
Đồ thị biểu diễn sự phụ thuộc giữa khối lượng chất giải phóng ra ở điện cực của bình điện phân và điện lượng tải qua bình 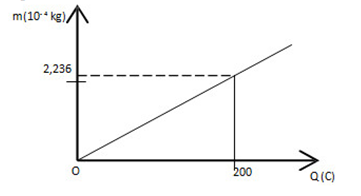 Đương lượng điện hóa của chất điện phân trong bình này là:
Câu 17 :
Bình điện phân có anốt làm bằng kim loại của chất điện phân có hóa trị 2. Cho dòng điện 0,2A chạy qua bình trong 16 phút 5 giây thì có 0,064g chất thoát ra ở điện cực. Kim loại dùng làm anốt của bình điện phân là:
Câu 18 :
Cho mạch điện như hình vẽ: 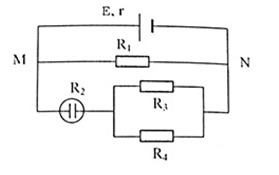 \(E = 13,5V, r = 1\Omega\), \({R_1} = 3\Omega\), \({R_3} = {R_4} = 4\Omega\). Bình điện phân dung dịch CuSO4, anot bằng đồng, có điện trở \({R_2}= 4\Omega\). Cường độ dòng điện qua bình điện phân có giá trị?
Câu 19 :
Cho mạch điện như hình vẽ: 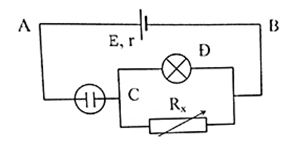 \(E = 9V; r = 0,5\Omega \). Bình điện phân chứa dung dịch đồng sunfat với hai cực bằng đồng. Đèn ghi \(6V - 9W\). \(R_x\) là một biến trở. Điều chỉnh \({R_x} = 12\Omega\) thì đèn sáng bình thường. Điện trở của bình điện phân là:
Câu 20 :
Người ta dùng $36$ nguồn giống nhau, mỗi nguồn có suất điện động \({E_0} = 1,5V\), điện trở trong \(r = 0,9\Omega \) để cung cấp điện cho một bình điện phân đựng dung dịch ZnSO4 với cực dương bằng kẽm, có điện trở \(R = 3,6\Omega \). Mắc hỗn hợp đối xứng bộ nguồn sao cho dòng điện qua bình điện phân là lớn nhất. Tính lượng kẽm bám vào catốt của bình điện phân trong thời gian $1$ giờ $4$ phút $20$ giây. Biết kẽm có $A = 65, n = 2$.
Câu 21 :
Cho mạch điện như hình vẽ: Nguồn điện có suất điện động \(E = 12V\), điện trở trong r = \(1\Omega \), \({R_2} = 12\Omega \) và là bình điện phân đựng dung dịch \(AgN{O_3}\) với điện cực anôt bằng bạc, \({R_1} = 3\Omega \), \({R_3} = 6\Omega \). Cho biết bạc (Ag) có khối lượng mol là 108g/mol, hóa trị 1, hằng số Faraday F = 96500C/mol. Khối lượng bạc bám vào catot sau thời gian 16 phút 5 giây là
Câu 22 :
Một bình điện phân đựng dung dịch CuSO4 có anốt bằng đồng. Hiệu điện thế đặt vào hai cực là 6 V. Sau 16 phút 5 giây, lượng đồng bám vào cực âm là 0,48 g (Cho Cu có A = 64, n = 2). Điện trở của bình điện phân là
Câu 23 :
Một bình điện phân dung dịch CuSO4 có anốt làm bằng đồng, điện trở của bình điện phân R = 8(Ω), được mắc vào hai cực của bộ nguồn E = 9(V), điện trở trong r = 1(Ω). Cho ACu = 64(đvc), nCu=2. Khối lượng Cu bám vào ca tốt trong thời gian 5h có giá trị là:
Câu 24 :
Dòng điện trong chất điện phân là dòng dịch chuyển của các ion dương và ion âm trong dung dịch. Điện tích của ion trong dung dịch không thể nhận giá trị nào dưới đây?
Câu 25 :
Cho dòng điện không đổi có cường độ 4 A chạy qua bình điện phân chứa dung dịch bạc nitrat (AgNO3) với anôt bằng bạc, catôt bằng than chì. Biết bạc có khối lượng mol nguyên tử A = 108 g/mol, có hóa trị n = 1. Lấy số Fa-ra-đây F = 96500 C/mol. Khối lượng bạc bám vào catôt của bình điện phân sau 965 giây là
Câu 26 :
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống. Hiện nay công nghệ mạ thường dùng công nghệ điện phân. Bể điện phân lúc này gọi là bể mạ có anot là một tấm kim loại để mạ, catot là vật cần mạ. Chất điện phân thường dùng là dung dịch muối kim loại để mạ trong đó có thêm một số chất phụ gia để làm cho lớp mạ bám vào bề mặt được chắc, bền và bóng đẹp. Muốn mạ đồng một tấm sắt có diện tích tổng cộng \(200\,\,c{m^2}\), người ta dùng tấm sắt làm catot của một bình điện phân đựng dung dịch \(CuS{O_4}\) và anot là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10\,\,A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64\,\,\left( {g/mol} \right);\,\,n = 2\) và có khối lượng riêng \(\rho = 8,{9.10^3}\,\,kg/{m^3}\).
Câu 27 :
Ứng dụng nào sau đây là của hiện tượng điện phân?
Câu 28 :
Bản chất dòng điện trong chất điện phân là:
Câu 29 :
Cho dòng điện có cường độ 2A chạy qua bình điện phân đựng dung dịch muối đồng có cực dương bằng đồng trong 1 giờ 4 phút 20 giây. Biết khối lượng mol của đồng là 64g/mol, đồng có hóa trị 2. Khối lượng đồng bám vào cực âm là
Câu 30 :
Hiện tượng điện phân không ứng dụng để
Câu 31 :
Chiều dày của lớp Niken phủ lên một tấm kim lọai là d = 0,05 (mm) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là \(30c{m^2}\). Cho biết Niken có khối lượng riêng là \(\rho {\rm{ \;}} = 8,{9.10^3}kg/{m^3}\), nguyên tử khối A = 58 và hoá trị n = 2. Cường độ dòng điện qua bình điện phân là:
Câu 32 :
Cho mạch điện như hình vẽ nguồn điện có suất điện động E=12V, điện trở trong \(1\Omega ,{{\rm{R}}_2} = 12\Omega \) là bình điện phân đựng dung dịch \({\rm{AgN}}{{\rm{O}}_3}\) với điện cực Anôt là bạc, \({{\rm{R}}_1} = 3\Omega \), \({{\rm{R}}_3} = 6\Omega \). Cho Ag có A = 108g/mol, n = 1. Khối lượng Ag bám vào catot sau 8 phút 5 giây là
Câu 33 :
Khi nhiệt độ tăng thì điện trở của chất điện phân
Lời giải và đáp án
Câu 1 :
Hạt mang tải điện trong chất điện phân là:
Đáp án : A Lời giải chi tiết :
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion dương theo chiều điện trường và các ion âm ngược chiều điện trường.
Câu 2 :
Bản chất dòng điện trong chất điện phân là
Đáp án : D Lời giải chi tiết :
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion dương theo chiều điện trường và các ion âm ngược chiều điện trường. => Bản chất dòng điện trong chất điện phân là dòng ion dương và dòng ion âm chuyển động có hướng theo hai chiều ngược nhau.
Câu 3 :
Trong các dung dịch điện phân , các ion mang điện tích âm là
Đáp án : B Lời giải chi tiết :
Trong các dung dịch điện phân, các ion mang điện tích âm là gốc axít và gốc bazơ
Câu 4 :
Chọn phát biểu đúng?
Đáp án : D Lời giải chi tiết :
Hiện tượng dương cực tan xảy ra khi điện phân một dung dịch muối kim loại mà anốt làm bằng chính kim loại ấy
Câu 5 :
Bản chất của hiện tượng dương cực tan là
Đáp án : C Lời giải chi tiết :
Bản chất của hiện tượng dương cực tan là cực dương của bình điện phân bị tác dụng hóa học tạo thành chất điện phân và tan vào dung dịch
Câu 6 :
Hiện tượng điện phân không ứng dụng để
Đáp án : C Lời giải chi tiết :
Ứng dụng của hiện tượng điện phân gồm: Điều chế hóa chất, luyện kim, mạ điện => Hiện tượng điện phân không ứng dụng để sơn tĩnh điện
Câu 7 :
Công thức nào sau đây là công thức đúng của định luật Fa-ra-đây?
Đáp án : C Lời giải chi tiết :
Biểu thức của định luật Fa-ra-đây: \(m = \frac{1}{F}\frac{A}{n}q = \frac{1}{F}\frac{A}{n}It \to I = \frac{{mFn}}{{At}}\)
Câu 8 :
Phát biểu nào sau đây là đúng?
Đáp án : D Lời giải chi tiết :
Khi có hiện tượng dương cực tan, dòng điện trong chất điện phân tuân theo định luật Ôm
Câu 9 :
Phát biểu nào sau đây không đúng khi khi nói về cách mạ một huy chương bạc:
Đáp án : B Lời giải chi tiết :
Khi mạ điện: + Vật cần được mạ dùng làm cực âm + Kim loại dùng để mạ làm cực dương + Chất điện phân là dung dịch muối của kim loại dùng để mạ => B - Đặt huy chương ở giữa anốt và catốt là sai
Câu 10 :
Khi điện phân dương cực tan, nếu tăng cường độ dòng điện và thời gian điện phân lên 2 lần thì khối lượng chất giải phóng ra ở điện cực.
Đáp án : C Phương pháp giải :
Vận dụng công thức Fa-ra-đây: \(m = \frac{1}{F}.\frac{A}{n}It\) Lời giải chi tiết :
Theo định luật Fa-ra-đây, ta có: \(m = \frac{1}{F}.\frac{A}{n}It\) => Khi tăng I và t lên hai lần thì khối lượng chất giải phóng ra ở điện cực sẽ tăng 4 lần
Câu 11 :
Khi điện phân dung dịch AgNO3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 1 h để có 27 gam Ag bám ở cực âm là
Đáp án : A Phương pháp giải :
Vận dụng công thức Fa-ra-đây: \(m = \frac{1}{F}.\frac{A}{n}It\) => \(I\, = \,\frac{{n.F.m}}{{A.t}}\) Với + m: khối lượng chất giải phóng ở điện cực (gam) + A: khối lượng mol của chất thu được ở điện cực + n: số electron trao đổi ở điện cực + I: cường độ dòng điện (A) + t: thời gian điện phân (s) + F: hằng số Faraday ≈ 96500 C.mol-1 Lời giải chi tiết :
Ta có khối lượng bạc bám ở cực âm: \(m = \frac{1}{F}.\frac{A}{n}It \to I = \frac{{mFn}}{{At}}\) Với m = 27 gam, F = 96500 C.mol-1, n = 1, A = 108, t = 1 giờ = 3600s \( \to I = \frac{{27.96500.1}}{{108.3600}}\, = \,6,7A\)
Câu 12 :
Điện phân cực dương tan một dung dịch trong 20 phút thì khối lượng cực âm tăng thêm 4 gam. Nếu điện phân trong một giờ với cùng cường độ dòng điện như trước thì khối lượng cực âm tăng thêm là
Đáp án : B Phương pháp giải :
Vận dụng công thức Fa-ra-đây: \(m = \dfrac{1}{F}.\dfrac{A}{n}It\) Lời giải chi tiết :
Ta có: + Khi điện phân trong thời gian t1 = 20 phút = 1200s: \({m_1} = 4g = \dfrac{{AI{t_1}}}{{Fn}}\) + Khi điện phân trong thời gian t2 = 1giờ = 3600s: \({m_2} = \dfrac{{AI{t_2}}}{{Fn}}\) \(\dfrac{{{m_2}}}{{{m_1}}} = \dfrac{{{t_2}}}{{{t_1}}} = \dfrac{{3600}}{{1200}} = 3 \to {m_2} = 3{m_1} = 3.4 = 12\,g\)
Câu 13 :
Hai bình điện phân: (FeCl3/Fe và CuSO4/Cu) mắc nối tiếp. Sau một khoảng thời gian, bình thứ nhất giải phóng một lượng sắt là 1,4 g. Lượng đồng giải phóng ở bình thứ hai trong cùng khoảng thời gian đó là bao nhiêu ? Biết nguyên tử lượng của đồng và sắt là 64 và 56, hóa trị của đồng và sắt là 2 và 3.
Đáp án : D Phương pháp giải :
Vận dụng công thức Fa-ra-đây: \(m = \frac{1}{F}.\frac{A}{n}It\) Lời giải chi tiết :
Áp dụng công thức định luật Fa-ra-đây, ta có: \({m_1} = \frac{{A_1I_1{t}}}{{Fn_1}}\) (1) \({m_2} = \frac{{A_2I_2{t}}}{{Fn_2}}\) (2) Do 2 bình mắc nối tiếp => I1 = I2= I. Chia (2) cho (1) \(\frac{{{m_2}}}{{{m_1}}} = \frac{{\frac{{{A_2}}}{{{n_2}}}}}{{\frac{{{A_1}}}{{{n_1}}}}} \to {m_2} = \frac{{{m_1}{A_2}{n_1}}}{{{n_2}{A_1}}} = \frac{{1,4.64.3}}{{2.56}} = 2,4\,g\)
Câu 14 :
Một bộ nguồn điện gồm $30$ pin mắc thành $3$ nhóm nối tiếp, mỗi nhóm có $10$ pin mắc song song, mỗi pin có suất điện động $0,9V$ và điện trở trong \(0,6\Omega\). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega\) được mắc vào hai cực của bộ nguồn nói trên. Anốt của bình điện phân bằng đồng. Khối lượng đồng bám vào catốt của bình trong thời gian $50$ phút là? Biết đồng có $A = 64, n = 2$
Đáp án : A Phương pháp giải :
+ Áp dụng biểu thức tính suất điện động và điện trở trong của bộ nguồn mắc hỗn hợp đối xứng + Áp dụng định luật Ôm cho toàn mạch + Áp dụng công thức định luật Faraday: \(m = \frac{1}{F}\frac{{AIt}}{n}\) Lời giải chi tiết :
Ta có: - Suất điện động của bộ nguồn: Eb = 3E0 = 3.0,9 = 2,7V - Điện trở trong của bộ nguồn: \({r_b} = 3\frac{r}{{10}} = 3.\frac{{0,6}}{{10}} = 0,18\Omega \) - Cường độ dòng điện trong mạch: \(I = \frac{{{E_b}}}{{R + {r_b}}} = \frac{{2,7}}{{205 + 0,18}} = 0,01316\,A\) - Khối lượng đồng bám vào catốt của bình trong thời gian 50 phút là: \(m = \frac{1}{F}\frac{{AIt}}{n} = \frac{{64.0,01316.50.60}}{{96500.2}} = 0,0131g\)
Câu 15 :
Muốn mạ đồng một tấm sắt có diện tích tổng cộng $200cm^2$, người ta dùng tấm sắt làm catốt của một bình điện phân đựng dung dịch $CuSO_4$ và anốt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ $I = 10A$ chạy qua trong thời gian $2$ giờ $40$ phút $50$ giây. Bề dày lớp đồng bám trên mặt tấm sắt là bao nhiêu? Biết đồng có $A = 64$, $n = 2$ và có khối lượng riêng $ρ = 8,9.10^3 kg/m^3$
Đáp án : C Phương pháp giải :
+ Áp dụng công thức định luật Faraday: \(m = \dfrac{1}{F}\dfrac{{AIt}}{n}\) + Áp dụng biểu thức tính khối lượng: $m = ρSh$ Lời giải chi tiết :
Ta có: Khối lượng đồng bám vào tấm sắt: \(m = \dfrac{1}{F}\dfrac{A}{n}It = \dfrac{1}{{96500}}\dfrac{{64}}{2}10.(2.60.60 + 40.60 + 50) = 32g\) Mặt khác, ta có: $m = ρSh$ \( \to h = \dfrac{m}{{\rho S}} = \dfrac{{{{32.10}^{ - 3}}}}{{8,{{9.10}^3}{{.200.10}^{ - 4}}}} = 1,{798.10^{ - 4}}m \approx 0,018cm\)
Câu 16 :
Đồ thị biểu diễn sự phụ thuộc giữa khối lượng chất giải phóng ra ở điện cực của bình điện phân và điện lượng tải qua bình  Đương lượng điện hóa của chất điện phân trong bình này là:
Đáp án : B Phương pháp giải :
Vận dụng biểu thức định luật I - Faraday: m = kq Lời giải chi tiết :
Theo định luật I - Faraday, ta có: m = kq \( \to k = \frac{m}{q} = \frac{{2,{{236.10}^{ - 4}}}}{{200}} = 1,{118.10^{ - 6}}kg/C\)
Câu 17 :
Bình điện phân có anốt làm bằng kim loại của chất điện phân có hóa trị 2. Cho dòng điện 0,2A chạy qua bình trong 16 phút 5 giây thì có 0,064g chất thoát ra ở điện cực. Kim loại dùng làm anốt của bình điện phân là:
Đáp án : C Phương pháp giải :
+ Áp dụng công thức định luật Faraday: \(m = \frac{1}{F}\frac{{AIt}}{n}\) + Sử dụng bảng tuần hoàn hóa học Lời giải chi tiết :
Ta có: Khối lượng chất thoát ra ở điện cực: \(m = \frac{1}{F}\frac{A}{n}It \leftrightarrow 0,064 = \frac{1}{{96500}}\frac{A}{2}.0,2.(16.60 + 5) \to A = 64\) => Kim loại dùng làm anot của bình điện phân là đồng có số khối A = 64
Câu 18 :
Cho mạch điện như hình vẽ:  \(E = 13,5V, r = 1\Omega\), \({R_1} = 3\Omega\), \({R_3} = {R_4} = 4\Omega\). Bình điện phân dung dịch CuSO4, anot bằng đồng, có điện trở \({R_2}= 4\Omega\). Cường độ dòng điện qua bình điện phân có giá trị?
Đáp án : D Phương pháp giải :
+ Áp dụng biểu thức xác định tổng trở + Áp dụng biểu thức định luật Ôm cho toàn mạch, đoạn mạch Lời giải chi tiết :
Mạch ngoài gồm: R1 // [R2 nt (R3 // R4)] \({R_{34}} = \dfrac{{{\rm{ }}{R_3}{R_4}}}{{{\rm{ }}{R_3} + {R_4}}} = {\rm{ }}\dfrac{{4.4}}{{4 + 4}} = 2\Omega \) R234 = R2 + R34 = 4 + 2 = 6$\Omega $ Tổng trở tương đương mạch ngoài: \(R = \dfrac{{{R_1}{R_{234}}}}{{{R_1} + {R_{234}}}} = \dfrac{{3.6}}{{3 + 6}} = 2\Omega \) Áp dụng định luật Ôm cho toàn mạch, ta có: \(I = \dfrac{E}{{R + r}} = \dfrac{{13,5}}{{2 + 1}} = 4,5A\) Hiệu điện thế giữa M,N là: UMN = I.R = 4,5.2 = 9V Cường độ dòng điện qua bình điện phân: \(I' = \dfrac{{{U_{MN}}}}{{{R_{234}}}} = \dfrac{9}{6} = 1,5A\)
Câu 19 :
Cho mạch điện như hình vẽ:  \(E = 9V; r = 0,5\Omega \). Bình điện phân chứa dung dịch đồng sunfat với hai cực bằng đồng. Đèn ghi \(6V - 9W\). \(R_x\) là một biến trở. Điều chỉnh \({R_x} = 12\Omega\) thì đèn sáng bình thường. Điện trở của bình điện phân là:
Đáp án : D Phương pháp giải :
+ Áp dụng biểu thức tính: \(P = \frac{{{U^2}}}{R}\) + Áp dụng biểu thức xác định tổng trở + Áp dụng biểu thức định luật Ôm cho toàn mạch, đoạn mạch Lời giải chi tiết :
Ta có: + Điện trở của đèn: \({R_d} = \frac{{{U^2}}}{P} = \frac{{{6^2}}}{9} = 4\Omega \) + Cường độ dòng điện qua đèn: \({I_d} = \frac{P}{U} = \frac{9}{6} = 1,5A\) + Ud = URx = 6V => Cường độ dòng điện qua Rx: \({I_x} = \frac{{{U_{{R_x}}}}}{{{R_x}}} = \frac{6}{{12}} = 0,5A\) Cường độ dòng điện chính trong mạch: I = Id + Ix = 1,5 + 0,5 = 2A Mặt khác: \(I = \frac{E}{{{R_N} + r}} \to {R_N} = \frac{E}{I} - r = \frac{9}{2} - 0,5 = 4\Omega \) Mạch ngoài gồm: Rb ( điện trở bình điện phân) nt (Rd // Rx) \({R_{dx}} = \frac{{{R_d}{R_x}}}{{{R_d} + {R_x}}} = \frac{{4.12}}{{4 + 12}} = 3\Omega \) \({R_N} = {\rm{ }}{R_b} + {\rm{ }}{R_{dx}} \to {R_b} = 4 - 3 = 1\Omega \)
Câu 20 :
Người ta dùng $36$ nguồn giống nhau, mỗi nguồn có suất điện động \({E_0} = 1,5V\), điện trở trong \(r = 0,9\Omega \) để cung cấp điện cho một bình điện phân đựng dung dịch ZnSO4 với cực dương bằng kẽm, có điện trở \(R = 3,6\Omega \). Mắc hỗn hợp đối xứng bộ nguồn sao cho dòng điện qua bình điện phân là lớn nhất. Tính lượng kẽm bám vào catốt của bình điện phân trong thời gian $1$ giờ $4$ phút $20$ giây. Biết kẽm có $A = 65, n = 2$.
Đáp án : B Phương pháp giải :
+ Áp dụng biểu thức tính suất điện động và điện trở trong của bộ nguồn mắc hỗn hợp đối xứng + Áp dụng định luật Ôm cho toàn mạch + Áp dụng bất đẳng thức cosi + Áp dụng công thức định luật Faraday: \(m = \frac{1}{F}\frac{{AIt}}{n}\) Lời giải chi tiết :
Gọi x - là số nhánh => Số nguồn trên một nhánh là: \(y = \frac{{36}}{x}\) Ta có: + Suất điện động của bộ nguồn: \({E_b} = y{E_0} = \frac{{36}}{x}{E_0} = \frac{{54}}{x}\) + Điện trở trong của bộ nguồn: \({r_b} = \frac{{yr}}{x} = \frac{{\frac{{36}}{x}.0,9}}{x} = \frac{{32,4}}{{{x^2}}}\) Cường độ dòng điện qua mạch: \(I = \frac{{{E_b}}}{{R + {r_b}}} = \frac{{\frac{{54}}{x}}}{{3,6 + \frac{{32,4}}{{{x^2}}}}} = \frac{{54}}{{3,6x + \frac{{32,4}}{x}}}\) Imax khi mẫu min Ta có: \(3,6{\rm{x}} + \frac{{32,4}}{x} \ge 2\sqrt {3,6{\rm{x}}.\frac{{32,4}}{x}} = 21,6\) Dấu “=” xảy ra khi \(3,6{\rm{x}} = \frac{{32,4}}{x} \to x = 3\) Khi đó : Imax = 2,5A Khối lượng kẽm bám vào catốt của bình điện phân trong thời gian 1 giờ 4 phút 20 giây là: \(m = \frac{1}{F}\frac{A}{n}It = \frac{1}{{96500}}\frac{{65}}{2}.2,5.(60.60 + 4.60 + 20) = 3,25g\)
Câu 21 :
Cho mạch điện như hình vẽ: Nguồn điện có suất điện động \(E = 12V\), điện trở trong r = \(1\Omega \), \({R_2} = 12\Omega \) và là bình điện phân đựng dung dịch \(AgN{O_3}\) với điện cực anôt bằng bạc, \({R_1} = 3\Omega \), \({R_3} = 6\Omega \). Cho biết bạc (Ag) có khối lượng mol là 108g/mol, hóa trị 1, hằng số Faraday F = 96500C/mol. Khối lượng bạc bám vào catot sau thời gian 16 phút 5 giây là
Đáp án : A Phương pháp giải :
Điện trở tương đương của đoạn mạch song song: \({R_{//}} = \dfrac{{{R_1}{R_2}}}{{{R_1} + {R_2}}}\) Điện trở tương đương của đoạn mạch nối tiếp: \({R_{nt}} = {R_1} + {R_2}\) Công thức định luật Ôm cho toàn mạch: \(I = \dfrac{E}{{{R_N} + r}}\) Công thức định luật Fa-ra-đây: \(m = \dfrac{1}{F}.\dfrac{A}{n}.It\) Lời giải chi tiết :
Cấu tạo mạch: \(\left( {{R_2}//{R_3}} \right)nt{R_1}\) Ta có: \({R_{23}} = \dfrac{{{R_2}{R_3}}}{{{R_2} + {R_3}}} = \dfrac{{12.6}}{{12 + 6}} = 4\,\,\left( \Omega \right)\) \( \Rightarrow {R_N} = {R_1} + {R_{23}} = 3 + 4 = 7\,\,\left( \Omega \right)\) Áp dụng định luật Ôm cho toàn mạch, ta có: \(I = \dfrac{E}{{{R_N} + r}} = \dfrac{{12}}{{7 + 1}} = 1,5\,\,\left( A \right) = {I_1} = {I_{23}}\) Ta có: \({U_{23}} = {I_{23}}.{R_{23}} = 1,5.4 = 6\,\,\left( V \right) = {U_2} = {U_3}\) \( \Rightarrow {I_2} = \dfrac{{{U_2}}}{{{R_2}}} = \dfrac{6}{{12}} = 0,5\,\,\left( A \right)\) Khối lượng bạc bám vào catot là: \({m_{Ag}} = \dfrac{1}{F}.\dfrac{A}{n}.{I_2}t = \dfrac{1}{{96500}}.\dfrac{{108}}{1}.0,5.\left( {16.60 + 5} \right) = 0,54\,\,\left( g \right)\)
Câu 22 :
Một bình điện phân đựng dung dịch CuSO4 có anốt bằng đồng. Hiệu điện thế đặt vào hai cực là 6 V. Sau 16 phút 5 giây, lượng đồng bám vào cực âm là 0,48 g (Cho Cu có A = 64, n = 2). Điện trở của bình điện phân là
Đáp án : B Phương pháp giải :
Áp dụng định luật faraday \(m = \frac{1}{F}.\frac{A}{n}.I.t\) Lời giải chi tiết :
Cường độ dòng điện chạy qua bình điện phân là \(m = \frac{1}{F}.\frac{A}{n}.I.t = > I = \frac{{m.F.n}}{{A.t}} = \frac{{0,48.96494.2}}{{64.965}} = 1,5A\) Điện trở của bình điện phân là \(R = \frac{\xi }{I} = \frac{6}{{1,5}} = 4\Omega \)
Câu 23 :
Một bình điện phân dung dịch CuSO4 có anốt làm bằng đồng, điện trở của bình điện phân R = 8(Ω), được mắc vào hai cực của bộ nguồn E = 9(V), điện trở trong r = 1(Ω). Cho ACu = 64(đvc), nCu=2. Khối lượng Cu bám vào ca tốt trong thời gian 5h có giá trị là:
Đáp án : A Phương pháp giải :
Sử dụng định luật Ôm cho toàn mạch, công thức tính khối lượng chất tạo thành ở điện cực của bình điện phân Lời giải chi tiết :
Cường độ dòng điện chạy qua bình điện phân là \(I = {E \over {R + r}} = {9 \over {8 + 1}} = 1\left( A \right)\) Khối lượng Cu bám vào ca tốt trong thời gian 5h là \(m = {1 \over F}{A \over n}It = {1 \over {96500}}.{{64} \over 2}.1.5.3600 = 5,97g\)
Câu 24 :
Dòng điện trong chất điện phân là dòng dịch chuyển của các ion dương và ion âm trong dung dịch. Điện tích của ion trong dung dịch không thể nhận giá trị nào dưới đây?
Đáp án : D Phương pháp giải :
Điện tích của ion bằng một số nguyên lần điện tích của electron: \(q = ne\) với \(n \in Z\) Lời giải chi tiết :
Nhận xét: điện tích: \(q = + {4.10^{ - 19}} = 2,5e \Rightarrow k = 2,5\,\,\left( {khong\,\,t/m} \right)\) → điện tích của ion không thể nhận giá trị \( + 4,{0.10^{ - 19}}\,\,C\)
Câu 25 :
Cho dòng điện không đổi có cường độ 4 A chạy qua bình điện phân chứa dung dịch bạc nitrat (AgNO3) với anôt bằng bạc, catôt bằng than chì. Biết bạc có khối lượng mol nguyên tử A = 108 g/mol, có hóa trị n = 1. Lấy số Fa-ra-đây F = 96500 C/mol. Khối lượng bạc bám vào catôt của bình điện phân sau 965 giây là
Đáp án : B Phương pháp giải :
Sử dụng biểu thức tính khối lượng chất bám ở catot của bình điện phân: \(m = \dfrac{1}{F}\dfrac{{{\rm{AIt}}}}{n}\) Lời giải chi tiết :
Khối lượng bạc bám vào catot của bình điện phân sau 965 giây là: \(m = \dfrac{1}{F}.\dfrac{{AIt}}{n} = \dfrac{1}{{96500}}\dfrac{{108.4.965}}{1} = 4,32g\)
Câu 26 :
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống. Hiện nay công nghệ mạ thường dùng công nghệ điện phân. Bể điện phân lúc này gọi là bể mạ có anot là một tấm kim loại để mạ, catot là vật cần mạ. Chất điện phân thường dùng là dung dịch muối kim loại để mạ trong đó có thêm một số chất phụ gia để làm cho lớp mạ bám vào bề mặt được chắc, bền và bóng đẹp. Muốn mạ đồng một tấm sắt có diện tích tổng cộng \(200\,\,c{m^2}\), người ta dùng tấm sắt làm catot của một bình điện phân đựng dung dịch \(CuS{O_4}\) và anot là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10\,\,A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64\,\,\left( {g/mol} \right);\,\,n = 2\) và có khối lượng riêng \(\rho = 8,{9.10^3}\,\,kg/{m^3}\).
Đáp án : A Phương pháp giải :
Khối lượng kim loại bám ở Catot: \(m = \dfrac{1}{F}.\dfrac{A}{n}It\) Thể tích: \(V = d.S = \dfrac{m}{\rho }\) Lời giải chi tiết :
Khối lượng đồng bám trên mặt tấm sắt là: \(m = \dfrac{1}{F}.\dfrac{A}{n}It = \dfrac{1}{{96500}}.\dfrac{{64}}{2}.10.9650 = 32\,\,\left( g \right)\) Thể tích của đồng là: \(V = \dfrac{m}{\rho }\) Lại có: \(V = d.S \Rightarrow \dfrac{m}{\rho } = d.S\) \( \Rightarrow d = \dfrac{m}{{\rho .S}} = \dfrac{{{{32.10}^{ - 3}}}}{{8,{{9.10}^3}{{.200.10}^{ - 4}}}} \approx 1,{8.10^{ - 4}}\,\,\left( m \right) = 0,18\,\,\left( {mm} \right)\)
Câu 27 :
Ứng dụng nào sau đây là của hiện tượng điện phân?
Đáp án : C Phương pháp giải :
Sử dụng ứng dụng hiện tượng điện phân. Lời giải chi tiết :
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống như luyện nhôm, tinh luyện đồng, điều chế clo, xút, mạ điện, đúc điện, ...
Câu 28 :
Bản chất dòng điện trong chất điện phân là:
Đáp án : D Phương pháp giải :
Sử dụng kiến thức về bản chất dòng điện trong chất điện phân. Lời giải chi tiết :
Bản chất dòng điện trong chất điện phân: Dòng điện trong chất điện phân là dòng ion dương và ion âm chuyển động có hướng theo hai chiều ngược nhau.
Câu 29 :
Cho dòng điện có cường độ 2A chạy qua bình điện phân đựng dung dịch muối đồng có cực dương bằng đồng trong 1 giờ 4 phút 20 giây. Biết khối lượng mol của đồng là 64g/mol, đồng có hóa trị 2. Khối lượng đồng bám vào cực âm là
Đáp án : C Phương pháp giải :
Áp dụng công thức: \(m = \frac{1}{F}.\frac{A}{n}.It\) Lời giải chi tiết :
Khối lượng đồng bám vào cực âm là: \(m = \frac{1}{F} \cdot \frac{{AIt}}{n} = \frac{1}{{96500}} \cdot \frac{{64.2.\left( {1.3600 + 4.60 + 20} \right)}}{2} = 2,56(g)\)
Câu 30 :
Hiện tượng điện phân không ứng dụng để
Đáp án : C Phương pháp giải :
Sử dụng ứng dụng của hiện tượng điện phân Lời giải chi tiết :
Hiện tượng điện phân ứng dụng để đúc điện, mạ điện, luyện nhôm ... không dùng để sơn tĩnh điện
Câu 31 :
Chiều dày của lớp Niken phủ lên một tấm kim lọai là d = 0,05 (mm) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là \(30c{m^2}\). Cho biết Niken có khối lượng riêng là \(\rho {\rm{ \;}} = 8,{9.10^3}kg/{m^3}\), nguyên tử khối A = 58 và hoá trị n = 2. Cường độ dòng điện qua bình điện phân là:
Đáp án : A Phương pháp giải :
Áp dụng công thức: \(m = \frac{1}{F}.\frac{A}{n}It\) và \(m = \rho .V\) Lời giải chi tiết :
Khối lượng của lớp Niken là: \(m = \rho .V = \rho .S.h = 8,{9.10^3}{.30.10^{ - 4}}.0,{05.10^{ - 3}} = 1,{335.10^{ - 3}}{\mkern 1mu} \left( {kg} \right)\) Cường độ dòng điện chạy qua bình điện phân là: \(I = \frac{{F.m.n}}{{A.t}} = \frac{{96500.1,{{335.10}^{ - 3}}.2}}{{58.30.60}} = 2,{46.10^{ - 3}}\left( A \right) \approx 2,5\left( {mA} \right)\)
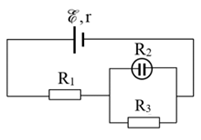
Câu 32 :
Cho mạch điện như hình vẽ nguồn điện có suất điện động E=12V, điện trở trong \(1\Omega ,{{\rm{R}}_2} = 12\Omega \) là bình điện phân đựng dung dịch \({\rm{AgN}}{{\rm{O}}_3}\) với điện cực Anôt là bạc, \({{\rm{R}}_1} = 3\Omega \), \({{\rm{R}}_3} = 6\Omega \). Cho Ag có A = 108g/mol, n = 1. Khối lượng Ag bám vào catot sau 8 phút 5 giây là
Đáp án : D Phương pháp giải :
Áp dụng công thức \(m = \frac{1}{F}.\frac{A}{n}It\) Lời giải chi tiết :
Điện trở mạch ngoài là: \({R_N} = \frac{{{R_2}.{R_3}}}{{{R_2} + {R_3}}} + {R_1} = \frac{{12.6}}{{12 + 6}} + 3 = 7\left( {\Omega {\rm{ \;}}} \right)\) Cường độ dòng điện qua mạch chính là: \(\begin{array}{*{20}{l}}{I = \frac{E}{{r + {R_N}}} = \frac{{12}}{{1 + 7}} = 1,5\left( A \right) = {I_1} = {I_{23}}}\\{ \Rightarrow {U_{23}} = {I_{23}}.{R_{23}} = 1,5.4 = 6\left( V \right) = {U_2} = {U_3}}\end{array}\) Cường độ dòng điện qua bình điện phân là: \(I = \frac{{{U_2}}}{{{R_2}}} = \frac{6}{{12}} = 0,5\left( A \right)\) Khối lượng bạc bám vào catot là: \(m = \frac{1}{F}.\frac{A}{n}It = \frac{1}{{96500}}.\frac{{108}}{1}.0,5.485 \approx 0,27\left( g \right)\)
Câu 33 :
Khi nhiệt độ tăng thì điện trở của chất điện phân
Đáp án : B Phương pháp giải :
Sử dụng lí thuyết về dòng điện trong chất điện phân. Lời giải chi tiết :
Khi nhiệt độ càng tăng thì chất điện li phân li càng tốt → tạo ra nhiều hạt tải điện. → Khi nhiệt độ tăng, điện trở của chất điện phân giảm là do số ion dương và ion âm trong bình điện phân tăng.
|



















Danh sách bình luận