Đề thi giữa kì 2 Hóa 11 Cánh diều - Đề số 2Nhận định nào sau đây sai khi nói về tính chất vật lí của alkaneĐề bài
Câu 1 :
Nhận định nào sau đây sai khi nói về tính chất vật lí của alkane
Câu 2 :
Dãy chất nào sau đây đều thuộc dãy alkane
Câu 3 :
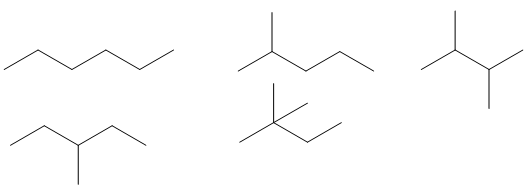
Alkane nào sau đây có mạch phân nhánh
Câu 5 :
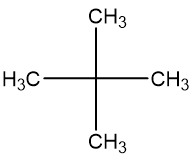
Phân tử khối của alkane X được xác định thông qua phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất = 44. Biết rằng khi X tác dụng với chlorine (1:1) thu được 2 sản phẩm thế chloro. Công thức cấu tạo của đồng phân X:
Câu 6 :
Khi cracking hoàn toàn một thể tích alkane X thu được ba thể tích hỗn hợp Y (các thể tích đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12. Công thức phân tử của X là:
Câu 7 :
Số đồng phân tương ứng với C6H14 là:
Câu 8 :
Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, alcohol methylic,… Thành phần chính của khí thiên nhiên là methane. Công thức phân tử của methane là
Câu 9 :
Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
Câu 10 :
Alkyne CH3-C≡C-CH3 có tên gọi là
Câu 11 :
Sục khí acetylene vào dung dịch AgNO3 trong NH3 thu được kết tủa màu gì?
Câu 12 :
Công thức cấu tạo của 4-methylpent-2-yne là
Câu 13 :
Xăng sinh học E10 là nhiên liệu hỗn hợp giữa (10% ethanol và 90% octane) về khối lượng, còn có tên là gasohol. Hiện nay có khoảng 40 nước trên thế giới đang sử dụng nhiên liệu này trong các động cơ đốt trong của xe hơi và phương tiện giao thông tải trọng nhẹ. Biết rằng nhiệt lượng cháy của nhiên liệu đo ở điều kiện tiêu chuẩn (25 oC, 100 kPa) được đưa trong bảng dưới đây: Để sản sinh năng lượng khoảng 2396 MJ thì cần đốt cháy hoàn toàn bao nhiêu tấn xăng E10 ở điều kiện tiêu chuẩn?
Câu 14 :
Cho các chất sau: CH2=CH-CH2-CH2-CH=CH2, CH2=CH-CH=CH-CH2-CH3, CH3-C(CH3)=CH-CH3, CH2=CH-CH2-CH=CH2. Số chất có đồng phân hình học là
Câu 15 :
Sục từ từ 4,958 lít (đkc) propylene vào bình đựng bromine dư (trong dung môi CCl4), khối lượng brom tối đa phản ứng là
Câu 16 :
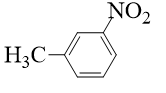
Chất hữu cơ nào sau đây là sản phẩm chính của phản ứng giữa toluene với Br2 đun nóng (có mặt bột Fe, tỉ lệ mol 1: 1)?
Câu 17 :
Cho sơ đồ phản ứng:
Câu 18 :
Khi cho 8 gam một alkyne tác dụng hết với AgNO3 trong NH3 dư, sau khi kết thúc phản ứng thu được 29,4 gam kết tủa. Công thức phân tử của ankin là
Câu 19 :
Khi đốt cháy hoàn toàn hỗn hợp 2 alkane là đồng đẳng kế tiếp, thu 8,6765 lít khí CO2 (đkc) và 9,0 gam H2O. Công thức phân tử của 2 ankan là
Câu 20 :
Cho hỗn hợp X gồm 0,1 mol C2H4 và 0,1 mol CH4 qua 100 gam dung dịch Br2 thấy thoát ra hỗn hợp khí Y có tỉ khối so với H2 là 9,2. Vậy nồng độ phần trăm của dung dịch Br2 là
Câu 22 :
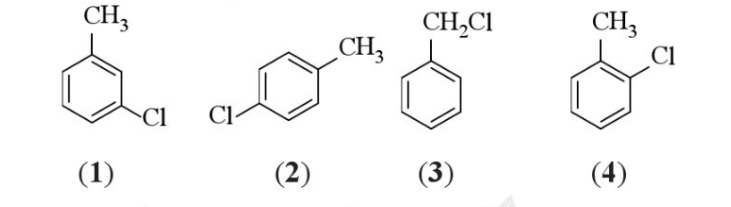
Cho các chất có công thức sau:
Trong các chất trên, những chất nào là sản phẩm chính khi cho toluene tác dụng với chlorine trong điều kiện đung nóng và có mặt FeCl3
Câu 23 :
Cho sơ đồ phản ứng sau: X và Y đều là các sản phẩm hữu cơ. Công thức cấu tạo thu gọn của X, Y lần lượt là:
Câu 24 :
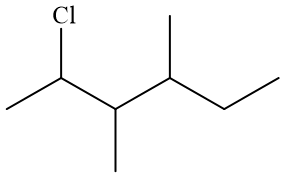
Tên gọi của chất nào sau đây không đúng?
Câu 25 :
Hai hydrocarbon A và B có cùng công thức phân tử là C5H12 tác dụng với chlorine thì A chỉ tạo ra một dẫn xuất monochloro duy nhất, còn B có thể tạo ra 4 dẫn xuất monochloro. Tên gọi của A và B lần lượt là
Câu 26 :
Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là
Câu 27 :
Công thức cấu tạo nào sau đây ứng với tên gọi không đúng?
Câu 28 :
Cho các chất sau: C6H5CH2Cl ; CH3CHClCH3 ; CH3CH2Br ; CH2=CHCH2Cl. Tên gọi gốc - chức của các chất trên lần lượt là
Câu 29 :
Cho dẫn xuất halogen có công thức cấu tạo sau:
Danh pháp thay thế của dẫn xuất halogen trên là
Câu 30 :
Nhiệt độ sôi của các dẫn xuất halogen được sắp xếp theo thứ tự: CH3F < CH3CI < CH3Br < CH3I. Nguyên nhân dẫn đến sự tăng dần nhiệt độ sôi từ CH3F đến CH3I là do
Lời giải và đáp án
Câu 1 :
Nhận định nào sau đây sai khi nói về tính chất vật lí của alkane
Đáp án : C Phương pháp giải :
Dựa vào tính chất vật lí của alkane Lời giải chi tiết :
Các alkane không phân cực nên không tan trong nước Đáp án C
Câu 2 :
Dãy chất nào sau đây đều thuộc dãy alkane
Đáp án : A Phương pháp giải :
Dựa vào công thức tổng quát của dãy alkane: CnH2n+2 Lời giải chi tiết :
Đáp án A
Câu 3 :
Alkane nào sau đây có mạch phân nhánh
Đáp án : B Phương pháp giải :
Dựa vào cấu tạo của alkane Lời giải chi tiết :
Đáp án B
Đáp án : D Phương pháp giải :
Dựa vào tên gọi của alkane X Lời giải chi tiết :
Đáp án D
Câu 5 :
Phân tử khối của alkane X được xác định thông qua phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất = 44. Biết rằng khi X tác dụng với chlorine (1:1) thu được 2 sản phẩm thế chloro. Công thức cấu tạo của đồng phân X:
Đáp án : A Phương pháp giải :
Dựa vào phổ khối lượng để xác định alkane X Lời giải chi tiết :
X có peak ion phân tử có giá trị m/z lớn nhất = 44 => M X = 44 => CTPT: C3H8 Đáp án A
Câu 6 :
Khi cracking hoàn toàn một thể tích alkane X thu được ba thể tích hỗn hợp Y (các thể tích đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12. Công thức phân tử của X là:
Đáp án : D Phương pháp giải :
Dựa vào tỉ khối của Y so với H2 để xác định phân tử khối của Y Lời giải chi tiết :
M Y = 12.2 = 24 Bảo toàn khối lượng: m X = m Y Vì cracking X thu được 3 thể tích hỗn hợp Y => MX = 3 MY => MX = 24.3 = 72 CTPT X: C5H12 Đáp án D
Câu 7 :
Số đồng phân tương ứng với C6H14 là:
Đáp án : A Phương pháp giải :
Viết đồng phân của C6H14 Lời giải chi tiết :
Đáp án A
Câu 8 :
Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, alcohol methylic,… Thành phần chính của khí thiên nhiên là methane. Công thức phân tử của methane là
Đáp án : A Phương pháp giải :
Dựa vào thành phần của khí thiên nhiên Lời giải chi tiết :
Thành phần chính của khí thiên nhiên là methane có công thức CH4 Đáp án A
Câu 9 :
Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
Đáp án : B Phương pháp giải :
Các chất có liên kết đôi trong mạch carbon có khả năng làm mất màu dung dịch Br2 Lời giải chi tiết :
Ethene có liên kết đôi nên làm mất màu Br2 Đáp án B
Câu 10 :
Alkyne CH3-C≡C-CH3 có tên gọi là
Đáp án : B Phương pháp giải :
Dựa vào quy tắc đọc tên của alkyne Lời giải chi tiết :
CH3-C≡C-CH3 : but – 2 – yne Đáp án B
Câu 11 :
Sục khí acetylene vào dung dịch AgNO3 trong NH3 thu được kết tủa màu gì?
Đáp án : A Lời giải chi tiết :
Acetylene tác dụng với AgNO3/NH3 thu được kết tủa vàng Đáp án A
Câu 12 :
Công thức cấu tạo của 4-methylpent-2-yne là
Đáp án : B Phương pháp giải :
Dựa vào tên gọi của alkyne Lời giải chi tiết :
4-methylpent-2-yne: (CH3)2CH-C≡CH-CH3. Đáp án B
Câu 13 :
Xăng sinh học E10 là nhiên liệu hỗn hợp giữa (10% ethanol và 90% octane) về khối lượng, còn có tên là gasohol. Hiện nay có khoảng 40 nước trên thế giới đang sử dụng nhiên liệu này trong các động cơ đốt trong của xe hơi và phương tiện giao thông tải trọng nhẹ. Biết rằng nhiệt lượng cháy của nhiên liệu đo ở điều kiện tiêu chuẩn (25 oC, 100 kPa) được đưa trong bảng dưới đây: Để sản sinh năng lượng khoảng 2396 MJ thì cần đốt cháy hoàn toàn bao nhiêu tấn xăng E10 ở điều kiện tiêu chuẩn?
Đáp án : B Phương pháp giải :
Dựa vào % ethanol và octan trong E10 Lời giải chi tiết :
Gọi khối lượng xăng E10 ở điều kiện tiêu chuẩn là x => khối lượng ethanol là 10%.x = 0,1x; khối lượng octane là: 90%x = 0,9x Nhiệt lượng cháy của ethanol và octane là: 0,1x. 29,6 + 0,9x.47,9 = 2396.103 => x = 52.103 kg = 5,2.10-2 tấn Đáp án B
Câu 14 :
Cho các chất sau: CH2=CH-CH2-CH2-CH=CH2, CH2=CH-CH=CH-CH2-CH3, CH3-C(CH3)=CH-CH3, CH2=CH-CH2-CH=CH2. Số chất có đồng phân hình học là
Đáp án : D Phương pháp giải :
Alkene có đồng phân hình học khi mỗi nguyên tử carbon ở liên kết đôi liên kết với các nguyên tử/nhóm nguyên tử khác nhau Lời giải chi tiết :
CH2=CH-CH=CH-CH2-CH3 Đáp án D
Câu 15 :
Sục từ từ 4,958 lít (đkc) propylene vào bình đựng bromine dư (trong dung môi CCl4), khối lượng brom tối đa phản ứng là
Đáp án : C Phương pháp giải :
Dựa vào phản ứng của propylene với Br2 Lời giải chi tiết :
n CH2=CH-CH3 = 4,598 : 24,79 = 0,2 mol CH2=CH-CH3 + Br2 \( \to \)CH2Br – CHBr – CH3 0,2 0,2 m Br2 = 0,2 . 160 = 32g Đáp án C
Câu 16 :
Chất hữu cơ nào sau đây là sản phẩm chính của phản ứng giữa toluene với Br2 đun nóng (có mặt bột Fe, tỉ lệ mol 1: 1)?
Đáp án : A Phương pháp giải :
Phản ứng thế halogen vào alkybenzene dễ hơn so với benzen và sản phẩm thế ưu tiên vị trí othor hoặc para Lời giải chi tiết :
Đáp án A
Câu 17 :
Cho sơ đồ phản ứng:
Đáp án : B Lời giải chi tiết :
X là acetylene, Y là benzen Đáp án B
Câu 18 :
Khi cho 8 gam một alkyne tác dụng hết với AgNO3 trong NH3 dư, sau khi kết thúc phản ứng thu được 29,4 gam kết tủa. Công thức phân tử của ankin là
Đáp án : D Lời giải chi tiết :
Gọi công thức tổng quát của alkyne: CnH2n-2 CnH2n-2 + AgNO3 + NH3 \( \to \)CnH2n-1Ag + NH4NO3 \(\frac{8}{{14n - 2}}\) \(\frac{{29,4}}{{14n - 1 + 108}}\) Ta có: \(\frac{8}{{14n - 2}}\)=\(\frac{{29,4}}{{14n - 1 + 108}}\)=> x = 3 Vậy alkyne là C3H4 Đáp án D
Câu 19 :
Khi đốt cháy hoàn toàn hỗn hợp 2 alkane là đồng đẳng kế tiếp, thu 8,6765 lít khí CO2 (đkc) và 9,0 gam H2O. Công thức phân tử của 2 ankan là
Đáp án : A Phương pháp giải :
Viết phương trình đốt cháy của alkane Lời giải chi tiết :
n CO2 = 8,6765:24,79 = 0,35 mol n H2O = 9: 18 = 0,5 mol Ta có: n H2O – n CO2 = n alkane => n alkane = 0,5 – 0,35 = 0,15 mol Bảo toàn nguyên tố O: 2 nO2 = 2.nCO2 + nH2O => n O2 = (0,35.2 + 0,5):2 = 0,6 mol Bảo toàn khối lượng: m alkane + m O2 = m CO2 + m H2O => m alkane = 0,35.44 + 0,5.18 – 0,6.32 = 5,2g M alkane = 5,2 : 0,15 = 34,66 => 2 alkane liên tiếp nhau là C2H6 và C3H8 Đáp án A
Câu 20 :
Cho hỗn hợp X gồm 0,1 mol C2H4 và 0,1 mol CH4 qua 100 gam dung dịch Br2 thấy thoát ra hỗn hợp khí Y có tỉ khối so với H2 là 9,2. Vậy nồng độ phần trăm của dung dịch Br2 là
Đáp án : A Lời giải chi tiết :
Vì sau khi hỗn hợp X phản ứng với dung dịch Br2 thu được hỗn hợp khí Y => C2H4 phản ứng dư. Gọi số mol Br2 phản ứng là a mol C2H4 + Br2 \( \to \)C2H4Br a a \(\begin{array}{l}{{\bar M}_Y} = 9,2.2 = 18,4\\{{\bar M}_Y} = \frac{{{m_Y}}}{{{n_Y}}} = \frac{{{m_{CH4}} + {m_{C2H4(du)}}}}{{{n_{CH4}} + {n_{C2H4(du)}}}} = \frac{{01,.16 + (0,1 - a).28}}{{0,1 + 0,1 - a}} = 18,4\\ \to a = 0,075\end{array}\) m Br2 = 0,075 . 160 = 12g => C%Br2 = \(\frac{{12}}{{100}}.100\% = 12\% \) đáp án A
Đáp án : D Phương pháp giải :
Dựa vào danh pháp của arene Lời giải chi tiết :
Đáp án D
Câu 22 :
Cho các chất có công thức sau:
Trong các chất trên, những chất nào là sản phẩm chính khi cho toluene tác dụng với chlorine trong điều kiện đung nóng và có mặt FeCl3
Đáp án : D Phương pháp giải :
Phản ứng thế chlorine vào alkybenzene ưu tiên sản phẩm thế ở vị trí orthor hoặc para Lời giải chi tiết :
(2) và (4) ở vị trí o và p Đáp án D
Câu 23 :
Cho sơ đồ phản ứng sau: X và Y đều là các sản phẩm hữu cơ. Công thức cấu tạo thu gọn của X, Y lần lượt là:
Đáp án : C Phương pháp giải :
Dựa vào tính chất hóa học của arene Lời giải chi tiết :
Vậy X là C6H5COOK và Y là C6H5COOH Đáp án C
Câu 24 :
Tên gọi của chất nào sau đây không đúng?
Đáp án : A Phương pháp giải :
• Tên theo danh pháp thay thế của alkane mạch phân nhánh: Số chỉ vị trí mạch nhánh + tên nhánh + tên alkane mạch chính • Tên của alkene và alkyne mạch không phân nhánh được gọi như sau: Tên tiền tố - số chỉ vị trí liên kết bội – tên hậu tố • Tên của alkene, alkyne có mạch nhánh được gọi như sau: Số chỉ vị trí nhánh – tên mạch nhánh + tên tiền tố (mạch chính) – số chỉ vị trí liên kết bội – tên hậu tố. • Khi gọi theo tên thay thế, vòng benzene được xem là mạch chính. Khi có hai nhóm thế trên vòng benzene, vị trí của chúng có thể được chỉ ra bằng các chữ số 1,2, 1,3 hay 1,4 hoặc bằng các chữ tương ứng là ortho (o), meta (m) hay para (p). Lời giải chi tiết :
Đáp án A
Câu 25 :
Hai hydrocarbon A và B có cùng công thức phân tử là C5H12 tác dụng với chlorine thì A chỉ tạo ra một dẫn xuất monochloro duy nhất, còn B có thể tạo ra 4 dẫn xuất monochloro. Tên gọi của A và B lần lượt là
Đáp án : A Phương pháp giải :
Dựa vào số dẫn xuất monochloro để xác định công thức cấu tạo. Lời giải chi tiết :
Đáp án A
Câu 26 :
Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là
Đáp án : B Phương pháp giải :
Nhóm halogen gắn vào nguyên tử carbon bậc nào thì được dẫn xuất halogen bậc đó Lời giải chi tiết :
2 – iodopropane: CH3 – CHI – CH3 là dẫn xuất halogen bậc II Đáp án B
Câu 27 :
Công thức cấu tạo nào sau đây ứng với tên gọi không đúng?
Đáp án : B Phương pháp giải :
Dựa vào quy tắc đọc tên của dẫn xuất halogen Lời giải chi tiết :
ClCH2Br: chlorobromomethane sai, tên đúng là bromochloromethane Đáp án B
Câu 28 :
Cho các chất sau: C6H5CH2Cl ; CH3CHClCH3 ; CH3CH2Br ; CH2=CHCH2Cl. Tên gọi gốc - chức của các chất trên lần lượt là
Đáp án : A Phương pháp giải :
Dựa vào tên gọi của dẫn xuất halogen Lời giải chi tiết :
C6H5CH2Cl: benzyl chloride; CH3CHClCH3: isopropyl chloride; CH3CH2Br: ethyl bromide; CH2=CHCH2Cl: allyl chloride Đáp án A
Câu 29 :
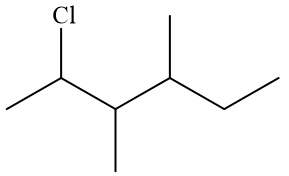
Cho dẫn xuất halogen có công thức cấu tạo sau:
Danh pháp thay thế của dẫn xuất halogen trên là
Đáp án : B Phương pháp giải :
Dựa vào quy tắc đọc tên của dẫn xuất halogen Lời giải chi tiết :
Đáp án B
Câu 30 :
Nhiệt độ sôi của các dẫn xuất halogen được sắp xếp theo thứ tự: CH3F < CH3CI < CH3Br < CH3I. Nguyên nhân dẫn đến sự tăng dần nhiệt độ sôi từ CH3F đến CH3I là do
Đáp án : C Lời giải chi tiết :
Do tương tăng van der Waals tăng dần từ CH3F đến CH3I Đáp án C
|

























Danh sách bình luận