Trắc nghiệm Bài 2. Nguyên tố hóa học - Hóa 10 Kết nối tri thứcĐề bài
Câu 1 :
Nguyên tố hóa học là những nguyên tử có cùng
Câu 2 :
Kí hiệu nguyên tử biểu thị đầy đủ đặc trưng cho một nguyên tử của một nguyên tố hóa học vì nó cho biết
Câu 3 :
Nguyên tố carbon có hai đồng vị bền: \({}_6^{12}C\) chiếm 98,89% và \({}_6^{13}C\) chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố carbon là
Câu 4 :
Trong dãy kí hiệu các nguyên tử sau: \({}_7^{14}A\), \({}_9^{19}B\), \({}_{26}^{56}E\), \({}_{27}^{56}F\), \({}_8^{17}G\), \({}_{10}^{20}H\), \({}_{11}^{23}I\), \({}_{10}^{22}K\) Các kí hiệu nào chỉ cùng 1 nguyên tố hóa học?
Câu 5 :
Cho ba nguyên tử có kí hiệu là \({}_{12}^{24}Mg\), \({}_{12}^{25}Mg\), \({}_{12}^{26}Mg\). Phát biểu nào sau đây sai?
Câu 6 :
Điện tích hạt nhân của nguyên tử chlorine có 17 electron là
Câu 7 :
Số neutron trong nguyên tử \({}_3^7Li\) là
Câu 8 :
Cho các nguyên tử X, Y, Z, T có các đặc điểm như sau: (1) nguyên tử X có 17 proton và số khối bằng 35 (2) nguyên tử Y có 17 neutron và số khối bằng 33 (3) nguyên tử Z có 17 neutron và 15 proton (4) nguyên tử T có 20 neutron và số khối bằng 37 Những nguyên tử là đồng vị của cùng một nguyên tố hóa học là
Câu 9 :
Nguyên tử A có 12 electron, 12 neutron, kí hiệu nguyên tử của A là
Câu 10 :
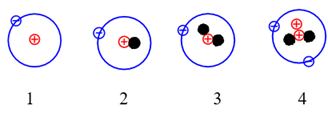
Cho những nguyên tử của các nguyên tố sau:
Những nguyên tử nào sau đây là đồng vị của nhau ?
Câu 11 :
Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3p1 . Số hiệu nguyên tử của nguyên tố X là
Câu 12 :
Nguyên tố X có 2 đồng vị bền X1 và X2. Đồng vị X1 có tổng số hạt là 18. Đồng vị X2 có tổng số hạt là 20. Biết rằng phần trăm số nguyên tử các đồng vị bằng nhau và các loại hạt trong X1 cũng bằng nhau. Nguyên tử khối trung bình của X là
Câu 13 :
Cho phổ khối của nguyên tố A được biểu diễn tại hình 1.33, Nguyên tử khối trung bình của A là
Câu 14 :
Phổ khối lượng của nguyên tố X được cho ở hình 1.34. Nguyên tử khối trung bình của nguyên tố này là bao nhiêu?
Câu 15 :
Trong tự nhiên, nguyên tử Chlorine có hai đồng vị bền là 35Cl và 37Cl. Tại sao nguyên tử khối tương đối của Chlorine thường được sử dụng là 35,5?
Câu 16 :
Nguyên tố X có ba đồng vị bền, thông tin về phần trăm số lượng nguyên tử tương ứng của từng đồng vị được cho trong bảng sau:
Phần trăm số lượng nguyên tử các đồng vị bền của X Nguyên tử khối trung bình của nguyên tố X là
Câu 17 :
Tai nạn hạt nhân tại Nhật Bản đã sinh ra một lượng rất nhỏ 131I, sự có mặt của 131I trong không khí có thể gây ung thư tuyến giáp khi con người tiếp xúc với nó; vậy nhưng khác với 131I, 127I lại là nguyên tố vi lượng cần thiết cho cơ thể con người với vai trò ngăn chặn sự hấp thụ phóng xạ 131I của tuyến giáp. Ngoài ra người sử dụng đủ hàm lượng 127I có tác dụng ngăn ngừa bệnh bướu cổ. Khẳng định nào sau đây là sai ?
Câu 18 :
Trong tự nhiên, nguyên tố Copper có hai đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Copper là 63,54. Thành phần % số nguyên tử của đồng vị 65Cu là
Câu 19 :
Argon được sử dụng trong các loại đèn điện vì nó không phản ứng với dây tóc bóng đèn ngay cả trong nhiệt độ cao, tạo môi trường luyện kim cho các nguyên tố có hoạt tính cao, là lớp khí bảo vệ để nuôi cấy các tinh thể silicon và gecmani trong công nghiệp sản xuất chất bán dẫn và là chất khí dùng trong các đèn plasma.Nguyên tố Argon có 3 loại đồng vị có số khối bằng 36; 38 và A. Phần trăm số nguyên tử tương ứng của 3 đồng vị lần lượt bằng 0,34%; 0,06% và 99,6%. Biết 125 nguyên tử Ar có khối lượng 4997,5 đvc. Số khối A của đồng vị thứ 3 là:
Câu 20 :
Một nguyên tố có 2 đồng vị mà số khối là 2 số nguyên liên tiếp và có tổng bằng 29. Biết rằng đồng vị nhẹ nhất có số proton bằng số số nơtron. Số nơtron của hai đồng vị lần lượt là:
Lời giải và đáp án
Câu 1 :
Nguyên tố hóa học là những nguyên tử có cùng
Đáp án : C Phương pháp giải :
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân Lời giải chi tiết :
- Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân - Số đơn vị điện tích hạt nhân = số proton => Nguyên tố hóa học là những nguyên tử có cùng số proton
Câu 2 :
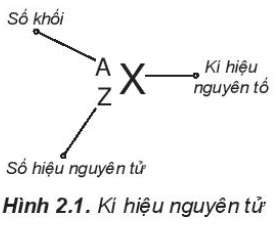
Kí hiệu nguyên tử biểu thị đầy đủ đặc trưng cho một nguyên tử của một nguyên tố hóa học vì nó cho biết
Đáp án : D Phương pháp giải :
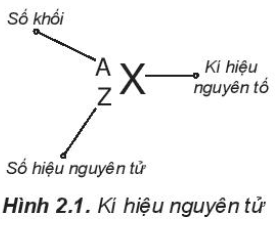
Lời giải chi tiết :
Dựa vào Hình 2.1, có thể thấy số đơn vị điện tích hạt nhân (Z) và số khối (A) được coi là những đặc trung cơ bản của nguyên tử
Câu 3 :
Nguyên tố carbon có hai đồng vị bền: \({}_6^{12}C\) chiếm 98,89% và \({}_6^{13}C\) chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố carbon là
Đáp án : B Phương pháp giải :
Nguyên tử khối trung bình:\(M = \frac{{aA + bB + cC + {\text{dD}} + ...}}{{100}}\) Trong đó: A, B, C, D… là số khối của các đồng vị a, b, c, d… là phần trăm của các đồng vị tương ứng Lời giải chi tiết :
Ta có: \({}^{12}C\)chiếm 98,89%; \(^{13}C\)chiếm 1,11% => \({M_C} = \frac{{98,89.12 + 1,11.13}}{{100}} = 12,011\) Vậy nguyên tử khối trung bình của C là 12,011
Câu 4 :
Trong dãy kí hiệu các nguyên tử sau: \({}_7^{14}A\), \({}_9^{19}B\), \({}_{26}^{56}E\), \({}_{27}^{56}F\), \({}_8^{17}G\), \({}_{10}^{20}H\), \({}_{11}^{23}I\), \({}_{10}^{22}K\) Các kí hiệu nào chỉ cùng 1 nguyên tố hóa học?
Đáp án : B Phương pháp giải :
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân Lời giải chi tiết :
H và K cùng 1 nguyên tố hóa học do có cùng số hiệu nguyên tử (số đơn vị điện tích hạt nhân) là 10
Câu 5 :
Cho ba nguyên tử có kí hiệu là \({}_{12}^{24}Mg\), \({}_{12}^{25}Mg\), \({}_{12}^{26}Mg\). Phát biểu nào sau đây sai?
Đáp án : A Lời giải chi tiết :
- Kí hiệu của nguyên tử có dạng với Z là số hiệu nguyên tử, A là số khối - Nhận thấy 3 nguyên tử đều có cùng số Z, khác số khối → 3 nguyên tử là đồng vị của nguyên tố Mg → B, C đúng Luôn có Z = số p = số e = 12
Câu 6 :
Điện tích hạt nhân của nguyên tử chlorine có 17 electron là
Đáp án : C Phương pháp giải :
Điện tích hạt nhân nguyên tử = số electron = số proton Lời giải chi tiết :
Nếu hạt nhân có Z proton, thì điện tích của hạt nhân sẽ bằng Z+ Chlorine có 17 electron => Có 17 proton => Điện tích hạt nhân = 17+
Câu 7 :
Số neutron trong nguyên tử \({}_3^7Li\) là
Đáp án : D Phương pháp giải :
Lời giải chi tiết :
- Số khối A = Z + N => 7 = 3 + N => N = 4 Vậy số neutron của nguyên tử \({}_3^7Li\) là 4
Câu 8 :
Cho các nguyên tử X, Y, Z, T có các đặc điểm như sau: (1) nguyên tử X có 17 proton và số khối bằng 35 (2) nguyên tử Y có 17 neutron và số khối bằng 33 (3) nguyên tử Z có 17 neutron và 15 proton (4) nguyên tử T có 20 neutron và số khối bằng 37 Những nguyên tử là đồng vị của cùng một nguyên tố hóa học là
Đáp án : D Phương pháp giải :
Các nguyên tử có cùng số proton là đồng vị của cùng 1 nguyên tố hóa học Lời giải chi tiết :
- Nguyên tử X có 17 proton, nguyên tử Y có 16 proton, nguyên tử Z có 15 proton, nguyên tử T có 17 proton => Nguyên tử X và T là đồng vị của cùng một nguyên tố hóa học (đều có 17 proton)
Câu 9 :
Nguyên tử A có 12 electron, 12 neutron, kí hiệu nguyên tử của A là
Đáp án : D Phương pháp giải :
Dựa vào kí hiệu của nguyên tử Lời giải chi tiết :
Vì nguyên tử A có 12e => E = P =12 Số khối A = 12 + 12 = 24 Vậy kí hiệu của A là: \({}_{12}^{24}A\) Đáp án D
Câu 10 :
Cho những nguyên tử của các nguyên tố sau:
Những nguyên tử nào sau đây là đồng vị của nhau ?
Đáp án : C Phương pháp giải :
Các nguyên tử nguyên tố có cùng số proton khác nhau về neutron được gọi là đồng vị của nhau Lời giải chi tiết :
1, 2, 3 cùng có 1 proton Đáp án C
Câu 11 :
Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3p1 . Số hiệu nguyên tử của nguyên tố X là
Đáp án : A Phương pháp giải :
Dựa vào số proton của nguyên tử X Lời giải chi tiết :
Nguyên tử X có 3 lớp electron => lớp 1 có 2 electron, lớp 2 có 8 electron, lớp 3 có 3 electron (vì lớp ngoài cùng nguyên tử X là 3p1) => có tổng: 2 + 8 + 3 = 13 electron Đáp án A
Câu 12 :
Nguyên tố X có 2 đồng vị bền X1 và X2. Đồng vị X1 có tổng số hạt là 18. Đồng vị X2 có tổng số hạt là 20. Biết rằng phần trăm số nguyên tử các đồng vị bằng nhau và các loại hạt trong X1 cũng bằng nhau. Nguyên tử khối trung bình của X là
Đáp án : D Phương pháp giải :
Tính số e, p, n của X Lời giải chi tiết :
Tổng số hạt trong X1: p + n + e = 18 Vì các loại hạt trong X1 bằng nhau => p = e = n = 6 Vì X1 và X2 là đồng vị của nhau nên số proton của X2 = 6 Các hạt trong X2: p = e = 6 => n = 20 – 6 – 6 = 8 Nguyên tử khối X1 = 6 + 6 = 12; nguyên tử khối X2 = 8 + 6 = 14 Nguyên tử khối trung bình của X là: (12 + 14 ): 2 = 13 Đáp án D
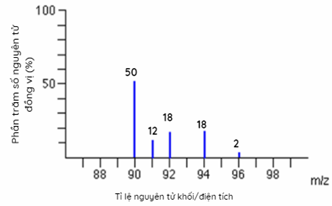
Câu 13 :
Cho phổ khối của nguyên tố A được biểu diễn tại hình 1.33, Nguyên tử khối trung bình của A là
Đáp án : A Phương pháp giải :
Dựa vào phần trăm số nguyên tử các đồng vị Lời giải chi tiết :
Nguyên tử khối trung bình của A: (90.50 + 12.91 + 18.92 + 18.94 + 96.2) : 100 = 91,32 Đáp án A
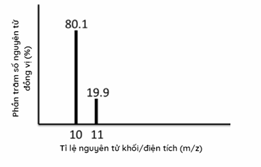
Câu 14 :
Phổ khối lượng của nguyên tố X được cho ở hình 1.34. Nguyên tử khối trung bình của nguyên tố này là bao nhiêu?
Đáp án : C Phương pháp giải :
Dựa vào phần trăm số nguyên tử đồng vị Lời giải chi tiết :
Nguyên tử khối trung bình của X: (80,1.10 + 19,9.11):100 = 10,2 Đáp án C
Câu 15 :
Trong tự nhiên, nguyên tử Chlorine có hai đồng vị bền là 35Cl và 37Cl. Tại sao nguyên tử khối tương đối của Chlorine thường được sử dụng là 35,5?
Đáp án : D Phương pháp giải :
Dựa vào kiến thức về đồng vị Lời giải chi tiết :
Vì giá trị 35,5 là nguyên tử khối trung bình của hai đồng vị Đáp án D
Câu 16 :
Nguyên tố X có ba đồng vị bền, thông tin về phần trăm số lượng nguyên tử tương ứng của từng đồng vị được cho trong bảng sau:
Phần trăm số lượng nguyên tử các đồng vị bền của X Nguyên tử khối trung bình của nguyên tố X là
Đáp án : C Phương pháp giải :
Dựa vào phần trăm số lượng nguyên tử Lời giải chi tiết :
Nguyên tử khối trung bình của X là: (24.79 + 25.10 + 26.11) : 100 = 24,32 Đáp án C
Câu 17 :
Tai nạn hạt nhân tại Nhật Bản đã sinh ra một lượng rất nhỏ 131I, sự có mặt của 131I trong không khí có thể gây ung thư tuyến giáp khi con người tiếp xúc với nó; vậy nhưng khác với 131I, 127I lại là nguyên tố vi lượng cần thiết cho cơ thể con người với vai trò ngăn chặn sự hấp thụ phóng xạ 131I của tuyến giáp. Ngoài ra người sử dụng đủ hàm lượng 127I có tác dụng ngăn ngừa bệnh bướu cổ. Khẳng định nào sau đây là sai ?
Đáp án : C Lời giải chi tiết :
131I và 127 I là hai nguyên tố hóa học khác nhau. Đáp án C
Câu 18 :
Trong tự nhiên, nguyên tố Copper có hai đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Copper là 63,54. Thành phần % số nguyên tử của đồng vị 65Cu là
Đáp án : A Phương pháp giải :
Dựa vào nguyên tử khối trung bình của Cu Lời giải chi tiết :
Gọi % đồng vị 63Cu và 65Cu lần lượt là a và b Ta có: a + b = 100 \({\bar M_{Cu}} = \frac{{a.63 + b.65}}{{100}} = 63,54\) => a = 73%; b = 27% Đáp án A
Câu 19 :
Argon được sử dụng trong các loại đèn điện vì nó không phản ứng với dây tóc bóng đèn ngay cả trong nhiệt độ cao, tạo môi trường luyện kim cho các nguyên tố có hoạt tính cao, là lớp khí bảo vệ để nuôi cấy các tinh thể silicon và gecmani trong công nghiệp sản xuất chất bán dẫn và là chất khí dùng trong các đèn plasma.Nguyên tố Argon có 3 loại đồng vị có số khối bằng 36; 38 và A. Phần trăm số nguyên tử tương ứng của 3 đồng vị lần lượt bằng 0,34%; 0,06% và 99,6%. Biết 125 nguyên tử Ar có khối lượng 4997,5 đvc. Số khối A của đồng vị thứ 3 là:
Đáp án : A Phương pháp giải :
Dựa vào % các đồng vị của A để tính số khối Lời giải chi tiết :
\(\frac{{36.0,34 + 38.0,06 + A.99,6}}{{100}} = \frac{{4997,5}}{{125}} \Rightarrow A = 40\) Đáp án A
Câu 20 :
Một nguyên tố có 2 đồng vị mà số khối là 2 số nguyên liên tiếp và có tổng bằng 29. Biết rằng đồng vị nhẹ nhất có số proton bằng số số nơtron. Số nơtron của hai đồng vị lần lượt là:
Đáp án : B Phương pháp giải :
Dựa vào kiến thức đồng vị Lời giải chi tiết :
A1 + (A1 + 1) = 29 => A1 = 14 => A2 = 15 N1 = Z = 7; N2 = 15 -7 = 8 Đáp án B
|



















Danh sách bình luận