Trắc nghiệm Bài 13. Liên kết hydrogen và tương tác van der Waals - Hóa 10 Kết nối tri thứcĐề bài
Câu 1 :
Liên kết hydrogen là loại liên kết hóa học được hình thành giữa các nguyên tử nào sau đây?
Câu 2 :
Tương tác van der Waals được hình thành do
Câu 3 :
Chất nào sau đây có thể tạo liên kết hydrogen?
Câu 4 :
Chất nào sau đây không thể tạo được liên kết hydrogen?
Câu 5 :
Tương tác van der Waals tồn tại giữa những
Câu 6 :
Cho các chất sau: . Chất có nhiệt độ sôi cao nhất là
Câu 7 :
Cho các chất sau: CH4, H2O, HF, BF3, C2H5OH, PCl5. Số chất tạo được liên kết hydrogen là
Câu 8 :
Nhiệt độ sôi của từng chất methane, ethane, propane, và butane là 1 trong 4 nhiệt độ sau: 0oC, -164oC, -42oC và -88oC. Nhiệt độ sôi -164oC là của chất nào sau đây?
Câu 9 :
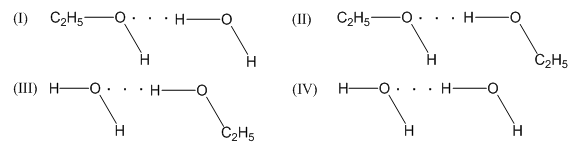
Giữa H2O và C2H5OH có thể tạo ra bao nhiêu kiểu liên kết hydrogen?
Câu 10 :
Cho các khí hiếm sau: He, Ne, Ar, Kr, Xe. Khí hiếm có nhiệt độ nóng chảy thấp nhất và cao nhất lần lượt là
Câu 11 :
Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử?
Câu 12 :
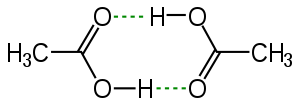
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
Câu 13 :
Sơ đồ nào sau đây thể hiện đúng liên kết hydrogen giữa 2 phân tử hydrogen fluoride (HF)?
Câu 14 :
Điều nào sau đây đúng khi nói về liên kết hydrogen liên phân tử?
Câu 15 :
Điều nào sau đây đúng khi nói về liên kết hydrogen nội phân tử?
Câu 16 :
Phát biểu nào sau đây là đúng?
Câu 17 :
H2O, NH3, HF, H2S, CO2, HCl. Số phân tử có thể tạo liên kết hydrogen với phân tử cùng loại là
Câu 18 :
Cho các chất sau: F2, Cl2, Br2, I2. Chất có nhiệt độ nóng chảy thấp nhất là
Câu 19 :
Cho các chất sau F2, Cl2, Br2, I2. Chất có nhiệt độ sôi cao nhất là
Câu 20 :
Dãy chất nào sau đây xếp theo thứ tự nhiệt độ sôi tăng dần?
Lời giải và đáp án
Câu 1 :
Liên kết hydrogen là loại liên kết hóa học được hình thành giữa các nguyên tử nào sau đây?
Đáp án : D Phương pháp giải :
- Điều kiện cần và đủ để tạo thành liên kết hydrogen: + Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như: F, N, O... + Nguyên tử F, O, N...liên kết với hydrogen phải có ít nhất 1 cặp electron hóa trị chưa liên kết Lời giải chi tiết :
Liên kết hydrogen là loại liên kết hóa học được hình thành giữa các nguyên tử F, N, O,...có độ âm điện lớn, đồng thời có cặp electron hóa trị chưa liên kết và nguyên tử hydrogen linh động
Câu 2 :
Tương tác van der Waals được hình thành do
Đáp án : C Lời giải chi tiết :
Tương tác van der Waals là tương tác tĩnh điện lưỡng cực - lưỡng cực giữa các nguyên tử hay phân tử
Câu 3 :
Chất nào sau đây có thể tạo liên kết hydrogen?
Đáp án : C Phương pháp giải :
- Điều kiện cần và đủ để tạo thành liên kết hydrogen: + Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,… + Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết Lời giải chi tiết :
- Nguyên tử H liên kết với các nguyên tử có độ âm điện lớn O - Nguyên tử O có 2 cặp electron chưa tham gia liên kết
Câu 4 :
Chất nào sau đây không thể tạo được liên kết hydrogen?
Đáp án : B Phương pháp giải :
- Điều kiện cần và đủ để tạo thành liên kết hydrogen: + Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,… + Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết Lời giải chi tiết :
H2O, CH3OH, NH3 đều có nguyên tử H liên kết với nguyên tử O, N có độ âm điện lớn và O, N đều có cặp electron tự do, chưa tham gia liên kết =>H2O, CH3OH, NH3 đều có liên kết hydrogen Chỉ có CH4 là không có liên kết hydrogen
Câu 5 :
Tương tác van der Waals tồn tại giữa những
Đáp án : D Phương pháp giải :
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực giữa các nguyên tử hay phân tử Lời giải chi tiết :
Tương tác van der Waals tồn tại giữa những nguyên tử hay phân tử
Câu 6 :
Cho các chất sau: . Chất có nhiệt độ sôi cao nhất là
Đáp án : D Phương pháp giải :
Trong dãy halogen, tương tác van der Waals tăng theo sự tăng của số electron (và proton) trong phân tử, làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của các chất Lời giải chi tiết :
Trong dãy halogen, tương tác van der Waals tăng theo sự tăng của số electron (và proton) trong phân tử, làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của các chất => I2 có nhiệt độ sôi cao nhất
Câu 7 :
Cho các chất sau: CH4, H2O, HF, BF3, C2H5OH, PCl5. Số chất tạo được liên kết hydrogen là
Đáp án : B Phương pháp giải :
- Điều kiện cần và đủ để tạo thành liên kết hydrogen: + Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,… + Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết Lời giải chi tiết :
- Các phân tử: H2O, HF, C2H5OH có + H liên kết với nguyên tử có độ âm điện lớn là O, F. + O, F còn các cặp electron tự do chưa tham gia liên kết => Có 3 chất tạo được liên kết hydrogen
Câu 8 :
Nhiệt độ sôi của từng chất methane, ethane, propane, và butane là 1 trong 4 nhiệt độ sau: 0oC, -164oC, -42oC và -88oC. Nhiệt độ sôi -164oC là của chất nào sau đây?
Đáp án : A Phương pháp giải :
Khi khối lượng phân tử tử tăng thì tương tác van der Waals tăng Lời giải chi tiết :
Methane có khối lượng phân tử nhỏ nhất => Tương tác van der Waals yếu nhất => Nhiệt độ sôi thấp nhất => Methane có nhiệt độ sôi là -164oC
Câu 9 :
Giữa H2O và C2H5OH có thể tạo ra bao nhiêu kiểu liên kết hydrogen?
Đáp án : D Phương pháp giải :
H2O và H2O H2O và C2H5OH C2H5OH và C2H5OH C2H5OH và H2O Lời giải chi tiết :
=> Có 4 kiểu liên kết hydrogen
Câu 10 :
Cho các khí hiếm sau: He, Ne, Ar, Kr, Xe. Khí hiếm có nhiệt độ nóng chảy thấp nhất và cao nhất lần lượt là
Đáp án : C Phương pháp giải :
Khối lượng phân tử tăng => Tương tác van der Waals tăng => Nhiệt độ sôi, nhiệt độ nóng chảy tăng Lời giải chi tiết :
He có khối lượng nhỏ nhất => Nhiệt độ nóng chảy thấp nhất Xe có khối lượng lớn nhất => Nhiệt độ nóng chảy cao nhất
Câu 11 :
Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử?
Đáp án : D Phương pháp giải :
Dựa vào - Định nghĩa liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết - Phân loại liên kết hydrogen: + Liên kết hydrogen nội phân tử: là liên kết hydrogen được tạo thành trong chính phân tử chất đó Điều kiện để có liên kết hydrogen nội phân tử:
+ Liên kết hydrogen liên phân tử: là liên kết hydrogen được tạo thành giữa phân tử này và phân tử khác Lời giải chi tiết :
- Đáp án: D - Giải thích: Trong 4 đáp án trên, chỉ có đáp án D thỏa mãn điều kiện để tạo liên kết hydrogen liên phân tử: Có nguyên tử H (đã liên kết với nguyên tố có độ âm điện cao là O) liên kết với một nguyên tử khác có độ âm điện lớn là O
Câu 12 :
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
Đáp án : D Phương pháp giải :
Dựa vào kích thước nguyên tử chlorine lớn hơn kích thước nguyên tử nitrogen => mật độ điện tích trên nguyên tử chlorine không đủ lớn Lời giải chi tiết :
- Đáp án: D
Câu 13 :
Sơ đồ nào sau đây thể hiện đúng liên kết hydrogen giữa 2 phân tử hydrogen fluoride (HF)?
Đáp án : A Phương pháp giải :
Dựa vào độ âm điện để xác định nguyên tử nào mang điện tích âm hay dương Lời giải chi tiết :
- Vì nguyên tử hydrogen có độ âm điện nhỏ hơn nguyên tử fluorine " nguyên tử hydrogen mang một phần điện tích dương và nguyên tử fluorine mang một phần điện tích âm => Đáp án: A
Câu 14 :
Điều nào sau đây đúng khi nói về liên kết hydrogen liên phân tử?
Đáp án : A Phương pháp giải :
- Định nghĩa liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết Lời giải chi tiết :
- Đáp án: A
Câu 15 :
Điều nào sau đây đúng khi nói về liên kết hydrogen nội phân tử?
Đáp án : B Phương pháp giải :
Dựa vào - Phân loại liên kết hydrogen: + Liên kết hydrogen nội phân tử: là liên kết hydrogen được tạo thành trong chính phân tử chất đó Điều kiện để có liên kết hydrogen nội phân tử:
+ Liên kết hydrogen liên phân tử: là liên kết hydrogen được tạo thành giữa phân tử này và phân tử khác Lời giải chi tiết :
- Đáp án: B
Câu 16 :
Phát biểu nào sau đây là đúng?
Đáp án : D Lời giải chi tiết :
- Đáp án: D - Giải thích: A, B, C đều sai vì liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết
Câu 17 :
H2O, NH3, HF, H2S, CO2, HCl. Số phân tử có thể tạo liên kết hydrogen với phân tử cùng loại là
Đáp án : A Phương pháp giải :
Dựa vào - Định nghĩa liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết Lời giải chi tiết :
Đáp án: A (H2O, NH3, HF)
Câu 18 :
Cho các chất sau: F2, Cl2, Br2, I2. Chất có nhiệt độ nóng chảy thấp nhất là
Đáp án : A Phương pháp giải :
Dựa vào - Đặc điểm của tương tác van der Waals: + Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất + Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng Lời giải chi tiết :
- Đáp án: A - Giải thích: Phân tử khối của F2 nhỏ nhất trong các chất trên
Câu 19 :
Cho các chất sau F2, Cl2, Br2, I2. Chất có nhiệt độ sôi cao nhất là
Đáp án : D Phương pháp giải :
Dựa vào - Đặc điểm của tương tác van der Waals: + Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất + Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng Lời giải chi tiết :
- Đáp án: D - Giải thích: Phân tử khối của I2 lớn nhất trong các chất trên
Câu 20 :
Dãy chất nào sau đây xếp theo thứ tự nhiệt độ sôi tăng dần?
Đáp án : D Phương pháp giải :
Dựa vào ảnh hưởng của liên kết hydrogen và tương tác van der Waals đến nhiệt độ sôi và nhiệt độ nóng chảy của các chất - Các chất có liên kết hydrogen đều có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn các chất không có liên kết hydrogen - Đặc điểm của tương tác van der Waals: + Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất + Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng Lời giải chi tiết :
- Phân tử H2O có liên kết hydrogen " nhiệt độ sôi cao nhất - Có " nhiệt độ sôi của H2S cao hơn nhiệt độ sôi của CH4 => Đáp án: D
|



















Danh sách bình luận