Trắc nghiệm Bài 1. Thành phần của nguyên tử - Hóa 10 Kết nối tri thứcĐề bài
Câu 1 :
Trong nguyên tử, hạt mang điện dương là
Câu 2 :
Aluminium là kim loại phổ biến nhất trên bỏ trái đất, được sử dụng trong các ngành xây dựng, ngành điện hoặc sản xuất đồ gia dụng. Hạt nhân của nguyên tử aluminium có điện tích bằng +13 và số khối là 27. Số proton, neutron và electron có trong nguyên tử aluminium lần lượt là
Câu 3 :
Tổng số hạt proton, neutron và electron trong nguyên tử X là 58. Trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 18. Xác định nguyên tử X
Câu 4 :
Phát biểu nào sau đây đúng?
Câu 5 :
Nguyên tử có đường kính lớn gấp khoảng 10 000 lần đường kính hạt nhân. Nếu ta phóng đại hạt nhân lên thành một quả bóng có đường kính 6 cm thì đường kính nguyên tử sẽ là
Câu 6 :
Beri và oxi lần lượt có khối lượng nguyên tử bằng: mBe = 9,012u; mO=15,999u. Khối lượng nguyên tử beri và oxi tính theo gam lần lượt là
Câu 7 :
Đặc điểm của electron là
Câu 8 :
Nhận định nào sau đây không đúng?
Câu 9 :
Số khối của nguyên tử bằng tổng
Câu 10 :
Phát biểu nào sau đây sai:
Câu 11 :
Cho nguyên tử X có tổng số hạt là 34, trong đó số hạt mang điện gấp 1,8333 lần số hạt không mang điện. Xác định số khối X
Câu 12 :
Nguyên tử Sodium có 12 neutron, 11 proton. Số hiệu nguyên tử của sodium là
Câu 13 :
Cho các phát biểu sau: (1). Tất cả các hạt nhân nguyên tử đều được cấu tạo từ các hạt proton và neutron. (2). Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ. (3). Trong nguyên tử số electron bằng số proton. (4). Trong hạt nhân nguyên tử hạt mang điện là proton và electron. (5). Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại. Số phát biểu đúng là
Câu 14 :
Nguyên tử của nguyên tố R được cấu tạo bởi 36 hạt, hạt mang điện gấp đôi hạt không mang điện. Số khối của nguyên tố đó là
Câu 15 :
Tổng số hạt trong ion X- là 53, số khối của X là
Câu 16 :
Mỗi nguyên tử nitrogen có 7 proton, 7 neutron, 7 electron và mp=1,6726.10-27kg; mn= 1,6748.10-27kg; me = 9,1094.10-31kg. Vậy khối lượng của phân tử N2 tính theo đơn vị gam (g) là
Câu 17 :
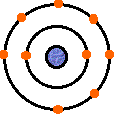
Có bao nhiêu proton trong nguyên tử trung hòa được biểu diễn ở hình bên dưới ?
Mô hình cấu tạo của nguyên tử.
Câu 18 :
Trong nguyên tử, hạt không mang điện có tên gọi là
Câu 19 :
Hạt mang điện trong hạt nhân nguyên tử là
Câu 20 :
Các hạt cấu tạo nên hạt nhân của hầu hết nguyên tử là
Lời giải và đáp án
Câu 1 :
Trong nguyên tử, hạt mang điện dương là
Đáp án : B Phương pháp giải :
- Trong nguyên tử: + Proton: +1 + Neutron: 0 + Electron: -1 Lời giải chi tiết :
Hạt mang điện tích dương trong nguyên tử là proton (+1)
Câu 2 :
Aluminium là kim loại phổ biến nhất trên bỏ trái đất, được sử dụng trong các ngành xây dựng, ngành điện hoặc sản xuất đồ gia dụng. Hạt nhân của nguyên tử aluminium có điện tích bằng +13 và số khối là 27. Số proton, neutron và electron có trong nguyên tử aluminium lần lượt là
Đáp án : C Phương pháp giải :
- Số đơn vị điện tích hạt nhân = số proton = số electron - Số khối = số proton + số neutron Lời giải chi tiết :
- Hạt nhân nguyên tử có điện tích là +13 => Số đơn vị điện tích hạt nhân = số proton = số electron = 13 - Số khối = số proton + số neutron => 27 = 13 + số neutron => Số neutron = 27 – 13 = 14 Số proton, neutron và electron có trong nguyên tử aluminium lần lượt là 13, 14, 13
Câu 3 :
Tổng số hạt proton, neutron và electron trong nguyên tử X là 58. Trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 18. Xác định nguyên tử X
Đáp án : A Phương pháp giải :
- Proton mang điện tích dương - Electron mang điện tích âm - Neutron không mang điện Lời giải chi tiết :
- Tổng số hạt proton, neutron và electron là 58 => p + n + e = 58 - Mà số p = số e => 2p + n = 58 (1) - Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 18 => (p + e) – n = 18 Hay: 2p – n = 18 (2) Từ (1) và (2) => p = e = 19 n = 20 - Ta có số proton = số đơn vị điện tích hạt nhân => Nguyên tử X có điện tích hạt nhân là +19 => X là Potassium: K
Câu 4 :
Phát biểu nào sau đây đúng?
Đáp án : B Phương pháp giải :
Nguyên tử H có 1 proton và 1 electron. Lời giải chi tiết :
Hạt nhân nguyên tử hydrogen chỉ có 1 proton, không có neutron
Câu 5 :
Nguyên tử có đường kính lớn gấp khoảng 10 000 lần đường kính hạt nhân. Nếu ta phóng đại hạt nhân lên thành một quả bóng có đường kính 6 cm thì đường kính nguyên tử sẽ là
Đáp án : C Phương pháp giải :
Đường kính nguyên tử = Đường kính hạt nhân x 10 000 Lời giải chi tiết :
Đường kính nguyên tử sau khi phóng đại là: 6.10 000 = 60 000 cm = 600 m
Câu 6 :
Beri và oxi lần lượt có khối lượng nguyên tử bằng: mBe = 9,012u; mO=15,999u. Khối lượng nguyên tử beri và oxi tính theo gam lần lượt là
Đáp án : A Phương pháp giải :
Ta có: 1u = 1,6605.10-24 gam Lời giải chi tiết :
Ta có: 1u = 1,6605.10-24 gam mBe = 9,012u = 9,012.1,6605.10-24 gam = 14,964.10-24 gam mO = 15,999u = 15,999.1,6605.10-24 gam = 26,566.10-24 gam
Câu 7 :
Đặc điểm của electron là
Đáp án : B Lời giải chi tiết :
Hạt electron mang điện tích âm và có khối lượng = 0,00055 amu
Câu 8 :
Nhận định nào sau đây không đúng?
Đáp án : A Lời giải chi tiết :
Hạt nhân của nguyên tử hydrogen không chứa neutron, chỉ chứa proton => A sai
Câu 9 :
Số khối của nguyên tử bằng tổng
Đáp án : A Phương pháp giải :
Số khối A = Z + N Lời giải chi tiết :
- Số khối A = Z + N - Mà Z = số p => Số khối nguyên tử bằng tổng số p và n
Câu 10 :
Phát biểu nào sau đây sai:
Đáp án : B Lời giải chi tiết :
- Trong nguyên tử: + Số hiệu nguyên tử = số proton = số electron + Số khối = số proton + số electron => Đáp án B sai
Câu 11 :
Cho nguyên tử X có tổng số hạt là 34, trong đó số hạt mang điện gấp 1,8333 lần số hạt không mang điện. Xác định số khối X
Đáp án : C Phương pháp giải :
- Số p = số e => 2p + n = 34 2p = 1,8333n
Lời giải chi tiết :
- Nguyên tử X có tổng số hạt là 34 => p + n + e = 34 - Mà số p = số e => 2p + n = 34 (1) - Số hạt mang điện gấp 1,8333 lần số hạt không mang điện => 2p = 1,8333n (2) - Từ (1) và (2) => p = 11, n = 12 => Số khối A = 11 + 12 = 23
Câu 12 :
Nguyên tử Sodium có 12 neutron, 11 proton. Số hiệu nguyên tử của sodium là
Đáp án : B Phương pháp giải :
Số hiệu nguyên tử = số proton
Lời giải chi tiết :
Ta có: số hiệu nguyên tử = số proton Mà số proton = 11 => Số hiệu nguyên tử của sodium là 11
Câu 13 :
Cho các phát biểu sau: (1). Tất cả các hạt nhân nguyên tử đều được cấu tạo từ các hạt proton và neutron. (2). Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ. (3). Trong nguyên tử số electron bằng số proton. (4). Trong hạt nhân nguyên tử hạt mang điện là proton và electron. (5). Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại. Số phát biểu đúng là
Đáp án : B Lời giải chi tiết :
(1) sai vì như hydrogen không có neutron. (2) sai vì khối lượng nguyên tử tập trung ở phần hạt nhân nguyên tử. (3) đúng. (4) sai vì hạt nhân không có electron. (5) đúng. => Có 2 phát biểu đúng.
Câu 14 :
Nguyên tử của nguyên tố R được cấu tạo bởi 36 hạt, hạt mang điện gấp đôi hạt không mang điện. Số khối của nguyên tố đó là
Đáp án : B Phương pháp giải :
Số khối = Z + N Lời giải chi tiết :
Ta có: 2Z + N = 36 2Z = 2N => 2N + N = 36 => N = 12 => Z = 12 A = Z + N = 12 + 12 = 24 Đáp án B
Câu 15 :
Tổng số hạt trong ion X- là 53, số khối của X là
Đáp án : B Phương pháp giải :
Số khối = Z + N Lời giải chi tiết :
Ta có: 2Z + N + 1 = 53 => 2Z + N = 52 \(\frac{{52}}{{3,5}} \le Z \le \frac{{52}}{3} \Rightarrow 14,9 \le Z \le 17,3\) Nếu Z = 15 (Là nguyên tố Phosphorus với A = 31) => N = 22 => A = 37 (loại) Nếu Z = 16 (Là nguyên tố sulfur với A = 32) => N = 20 => A = 36 (loại) Nếu Z = 17 => N = 18 => A = 35 => Nguyên tố Cl => Chọn B
Câu 16 :
Mỗi nguyên tử nitrogen có 7 proton, 7 neutron, 7 electron và mp=1,6726.10-27kg; mn= 1,6748.10-27kg; me = 9,1094.10-31kg. Vậy khối lượng của phân tử N2 tính theo đơn vị gam (g) là
Đáp án : C Lời giải chi tiết :
m N2 = 2.103.(7.1,6748.10-27 + 7.1,6726.10-27 + 7.9,1094.10-31) = 4,6876.10-23g
Câu 17 :
Có bao nhiêu proton trong nguyên tử trung hòa được biểu diễn ở hình bên dưới ?
Mô hình cấu tạo của nguyên tử.
Đáp án : B Phương pháp giải :
Số P = E Lời giải chi tiết :
Lớp 1 có 2 electron; lớp 2 có 7 electron => tổng số e = 2 + 7 = 9 electron Đáp án B
Câu 18 :
Trong nguyên tử, hạt không mang điện có tên gọi là
Đáp án : C Phương pháp giải :
Dựa vào cấu tạo nguyên tử Lời giải chi tiết :
Trong hạt nhân, hạt không mang điện là neutron Đáp án C
Câu 19 :
Hạt mang điện trong hạt nhân nguyên tử là
Đáp án : B Phương pháp giải :
Dựa vào cấu tạo nguyên tử Lời giải chi tiết :
Trong hạt nhân nguyên tử, hạt mang điện là proton Đáp án B
Câu 20 :
Các hạt cấu tạo nên hạt nhân của hầu hết nguyên tử là
Đáp án : C Phương pháp giải :
Dựa vào cấu tạo nguyên tử Lời giải chi tiết :
Hạt cấu tạo nên hạt nhân là proton và neutron Đáp án C
|



















Danh sách bình luận