Bài 2. Thành phần của nguyên tử trang 13, 14, 15, 16, 17, 18, 19 Hóa 10 Chân trời sáng tạoTải vềTừ rất lâu, các nhà khoa học đã nghiên cứu các mô hình nguyên tử Quan sát Hình 2.1, cho biết thành phần nguyên tử gồm những loại hạt nào? Cho biết vai trò của màn huỳnh quang trong thí nghiệm ở Hình 2.2 Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Tải về
CH tr 13 MĐ
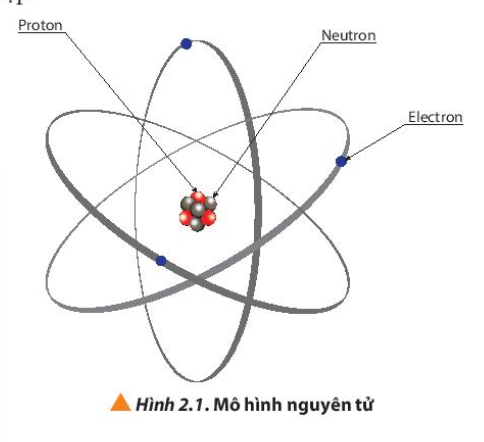
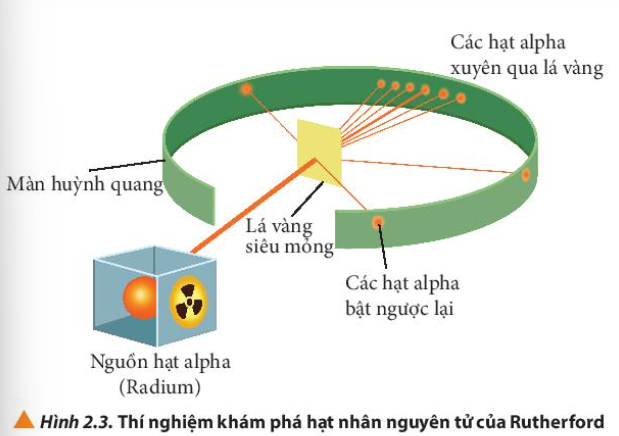
Lời giải chi tiết: - Nguyên tử gồm 3 hạt cơ bản: + Hạt electron: mang điện tích âm + Hạt proton: mang điện tích dương + Hạt neutron: không mang điện - Cơ sở tìm ra: + Electron: phóng điện trong ống thủy tinh chân không (ống tia âm cực) + Proton và neutron: tiến hành bắn phá 1 chùm hạt alpha lên 1 lá vàng siêu mỏng CH tr 13 CH
Phương pháp giải: Quan sát Hình 2.1, nêu các hạt cấu tạo nên nguyên tử Lời giải chi tiết: - Các hạt cấu tạo nên nguyên tử là: + Electron + Proton + Neutron CH tr 14 CH
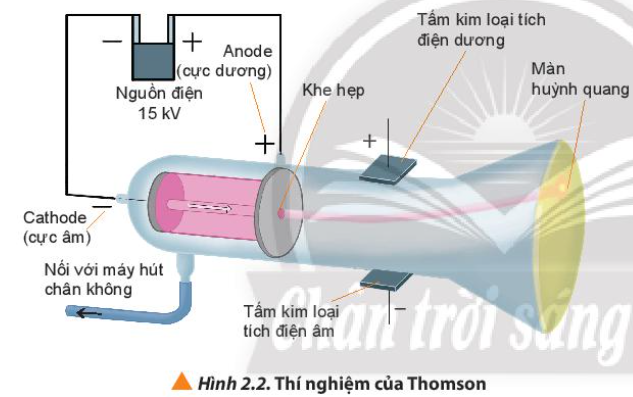
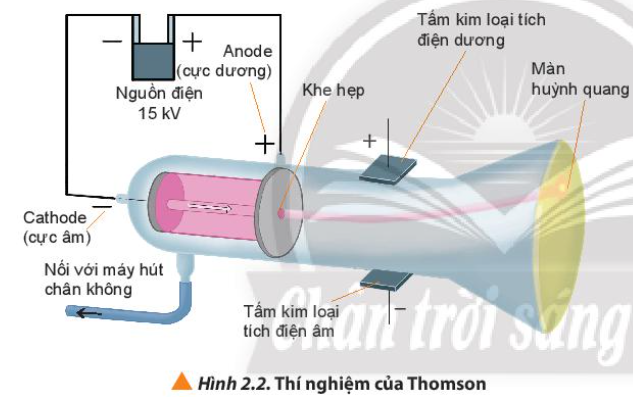
Phương pháp giải: Ông quan sát thấy màn huỳnh quang trong ống phát sáng Lời giải chi tiết: Ông quan sát thấy màn huỳnh quang trong ống phát sáng do những tia phát ra từ cực âm (tia âm cực) => Quan sát và phát hiện ra tia âm cực CH tr 14 CH
Phương pháp giải: Trái dấu thì hút nhau Lời giải chi tiết: Tia âm cực mang điện tích âm => Sẽ bị hút về cực dương của trường điện (trái dấu hút nhau, cùng dấu đẩy nhau) CH tr 14 CH
Phương pháp giải: - Các electron chuyển động hỗn loạn Lời giải chi tiết: Tia âm cực (các electron) chuyển động hỗn loạn, va đập vào chong chóng làm chong chóng quay CH tr 16 CH
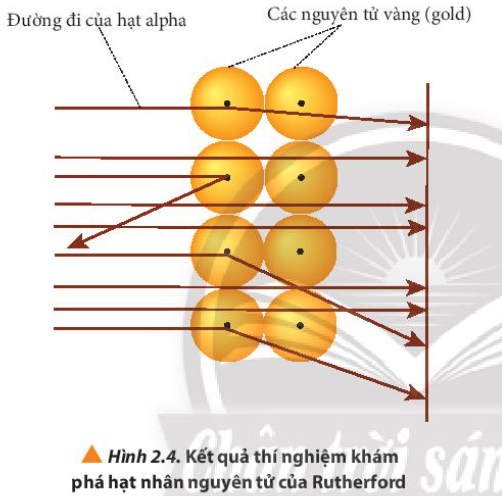
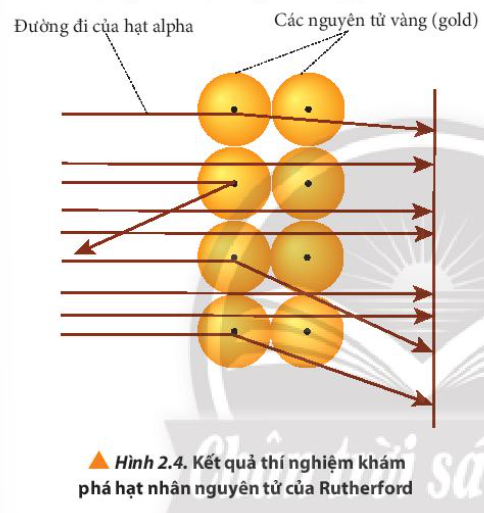
Phương pháp giải: - Quan sát Hình 2.3 để nhận xét đường đi - Quan sát Hình 2.4 để giải thích đường đi Lời giải chi tiết: - Quan sát Hình 2.3 thấy được: hầu hết các hạt α đi thẳng, có vài hạt bị bắn theo đường gấp khúc - Quan sát Hình 2.4 giải thích: các hạt α bị bắn theo đường gấp khúc là do va vào hạt nhân của nguyên tử vàng, các hạt không va vào hạt nhân thì đi thẳng CH tr 16 LT
Phương pháp giải: Nguyên tử trung hòa về điện: số đơn vị điện tích dương của hạt nhân = số đơn vị điện tích âm của các electron trong nguyên tử Lời giải chi tiết: - Nguyên tử oxygen có 8 electron => Số đơn vị điện tích âm của các electron trong nguyên tử oxygen là 8 - Mà số đơn vị điện tích dương hạt nhân = số đơn vị điện tích âm của các electron trong nguyên tử => Hạt nhân của nguyên tử oxygen có điện tích: +8 CH tr 16 CH
Phương pháp giải: - Hạt nhân gồm 2 hạt: + Proton mang điện tích dương: +1 + Neutron không mang điện Lời giải chi tiết: - Hạt nhân gồm 2 hạt: + Proton mang điện tích dương: +1 + Neutron không mang điện - Hạt nhân nguyên tử mang điện tích dương => Điện tích của hạt nhân nguyên tử do hạt proton quyết định => Số đơn vị điện tích hạt nhân = số proton trong hạt nhân CH tr 17 LT
Phương pháp giải: - Đơn vị điện tích hạt nhân = số proton - Số đơn vị điện tích dương của hạt nhân = số đơn vị điện tích âm của các electron trong nguyên tử => Số đơn vị điện tích hạt nhân = số proton = số electron trong nguyên tử Lời giải chi tiết: - Nguyên tử natri có điện tích hạt nhân là +11 => Số đơn vị điện tích hạt nhân = 11 - Mà số đơn vị điện tích hạt nhân = số proton = số electron trong nguyên tử => Nguyên tử natri có 11 proton và 11 electron CH tr 17 CH
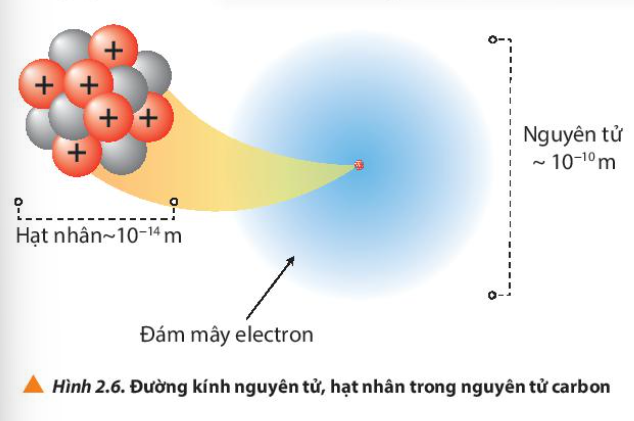
Phương pháp giải: - Đường kính nguyên tử = 10-10m - Đường kính hạt nhân = 10-14m Lời giải chi tiết: - Đường kính nguyên tử = 10-10m - Đường kính hạt nhân = 10-14m => Tỉ lệ đường kính nguyên tử và đường kính hạt nhân:
=> Đường kính nguyên tử lớn hơn rất nhiều so với đường kính hạt nhân CH tr 18 CH
Phương pháp giải: Tỉ lệ khối lượng 1 proton với 1 electron
Lời giải chi tiết: Tỉ lệ khối lượng 1 proton với 1 electron:
=> Khối lượng 1 electron nhỏ hơn rất nhiều so với khối lượng 1 proton => Có thể coi khối lượng nguyên tử = khối lượng hạt nhân do khối lượng của electron không đáng kể so với khối lượng của proton và neutron CH tr 18 LT
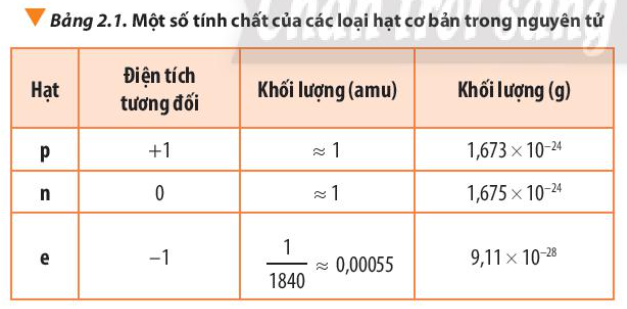
Phương pháp giải: Khối lượng nguyên tử = số p x khối lượng p + số n x khối lượng n + số e x khối lượng e Lời giải chi tiết: Khối lượng p = 1,673.10-24 gam = 1 amu Khối lượng n = 1,675.10-24 gam = 1 amu Khối lượng e = 9,11.10-28 gam = 0,00055 amu - Khối lượng nguyên tử oxygen theo đơn vị gam: 8 x 1,673.10-24 + 8 x 1,675.10-24 + 8 x 9,11.10-28 = 2,679.10-23 gam - Khối lượng nguyên tử oxygen theo đơn vị amu: 8 x 1 + 8 x 1 + 8 x 0,00055 = 16,0044 amu CH tr 19 VD
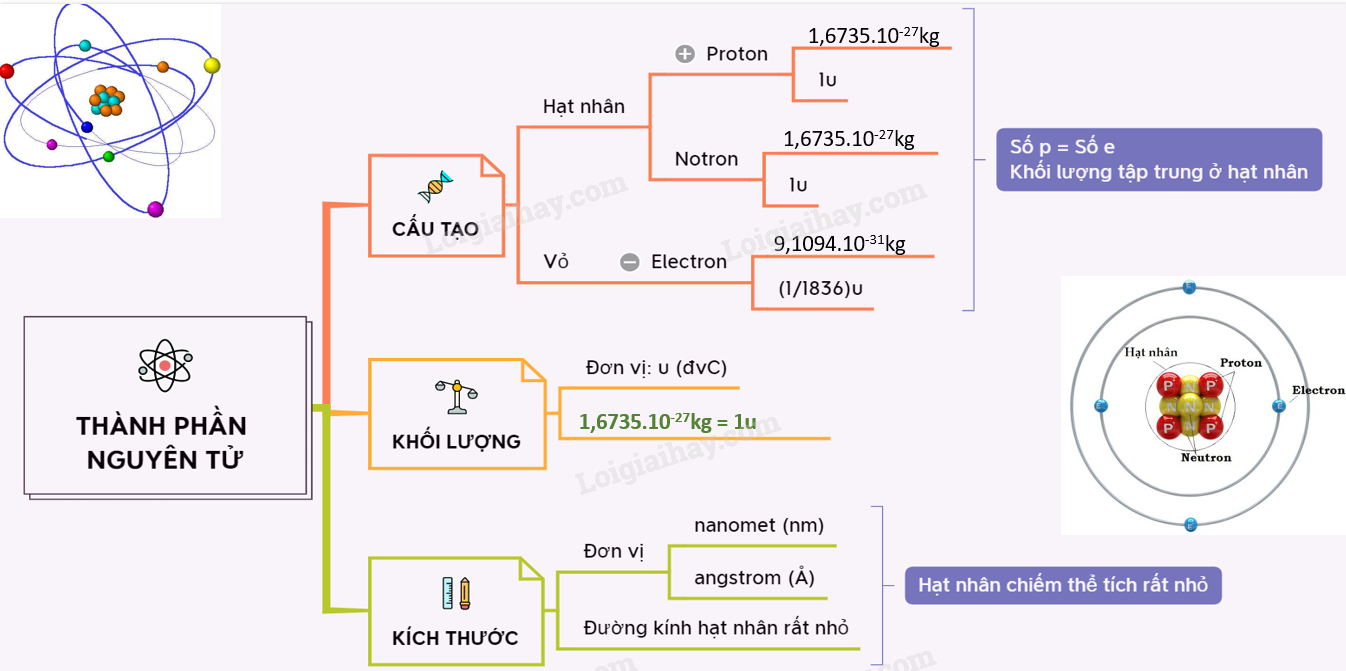
Phương pháp giải: - Nội dung chính bài học: + Cấu tạo nguyên tử + Kích thước nguyên tử, hạt nhân + Khối lượng của proton, electron, neutron => Khối lượng nguyên tử Lời giải chi tiết:
CH tr 19 BT1
Phương pháp giải: Quan sát Hình 2.4 Lời giải chi tiết: - Khi bắn các hạt α vào lá vàng, hầu hết các hạt α đi thẳng, không va vào hạt nào (trừ các hạt va vào hạt nhân) => Nguyên tử có cấu tạo rỗng CH tr 19 BT2
Phương pháp giải: - Thành phần cấu tạo của nguyên tử: + Hạt nhân: proton (mang điện dương) và neutron (không mang điện) có khối lượng gần bằng 1 amu + Vỏ nguyên tử: electron (mang điện âm) có khối lượng gần bằng 0 amu Lời giải chi tiết: Thông tin ở đáp án B không đúng vì electron nằm ở lớp vỏ, không nằm ở trong hạt nhân Đáp án B CH tr 19 BT3
Phương pháp giải: - Thành phần cấu tạo của nguyên tử: + Hạt nhân: proton (mang điện dương) và neutron (không mang điện) + Vỏ nguyên tử: electron (mang điện âm) Lời giải chi tiết: a) Hạt mang điện tích dương => Proton b) Hạt được tìm thấy trong hạt nhân và không mang điện => Neutron c) Hạt mang điện tích âm => Electron CH tr 19 BT4
Phương pháp giải: a) 1 electron có khối lượng = 9,11.10-28 gam b) 1 electron có khối lượng = 9,11.10-28 gam 1 mol electron có 6,022x1023 hạt electron Lời giải chi tiết: a) 1 electron có khối lượng = 9,11.10-28 gam \( = \frac{1}{{9,{{11.10}^{ - 28}}}} = 1,098{\rm{ }} \times {\rm{ }}{10^{27}}\;\) (hạt) b) 1 electron có khối lượng = 9,11.10-28 gam 1 mol electron có 6,022x1023 hạt electron => Khối lượng 1 mol electron = 9,11.10-28 x 6,022x1023 = 5,49.10-4 gam
|














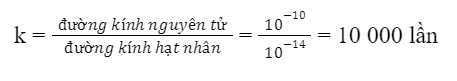
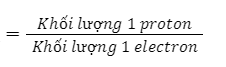
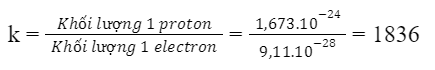
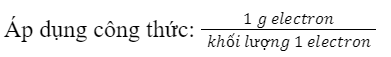
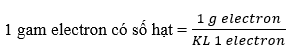






Danh sách bình luận