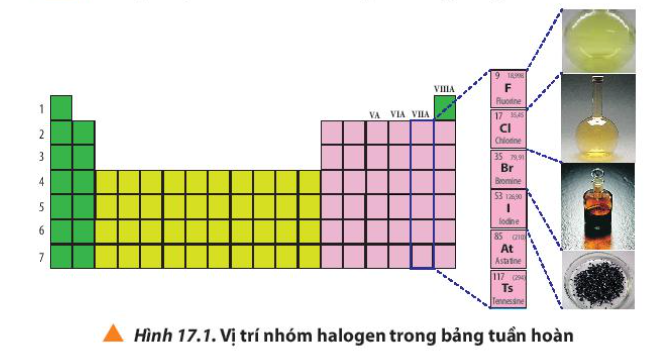
Bài 17. Tính chất vật lí và hóa học các đơn chất nhóm VIIA trang 105, 106, 107, 108, 109, 110, 111, 112, 113 Hóa 10 Chân trời sáng tạoTrong đèn halogen, bao quanh dây tóc làm bằng wolfram là các khí hiếm như krypton, xenon và một lượng nhỏ halogen như bromine hoặc iodine 1. Quan sát Hình 17.1, cho biết vị trí nhóm halogen trong bảng tuần hoàn Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
CH tr 105 MĐ
Phương pháp giải:
Lời giải chi tiết: - Nhóm halogen gồm những nguyên tố nhóm VIIA: fluorine (F), chlorine (Cl), bromine (Br), iodine (I), astatine (At), tennessine (Ts) - Tính chất: tác dụng với kim loại, hydrogen, dung dịch kiềm, muối halide - Ứng dụng: + Fluorine: chảo chống dính, kem đánh răng + Chlorine: sát khuẩn, khử trùng + Bromine: thuốc an thần, tráng phim ảnh + Iodine: chống bướu cổ, chất xúc tác, dược phẩm, thuốc nhuộm CH tr 106 CH
Phương pháp giải: Quan sát Hình 17.1 và nhận xét Lời giải chi tiết: Halogen nằm ở nhóm VIIA trong bảng tuần hoàn CH tr 106 CH
Phương pháp giải: CaF2, Ca5(PO4)3F, Na3AlF6, NaCl, KCl Lời giải chi tiết: Một số chất chứa nguyên tố halogen + Fluorite: CaF2 + Fluorapatite: Ca5(PO4)3F + Cryolite: Na3AlF6 + Muối ăn: NaCl, KCl + Brommargyrite: AgBr + Iodargyrite: AgI CH tr 106 CH
Phương pháp giải: Tồn tại dưới dạng hợp chất Lời giải chi tiết: Trong tự nhiên, các halogen không tồn tại dưới dạng đơn chất, chủ yếu tồn tại dưới dạng muối của các ion halide CH tr 107 LT
Phương pháp giải: Thành phần của biển và đại dương là muối NaCl, KCl Lời giải chi tiết: Trên Trái Đất, 71% là biển và đại dương mà thành phần chủ yếu của nước biển là muối chloride => Hàm lượng nguyên tố chloride là nhiều nhất trong tự nhiên CH tr 107 CH
Phương pháp giải: Các nguyên tố nhóm halogen đều có 7 electron ở lớp ngoài cùng Lời giải chi tiết: - F: (He)2s22p5 - Cl: (Ne)3s23p5 - Br: (Ar)4s24p5 - I: (Kr)5s25p5 CH tr 107 CH
Phương pháp giải: - Các nguyên tố nhóm halogen có 7 electron ở lớp ngoài cùng Lời giải chi tiết: - Các nguyên tố nhóm halogen có 7 electron ở lớp ngoài cùng => Có xu hướng nhận 1 electron (liên kết ion) hoặc bỏ ra 1 electron để góp chung (liên kết cộng hóa trị) để có cấu hình electron bền vững của khí hiếm CH tr 108 CH
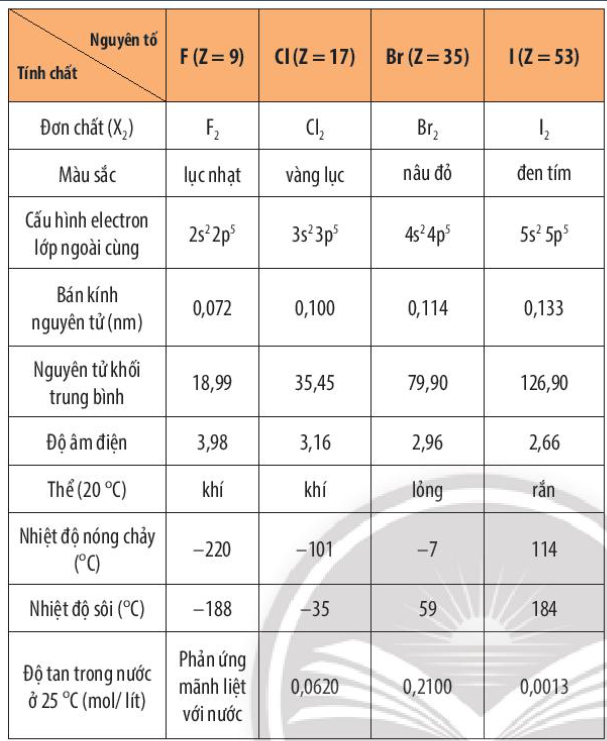
Phương pháp giải: Quan sát Bảng 17.1 và nhận xét Lời giải chi tiết: - Trong nhóm halogen, đi từ F đến I + Màu sắc: đậm dần: lục nhạt – vàng lục – nâu đỏ - đen tím + Thể ở điều kiện thường: khí – khí – lỏng – rắn + Nhiệt độ nóng chảy, nhiệt độ sôi: tăng dần CH tr 108 CH
Phương pháp giải: Phụ thuộc vào tương tác van der Waals Lời giải chi tiết: Nhiệt độ nóng chảy và nhiệt độ sôi của đơn chất halogen bị ảnh hưởng với tương tác van der Waals giữa các phân tử. Từ fluorine đến iodine, khối lượng phân tử và bán kính nguyên tử tăng, làm tăng tương tác van der Waals, dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi tăng CH tr 108 LT
Phương pháp giải: Trong nhóm halogen đi từ trên xuống dưới, khối lượng phân tử và bán kính nguyên tử tăng => Lực tăng tác van der Waals tăng Lời giải chi tiết: Trong nhóm halogen đi từ trên xuống dưới, khối lượng phân tử và bán kính nguyên tử tăng => Lực tăng tác van der Waals tăng => Nhiệt độ sôi tăng => Astatine trong điều kiện thường tồn tại ở thể rắn CH tr 109 CH
Phương pháp giải: Các nguyên tử halogen có 7 electron ở lớp ngoài cùng Lời giải chi tiết: - Halogen có cấu hình electron lớp ngoài cùng là ns2np5, nên nguyên tử có xu hướng nhận thêm 1 electron hoặc dùng chung electron với nguyên tử khác để đạt cấu hình electron bền vững của khí hiếm Sơ đồ: X + 1e → X- CH tr 109 CH
Phương pháp giải: Trong phản ứng với kim loại, halogen sẽ nhận 1 electron của kim loại tạo thành ion halide X- Lời giải chi tiết: - Trong phản ứng với kim loại, các halogen từ số oxi hóa 0 sẽ nhận thêm 1 electron thành số oxi hóa -1 - Sơ đồ: F + 1e → F- Cl + 1e → Cl- Br + 1e → Br- I + 1e → I- CH tr 110 CH
Phương pháp giải:
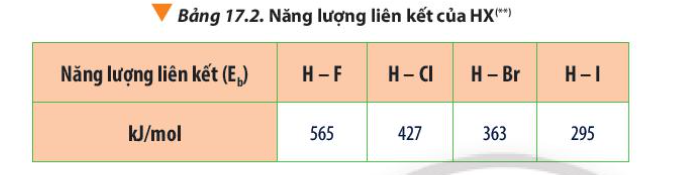
Lời giải chi tiết: - Đi từ F đến I + Điều kiện phản ứng với hydrogen khó dần + Năng lượng liên kết H-X giảm dần => Độ bền H-X giảm dần => Khả năng phản ứng của các halogen với hydrogen giảm dần CH tr 110 CH
Phương pháp giải: - Xác định số oxi hóa của Cl trong 2 phản ứng: Lời giải chi tiết: - Phản ứng thứ nhất: \(\mathop {C{l_2}}\limits^0 + 2NaOH \to Na\mathop {Cl}\limits^{ - 1} + Na\mathop {Cl}\limits^{ + 1} O + {H_2}O\) => Số oxi hóa của Cl từ 0 thành -1 và +1 => Phản ứng oxi hóa khử trong đó, Cl2 vừa là chất oxi hóa vừa là chất khử - Phản ứng thứ 2: \(\mathop {3C{l_2}}\limits^0 + 6NaOH\xrightarrow{{ > {{70}^o}C}}5Na\mathop {Cl}\limits^{ - 1} + Na\mathop {Cl}\limits^{ + 5} {O_3} + 3{H_2}O\) => Số oxi hóa của Cl từ 0 thành -1 và +5 => Phản ứng oxi hóa khử trong đó, Cl2 vừa là chất oxi hóa vừa là chất khử CH tr 111 CH
Phương pháp giải: Tiến hành thí nghiệm và quan sát Lời giải chi tiết: - Ống nghiệm 1: dung dịch không màu chuyển thành màu vàng nhạt - Ống nghiệm 2: dung dịch không màu chuyển thành vàng, khi cho hồ tinh bột (không màu) thì dung dịch chuyển màu xanh tím CH tr 111 CH
Phương pháp giải: - Ống 1: Cl2 + 2NaBr → 2NaCl + Br2 - Ống 2: Br2 + 2NaI → 2NaBr + I2 Lời giải chi tiết: - Giải thích kết quả: + Ống nghiệm 1: dung dịch không màu chuyển thành màu vàng nhạt của Br2 Cl2 + 2NaBr → 2NaCl + Br2 + Ống nghiệm 2: dung dịch không màu chuyển thành vàng của I2, khi cho hồ tinh bột (không màu) thì dung dịch chuyển màu xanh tím do I2 làm đổi màu hồ tinh bột Br2 + 2NaI → 2NaBr + I2 CH tr 111 CH
Phương pháp giải: Tiến hành thí nghiệm và quan sát hiện tượng Lời giải chi tiết: Hiện tượng: Giấy màu ẩm bị nhạt màu dần sau đó mất màu CH tr 112 CH
Phương pháp giải: 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O Lời giải chi tiết: Sản phẩm tạo thành có khí Cl2, khí Cl2 bay lên tác dụng với H2O (giấy màu ẩm) tạo thành hỗn hợp có tính tẩy màu Cl2 + H2O → HCl + HClO => Giấy màu ẩm bị nhạt màu dần sau đó mất màu CH tr 112 LT
Phương pháp giải:
Lời giải chi tiết: Cu + Cl2 → CuCl2 (1) 2Al + 3Br2 → 2AlBr3 (2) 2Ca(OH)2 + 2Cl2 → CaCl2 + Ca(ClO)2 + 2H2O (3) 6KOH + 3Br2 \(\xrightarrow{{ > {{70}^o}C}}\) 5KBr + KBrO3 + 3H2O (4) Cl2 + 2KBr → 2KCl + Br2 (5) Br2 + 2NaI → 2KBr + I2 (6) CH tr 112 VD
Phương pháp giải: Tính tẩy màu: sát trùng, sát khuẩn Lời giải chi tiết: - Tính tẩy màu của khí chlorine ẩm được ứng dụng trong lĩnh vực + Diệt trùng nước sinh hoạt, diệt các loại vi khuẩn gây bệnh + Tẩy trắng sợi, vải, giấy CH tr 113 CH
Phương pháp giải: - Fluorine, chlorine, bromine, iodine Lời giải chi tiết: - Fluorine: dùng làm chảo chống dính, thuốc trừ sâu, chống gián và được cho vào thuốc đánh răng, tạo men răng - Chlorine: chất tẩy trắng, khử trùng nước, sản xuất 1 số chất hữu cơ - Bromine: thuốc an thần, thuốc trừ sâu, thuốc nhuộm, mực in, tráng phim ảnh - Iodine: phòng bướu cổ, thiểu năng trí tuệ; ngoài ra còn dùng để sát trùng và dùng trong dược phẩm, thuốc nhuộm => Halogen có vai trò rất quan trọng trong đời sống, sản xuất và y tế CH tr 113 CH
Phương pháp giải:
Lời giải chi tiết: - Fluorine được dùng làm chất sinh hàn trong tủ lạnh. Ngoài ra còn dùng trong công nghiệp hạt nhân để làm giàu 235U - Hợp chất của bromine được dùng nhiều trong công nghiệp dầu mỏ, hóa chất cho nông nghiệp CH tr 113 VD
Phương pháp giải: Nước Javel có tính tẩy màu Lời giải chi tiết: Nước Javel có tính oxi hóa mạnh, có tính tẩy màu nên có thể tẩy được vết mực trên áo trắng nhưng không nên sử dụng trên vải quần, áo màu vì nước Javel sẽ làm mất màu của quần áo đó CH tr 113 BT1
Phương pháp giải:
Lời giải chi tiết: a) Cl2 + H2 → 2HCl b) F2 + Cu → CuF2 c) I2 + 2Na → 2NaI d) Cl2 + Fe → FeCl3 e) Br2 + Ca(OH)2 → CaBr2 + Ca(BrO)2 + 2H2O f) 3Cl2 + 6KOH \(\xrightarrow{{{{100}^o}C}}\) 5KCl + KClO3 + 3H2O g) Br2 + 2KI → 2KBr + I2 CH tr 113 BT2
Phương pháp giải: Các nguyên tố halogen có độ âm điện lớn Lời giải chi tiết: Các nguyên tố halogen có độ âm điện lớn, dễ nhận 1 electron => Có tính oxi hóa mạnh => Dễ tham gia các phản ứng tạo thành hợp chất => Trong tự nhiên, halogen không tồn tại dạng đơn chất CH tr 113 BT3
Phương pháp giải: Dựa vào công thức tính nồng độ phần trăm Lời giải chi tiết:
a) 200 lít nước => 200 000g nước 250 mg = 0,25g Đặt x là số viên nén chloramine B 25% (loại viên 1 gam) => m chất tan = 0,25x (gam) Áp dụng công thức tính nồng độ phần trăm ta có: 0,001% = \(\frac{{0,25{\rm{x}}}}{{200000 + 0,25{\rm{x}}}}.100\% \) => x = 8 Vậy cần dùng 8 viên nén để xử lí bình chứa 200 lít nước b) 1 lít nước => 1 kg nước = 1000g nước đặt y là khối lượng chloramine B 25% dạng bột cần dùng => m chất tan = 0,25y (gam) Áp dụng công thức tính nồng độ phần trắm ta có: \(2\% = \frac{{0,25y}}{{1000 + 0,25y}}.100\% \) => y = 81,6g Vậy cần sử dụng 81,6g để pha với 1 lít nước
|
















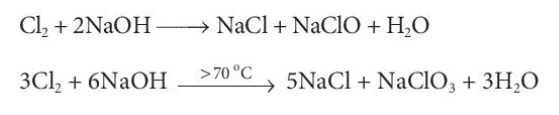







Danh sách bình luận