Bài 16. Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học trang 98, 99, 100, 101, 102, 103, 104 Hóa 10 Chân trời sáng tạoThực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn (a), 1. Tiến hành thí nghiệm 1 và quan sát hiện tượng của thí nghiệm. Nhận xét mối liên hệ giữa thể tích dung dịch Na2S2O3 với thời gian xuất hiện kết tủa Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
CH tr 98 MĐ
Lời giải chi tiết: (a) Ảnh hưởng của nhiệt độ (b) Ảnh hưởng của áp suất (c) Ảnh hưởng của nồng độ CH tr 98 CH
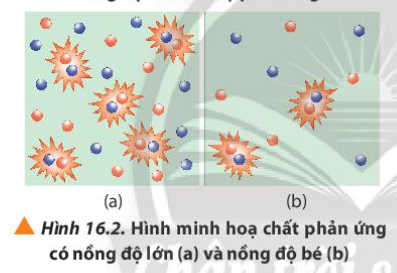
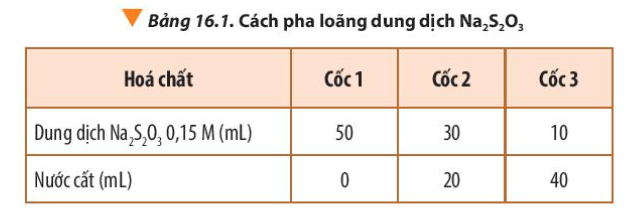
Phương pháp giải: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng Lời giải chi tiết: Thể tích dung dịch Na2S2O3 càng nhiều => Nồng độ Na2S2O3 càng cao => Thời gian xuất hiện kết tủa càng nhanh CH tr 99 CH
Phương pháp giải: Nồng độ cao => Mật độ các hạt chất tham gia cao => Tăng độ va chạm giữa các hạt chất tham gia Lời giải chi tiết: Khi nồng độ Na2S2O3 cao => Các hạt phân tử Na2S2O3 nhiều => Tăng sự va chạm giữa Na2S2O3 và phân tử H2SO4 => Tăng khả năng tạo thành kết tủa CH tr 99 LT
Phương pháp giải: Nồng độ H2SO4 giảm => Tốc độ phản ứng giảm Lời giải chi tiết: Khi pha loãng dung dịch H2SO4 => Nồng độ H2SO4 giảm => Tốc độ phản ứng giảm CH tr 99 CH
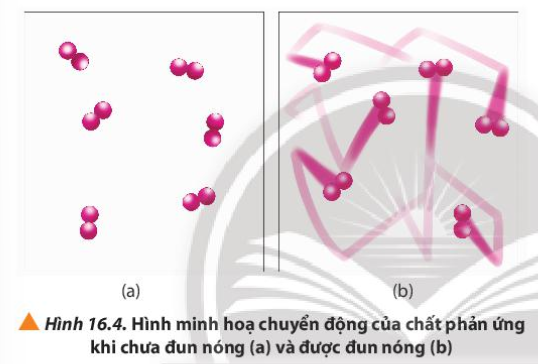
Lời giải chi tiết: Khi tăng nhiệt độ, tốc độ phản ứng tăng CH tr 100 CH
Phương pháp giải: Khi tăng nhiệt độ, các chất chuyển động với tốc độ lớn Lời giải chi tiết: - Cốc (2) ở nhiệt độ thường, các hạt KMnO4, H2C2O4 và H2SO4 chuyển động với tốc độ nhỏ, khả năng va chạm ít => Phản ứng diễn ra chậm => Lâu mất màu - Cốc (1) ở nhiệt độ cao, các hạt KMnO4, H2C2O4 và H2SO4 chuyển động với tốc độ lớn, khả năng va chạm cao => Phản ứng diễn ra nhanh => Nhanh mất màu CH tr 100 LT
Phương pháp giải:
Lời giải chi tiết:
CH tr 101 CH
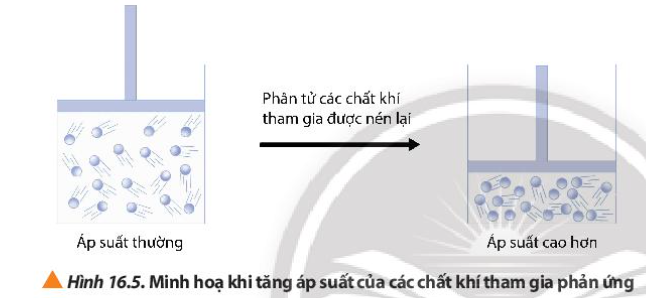
Phương pháp giải: Quan sát Hình 16.5 và rút ra nhận xét Lời giải chi tiết: Khi tăng áp suất của bình, mật độ phân bố của các phân tử chất khí trong bình kín tăng CH tr 101 LT
Lời giải chi tiết: - Trong phản ứng hóa học có sự tham gia của chất khí, áp xuất sẽ ảnh hưởng đến tốc độ phản ứng => Yếu tố áp suất ảnh hưởng đến tốc độ phản ứng (1) - Khi tăng áp suất, tốc độ phản ứng tăng CH tr 101 CH
Phương pháp giải: Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng Lời giải chi tiết: Tốc độ khí thoát ra ở bình 2 nhanh hơn bình 1 CH tr 101 CH
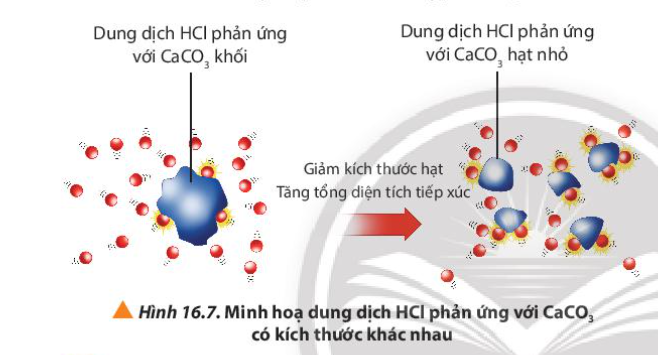
Lời giải chi tiết: Kích thước các hạt CaCO3 càng nhỏ thì tốc độ phản ứng càng nhanh CH tr 102 CH
Phương pháp giải: Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng Lời giải chi tiết: - Ở bình 2, CaCO3 ở dạng hạt nhỏ => Tổng diện tích tiếp xúc giữa CaCO3 với HCl tăng => Tốc độ phản ứng bình 2 tăng => Tốc độ khí thoát ra ở bình 2 nhanh hơn CH tr 102 LT
Phương pháp giải: Khi củi được chẻ nhỏ, tổng diện tích tiếp xúc của củi với oxygen tăng Lời giải chi tiết: - Khi củi được chẻ nhỏ => Tổng diện tích tiếp xúc của củi với oxygen tăng - Mà oxygen duy trì sự cháy => Tăng tốc độ cháy của củi => Củi sẽ cháy nhanh hơn và mạnh hơn CH tr 102 CH
Lời giải chi tiết: - Hiện tượng: Tàn đóm ở ống nghiệm (1) cháy le lói, tàn đóm ở ống nghiệm (2) bùng cháy => Tàn đóm ở ống nghiệm (2) cháy mạnh hơn CH tr 103 LT
Phương pháp giải: Chất xúc tác làm tăng tốc độ của phản ứng hóa học Lời giải chi tiết: Khi ta nhai cơm lâu trong miệng thấy có cảm giác ngọt vì tinh bột trong cơm đã chịu tác dụng của enzim amilaza trong nước bọt và biến đổi một thành phần thành đường mantôzơ, đường này đã tác động vào các gai vị giác trên lưỡi cho ta cảm giác ngọt. CH tr 103 CH
Phương pháp giải: a) Ảnh hưởng của nồng độ b) Ảnh hưởng của áp suất c) Ảnh hưởng của diện tích tiếp xúc d) Ảnh hưởng của nhiệt độ Lời giải chi tiết: a) Ảnh hưởng của nồng độ: Dùng bình chứa oxygen có nồng độ oxygen cao hơn không khí => Phản ứng cháy dễ dàng xảy ra b) Ảnh hưởng của áp suất: Dùng nồi áp suất làm tăng áp suất trong nồi => Thực phẩm trong nồi áp suất sẽ nhanh chín hơn c) Ảnh hưởng của diện tích tiếp xúc: Đậy nắp lò làm hạn chế diện tích tiếp xúc của than với oxygen trong không khí => Phản ứng cháy diễn ra chậm => Giữ than cháy được lâu hơn d) Ảnh hưởng của nhiệt độ: Khi để thức ăn trong tủ lạnh => Nhiệt độ bị giảm => Kìm hãm phản ứng oxi hóa thức ăn => Thức ăn sẽ lâu bị ôi thiu CH tr 104 VD
Lời giải chi tiết: Trong quá trình lên men giấm, người ta thường cho chuối hay nước dừa vào giúp tăng mùi thơm của giấm và kích thích con giấm lên men nhanh hơn vì con giấm sử dụng đường làm thức ăn. CH tr 104 BT1
Phương pháp giải: Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng Lời giải chi tiết: Khi chia con gà thành các phần nhỏ thì món ăn sẽ nhanh chín hơn. Vì khi chia nhỏ, tổng diện tích tiếp xúc của con gà với chảo nóng nhiều hơn => Tốc độ chín thức ăn nhanh hơn CH tr 104 BT2
Lời giải chi tiết: - Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng - Khi tăng nhiệt độ, tốc độ phản ứng tăng - Đối với phản ứng có chất khí tham gia, tốc độ phản ứng tăng khi tăng áp suất - Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng - Chất xúc tác làm tăng tốc độ của phản ứng hóa học, nhưng vẫn được bảo toàn về chất lượng khi kết thúc phản ứng CH tr 104 BT3
Phương pháp giải: a) Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng b) Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng c) Khi tăng nhiệt độ, tốc độ phản ứng tăng Lời giải chi tiết: a) Khi thay a g hạt Zn = a g bột Zn => Chất tham gia được nghiền nhỏ => Diện tích bề mặt tiếp xúc của Zn với HCl tăng => Tốc độ phản ứng tăng => Khí thoát ra nhanh hơn b) Khi thay dung dịch HCl 2 M = dung dịch HCl 1 M => Nồng độ chất tham gia giảm => Tốc độ phản ứng giảm => Khí thoát ra chậm hơn c) Khi đun nóng nhẹ dung dịch HCl => Nhiệt độ của phản ứng tăng => Tốc độ phản ứng tăng => Khí thoát ra nhanh hơn CH tr 104 BT4
Phương pháp giải:
Lời giải chi tiết:
|
















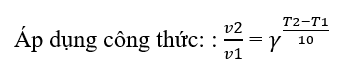











Danh sách bình luận