Đề thi giữa kì 2 Hóa 10 - Kết nối tri thức - Đề số 5Phát biểu nào sau đây là đúng?Đề bài
Câu 1 :
Phát biểu nào sau đây là đúng?
Câu 2 :
Phát biểu nào sau đây không đúng?
Câu 3 :
Số oxi hóa của chromium (Cr) trong Na2CrO4 là
Câu 4 :
Số oxi hóa của carbon và oxygen trong C2O42- lần lượt là:
Câu 5 :
Số oxi hóa của Cl trong các chất NaClO, NaClO2, NaClO3, NaClO4 lần lượt là:
Câu 6 :
Cho các phát biểu sau: (a) Sự oxi hóa là sự nhường electron hay sự làm tăng số oxi hóa. (b) Trong quá trình oxi hóa, chất khử nhận electron. (c) Sự khử là sự nhận electron hay là sự làm giảm số oxi hóa. (d) Trong quá trình khử, chất oxi hóa nhường electron. (e) Trong quá trình khử, chất oxi hóa nhận electron và bị khử xuống số oxi hóa thấp hơn. (f) Trong quá trình oxi hóa, chất khử nhường electron và bị oxi hóa lên số oxi hóa cao hơn. Số phát biểu đúng là
Câu 8 :
Cho 4,8 gam Mg tác dụng với lượng dư dung dịch HNO3 đặc, nóng thu được V lít khí NO2 (ở đkc, là sản phẩm khử duy nhất). Giá trị của V là
Câu 9 :
Chlorine vừa đóng vai trò chất oxi hóa, vừa đóng vai trò chất khử trong các phản ứng nào sau đây?
Câu 10 :
Phát biểu nào sau đây đúng?
Câu 11 :
Nung nóng hai ống nghiệm chứa NaHCO3 và P, xảy ra các phản ứng sau: 2 NaHCO3 (s) \( \to \)Na2CO3(s) + CO2(g) + H2O(g) (1) 4P(s) + 5O2(g) \( \to \)2P2O5(s) (2) Khi ngừng đun nóng, phản ứng (1) dừng lại còn phản ứng (2) tiếp tục xảy ra, chứng tỏ
Câu 12 :
Cho phản ứng hóa học xảy ra ở điều kiện chuẩn sau: 2NO2 (đỏ nâu) \( \to \)N2O4 (không màu) Biết NO2 và N2O4 có \({\Delta _f}H_{298}^0\)tương ứng là 33,18 KJ/mol và 9,16 KJ/mol. Điều này chứng tỏ phản ứng
Câu 13 :
Cho các phản ứng sau: (1) C (s) + CO2(g) \( \to \) 2CO (g) \({\Delta _r}H_{298}^0 = 173,6kJ\) (2) C (s) + H2O (g) \( \to \)CO (g) + H2 (g) \({\Delta _r}H_{298}^0 = 133,8kJ\) (3) CO (g) + H2O (g) \( \to \)CO2 (g) + H2 (g) Ở 500K, 1 atm, biến thiên enthalpy của phản ứng (3) có giá trị là
Câu 14 :
Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn: (1) \({N_2}(g) + {O_2}(g) \to 2NO(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0(1)\) (2) \(NO(g) + \frac{1}{2}{O_2}(g) \to N{O_2}(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0(2)\) Cho các phát biểu sau:
Số phát biểu không đúng là
Câu 15 :
Cho enthalpy tạo thành chuẩn của một số chất sau:
Biến thiên enthalpy chuẩn của phản ứng: CaCO3(s) \( \to \)CaO(s) + CO2(g)
Câu 16 :
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
Biến thiên enthalpy của phản ứng C3H8(g) → CH4(g) + C2H4(g) có giá trị là
Câu 17 :
Cho phản ứng sau: 2SO2 (g) + O2 (g) → 2SO3 (g) Biết (kJ.mol-1 ) của SO2 và SO3 lần lượt là –296,83 và –395,72. Biến thiên enthalpy của phản ứng trên ở điều kiện chuẩn có giá trị là
Câu 18 :
Nhiệt tạo thành chuẩn của một chất là nhiệt lượng tạo thành 1 mol chất đó từ chất nào ở điều kiện chuẩn?
Câu 19 :
Phản ứng nào sau đây là phản ứng toả nhiệt?
Câu 20 :
Cho các phát biểu: (a) Biến thiên enthalpy chuẩn của một phản ứng hóa học là lượng nhiệt kèm theo phản ứng đó ở áp suất 1 atm và 25o C. (b) Nhiệt (tỏa ra hay thu vào) kèm theo một phản ứng được thực hiện ở 1 bar và 298 K là biến thiên enthalpy chuẩn của phản ứng đó. (c) Một số phản ứng khi xảy ra làm môi trường xung quanh nóng lên là phản ứng thu nhiệt. (d) Một số phản ứng khi xảy ra làm môi trường xung quanh lạnh đi là do các phản ứng này thu nhiệt và lấy nhiệt từ môi trường. Số phát biểu đúng là
Lời giải và đáp án
Câu 1 :
Phát biểu nào sau đây là đúng?
Đáp án : A Phương pháp giải :
Dựa vào kiến thức về phản ứng oxi hóa khử Lời giải chi tiết :
A đúng vì các nguyên tử trong đơn chất đều bằng 0 B sai vì tổng số oxi hóa trong một ion đa nguyên tử bằng điện tích của ion C sai vì hầu hết hợp chất hydrogen có số oxi hóa +1 D sai vì hầu hết hợp chất oxygen có số oxi hóa – 2 Đáp án A
Câu 2 :
Phát biểu nào sau đây không đúng?
Đáp án : A Phương pháp giải :
Dựa vào kiến thức về phản ứng oxi hóa khử Lời giải chi tiết :
A sai vì số oxi hóa của một nguyên tử một nguyên tố trong hợp chất được xác định theo quy tắc xác định số oxi hóa với tổng điện tích = điện tích của hợp chất Đáp án A
Câu 3 :
Số oxi hóa của chromium (Cr) trong Na2CrO4 là
Đáp án : C Phương pháp giải :
Dựa vào quy tắc xác định số oxi hóa Lời giải chi tiết :
Gọi số oxi hóa của Cr trong hợp chất là x => 2.+1 + x + -2.4 = 0 => x =+6 Đáp án C
Câu 4 :
Số oxi hóa của carbon và oxygen trong C2O42- lần lượt là:
Đáp án : A Phương pháp giải :
Dựa vào quy tắc xác định số oxi hóa Lời giải chi tiết :
Số oxi hóa của oxygen là –2 => số oxi hóa của C là: 2.x + -2. 4 = -2 => x = +3 Đáp án A
Câu 5 :
Số oxi hóa của Cl trong các chất NaClO, NaClO2, NaClO3, NaClO4 lần lượt là:
Đáp án : C Phương pháp giải :
Dựa vào quy tắc xác định số oxi hóa của nguyên tử Lời giải chi tiết :
\(Na\mathop {Cl}\limits^{ + 1} O,Na\mathop {Cl}\limits^{ + 3} {O_2},Na\mathop {Cl}\limits^{ + 5} {O_3},Na\mathop {Cl}\limits^{ + 7} {O_4}\) Đáp án C
Câu 6 :
Cho các phát biểu sau: (a) Sự oxi hóa là sự nhường electron hay sự làm tăng số oxi hóa. (b) Trong quá trình oxi hóa, chất khử nhận electron. (c) Sự khử là sự nhận electron hay là sự làm giảm số oxi hóa. (d) Trong quá trình khử, chất oxi hóa nhường electron. (e) Trong quá trình khử, chất oxi hóa nhận electron và bị khử xuống số oxi hóa thấp hơn. (f) Trong quá trình oxi hóa, chất khử nhường electron và bị oxi hóa lên số oxi hóa cao hơn. Số phát biểu đúng là
Đáp án : A Phương pháp giải :
Dựa vào kiến thức về phản ứng oxi hóa khử Lời giải chi tiết :
(a) đúng (b) sai, chất khử nhường electron (c) đúng (d) sai, chất oxi hóa nhận electron (e) đúng (f) đúng Đáp án A
Đáp án : B Phương pháp giải :
Cân bằng phương trình theo phương pháp bảo toàn electron Lời giải chi tiết :
Tỉ lệ a:d là 1:1 Đáp án B
Câu 8 :
Cho 4,8 gam Mg tác dụng với lượng dư dung dịch HNO3 đặc, nóng thu được V lít khí NO2 (ở đkc, là sản phẩm khử duy nhất). Giá trị của V là
Đáp án : A Phương pháp giải :
Dựa vào bảo toàn electron Lời giải chi tiết :
Mg + 4HNO3 \( \to \)Mg(NO3)2 + 2NO2 + 2H2O 0,2 \( \to \) 0,4 V NO2 = 0,4 . 24,79 = 9,916 lít Đáp án A
Câu 9 :
Chlorine vừa đóng vai trò chất oxi hóa, vừa đóng vai trò chất khử trong các phản ứng nào sau đây?
Đáp án : D Phương pháp giải :
Chất vừa đóng vai trò chất oxi hóa, vừa đóng vai trò chất khử là chất vừa tăng và giảm số oxi hóa Lời giải chi tiết :
2 NaOH + Cl2 \( \to \)NaCl + NaClO + H2O Cl2 đóng vai trò vừa là chất khử vừa là chất oxi hóa Đáp án D
Câu 10 :
Phát biểu nào sau đây đúng?
Đáp án : A Lời giải chi tiết :
Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298K Đáp án A
Câu 11 :
Nung nóng hai ống nghiệm chứa NaHCO3 và P, xảy ra các phản ứng sau: 2 NaHCO3 (s) \( \to \)Na2CO3(s) + CO2(g) + H2O(g) (1) 4P(s) + 5O2(g) \( \to \)2P2O5(s) (2) Khi ngừng đun nóng, phản ứng (1) dừng lại còn phản ứng (2) tiếp tục xảy ra, chứng tỏ
Đáp án : B Phương pháp giải :
Dựa vào khái niệm về phản ứng thu nhiệt và tỏa nhiệt Lời giải chi tiết :
Khi ngừng đun nóng, phản ứng (1) dừng lại => (1) là phản ứng thu nhiệt; phản ứng (2) tiếp tục xảy ra => (2) là phản ứng tỏa nhiệt Đáp án B
Câu 12 :
Cho phản ứng hóa học xảy ra ở điều kiện chuẩn sau: 2NO2 (đỏ nâu) \( \to \)N2O4 (không màu) Biết NO2 và N2O4 có \({\Delta _f}H_{298}^0\)tương ứng là 33,18 KJ/mol và 9,16 KJ/mol. Điều này chứng tỏ phản ứng
Đáp án : C Phương pháp giải :
Dựa vào enthalpy tạo thành chuẩn của chất Lời giải chi tiết :
\({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0({N_2}{{\rm{O}}_4}) - {\Delta _f}H_{298}^0(N{O_2})\)= 9,16 – 33,18 = -24,02 => phản ứng tỏa nhiệt N2O4 bền hơn NO2 Đáp án C
Câu 13 :
Cho các phản ứng sau: (1) C (s) + CO2(g) \( \to \) 2CO (g) \({\Delta _r}H_{298}^0 = 173,6kJ\) (2) C (s) + H2O (g) \( \to \)CO (g) + H2 (g) \({\Delta _r}H_{298}^0 = 133,8kJ\) (3) CO (g) + H2O (g) \( \to \)CO2 (g) + H2 (g) Ở 500K, 1 atm, biến thiên enthalpy của phản ứng (3) có giá trị là
Đáp án : A Phương pháp giải :
Dựa vào biến thiên enthalpy của phản ứng (1) và (2) Lời giải chi tiết :
\({\Delta _r}H_{298}^0(3) = {\Delta _r}H_{298}^0(2) - {\Delta _r}H_{298}^0(1)\)= 133,8 – 173,6 = -39,8 kJ Đáp án A
Câu 14 :
Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn: (1) \({N_2}(g) + {O_2}(g) \to 2NO(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0(1)\) (2) \(NO(g) + \frac{1}{2}{O_2}(g) \to N{O_2}(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0(2)\) Cho các phát biểu sau:
Số phát biểu không đúng là
Đáp án : C Phương pháp giải :
Dựa vào kiến thức về biến thiên enthalpy của phản ứng Lời giải chi tiết :
(a) đúng (b) sai, vì enthalpy chuẩn được tạo ra từ các đơn chất bền vững (c) đúng (d) đúng (e) đúng Đáp án C
Câu 15 :
Cho enthalpy tạo thành chuẩn của một số chất sau:
Biến thiên enthalpy chuẩn của phản ứng: CaCO3(s) \( \to \)CaO(s) + CO2(g)
Đáp án : D Phương pháp giải :
Dựa vào enthalpy tạo thành chuẩn của chất Lời giải chi tiết :
\({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0(CaO) + {\Delta _f}H_{298}^0(C{O_2}) - {\Delta _f}H_{298}^0(CaC{O_3})\)= -635,10 + (-393,50) – (-1206,90) = 178,3 kJ Đáp án D
Câu 16 :
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
Biến thiên enthalpy của phản ứng C3H8(g) → CH4(g) + C2H4(g) có giá trị là
Đáp án : C Phương pháp giải :
Dựa vào năng lượng liên kết của chất Lời giải chi tiết :
\({\Delta _r}H_{298}^0\)= EC3H8 – ECH4 – EC2H4 = 2. EC-C + 8. E C-H – 4. E C-H – E C=C – 4 E C-H = 2.346 + 8. 418 – 4.418 – 612 – 4.418 = 80 KJ Đáp án C
Câu 17 :
Cho phản ứng sau: 2SO2 (g) + O2 (g) → 2SO3 (g) Biết (kJ.mol-1 ) của SO2 và SO3 lần lượt là –296,83 và –395,72. Biến thiên enthalpy của phản ứng trên ở điều kiện chuẩn có giá trị là
Đáp án : B Phương pháp giải :
Dựa vào công thức tính biến thiên enthalpy Lời giải chi tiết :
\({\Delta _r}H_{298}^0\)= 2. \({\Delta _f}H_{298}^0\)(SO3) – 2.\({\Delta _f}H_{298}^0\)(SO2) - \({\Delta _f}H_{298}^0\)(O2) = 2. -395,72 – 2.(-296,83) – 0 = -197,78 kJ Đáp án B
Câu 18 :
Nhiệt tạo thành chuẩn của một chất là nhiệt lượng tạo thành 1 mol chất đó từ chất nào ở điều kiện chuẩn?
Đáp án : B Phương pháp giải :
Dựa vào khái niệm nhiệt tạo thành chuẩn của chất Lời giải chi tiết :
Nhiệt tạo thành chuẩn của một chất là lượng nhiệt tạo thành 1 mol chất từ những đơn chất bền vững nhất ở điều kiện chuẩn Đáp án B
Câu 19 :
Phản ứng nào sau đây là phản ứng toả nhiệt?
Đáp án : C Phương pháp giải :
Dựa vào khái niệm về phản ứng tỏa nhiệt, phản ứng thu nhiệt Lời giải chi tiết :
Phản ứng oxi hóa glucose trong cơ thể là phản ứng tỏa nhiệt
Câu 20 :
Cho các phát biểu: (a) Biến thiên enthalpy chuẩn của một phản ứng hóa học là lượng nhiệt kèm theo phản ứng đó ở áp suất 1 atm và 25o C. (b) Nhiệt (tỏa ra hay thu vào) kèm theo một phản ứng được thực hiện ở 1 bar và 298 K là biến thiên enthalpy chuẩn của phản ứng đó. (c) Một số phản ứng khi xảy ra làm môi trường xung quanh nóng lên là phản ứng thu nhiệt. (d) Một số phản ứng khi xảy ra làm môi trường xung quanh lạnh đi là do các phản ứng này thu nhiệt và lấy nhiệt từ môi trường. Số phát biểu đúng là
Đáp án : A Phương pháp giải :
Dựa vào phản ứng tỏa nhiệt và phản ứng thu nhiệt Lời giải chi tiết :
(a) sai, áp suất 1 bar và 298K (b) đúng (c) sai, đó là phản ứng tỏa nhiệt (d) đúng Đáp án A
|














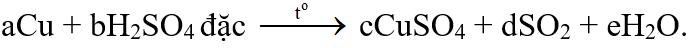

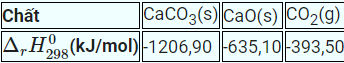

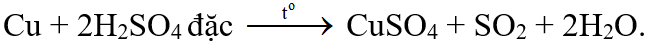









Danh sách bình luận