Đề thi giữa kì 2 Hóa 11 - Đề số 3Đề bài
Câu 1 :
Đốt cháy hoàn toàn ankin A thu được 19,8 gam CO2 và 5,4 gam nước. Ankin A là
Câu 2 :
Cho chất axetilen (C2H2) và benzen (C6H6), hãy chọn nhận xét đúng trong các nhận xét sau :
Câu 3 :
Sản phẩm của phản ứng thế clo (1:1, ánh sáng) vào 2,2-đimetylpropan là : (1) (CH3)3CCH2Cl (2) CH3C(CH2Cl)2CH3 (3) CH3ClC(CH3)3
Câu 4 :
Kết luận nào sau đây là đúng ?
Câu 5 :
Cho các chất: xiclobutan, 2-metylpropen, but-1-en, cis-but-2-en, 2-metylbut-2-en. Dãy gồm các chất sau khi phản ứng với H2 (dư, xúc tác Ni, to), cho cùng một sản phẩm là:
Câu 6 :
Cho propen, propin, đivinyl tác dụng với HCl (tỉ lệ 1 : 1), số sản phẩm thu được lần lượt là
Câu 7 :
Trùng hợp 60 kg propilen thu được m kg polime, biết H = 70%. Giá trị của m là
Câu 8 :
Có bao nhiêu ankađien có công thức phân tử C4H6 ?
Câu 9 :
Hỗn hợp X gồm 3 khí C3H4, C2H2 và H2 cho vào bình kín dung tích 8,96 lít (đktc) chứa bột Ni, nung nóng bình một thời gian thu được hỗn hợp khí Y. Biết tỉ khối của X so với Y là 0,75. Số mol H2 tham gia phản ứng là:
Câu 10 :
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 16,80 lít khí CO2 ; 2,80 lít N2 (các thể tích đo ở đktc) và 20,25 gam H2O. CTPT của X là :
Câu 11 :
Thực hiện phản ứng đề hiđro hóa một hiđrocacbon M thuộc dãy đồng đẳng của metan thu được một hỗn hợp gồm H2 và 3 hiđrocacbon N, P, Q. Đốt cháy hoàn toàn 4,48 lít khí N hoặc P, hoặc Q đều thu được 17,92 lít CO2 và 14,4 gam H2O (thể tích các khí ở đktc). Công thức cấu tạo của M là
Câu 12 :
Hỗn hợp khí X gồm axetilen và propilen. Cho V lít hỗn hợp X đi qua dung dịch AgNO3/NH3 dư thu được 96 gam kết tủa. Mặt khác V lít hỗn hợp X phản ứng vừa đủ với 20,16 lít H2. Các thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của V là
Câu 13 :
Phân tử metan không tan trong nước vì lí do nào sau đây ?
Câu 14 :
Cho hỗn hợp 2 ankan A và B ở thể khí, có tỉ lệ số mol trong hỗn hợp nA : nB = 1 : 4. Khối lượng phân tử trung bình là 52,4. Công thức phân tử của hai ankan A và B lần lượt là :
Câu 15 :
Trong bình kín (ở 210oC) đựng hỗn hợp A (gồm 2 ankin X và Y là đồng đẳng liên tiếp, MX < MY). Thêm một lượng không khí vừa đủ (khi đó áp suất trong bình đạt 0,81 atm) rồi bật tia lửa điện để đốt cháy hết X và Y rồi đưa bình về 210oC, thấy áp suất trong bình = 0,836 atm. Biết trong không khí chứa 80% thể tích N2, còn lại là O2. CTPT của Y là
Câu 16 :
Thực hiện phản ứng crackinh m gam isobutan, thu được hỗn hợp A gồm các hiđrocacbon. Dẫn hỗn hợp A qua bình nước brom có hòa tan 6,4 gam brom. Nước brom mất màu hết, có 4,704 lít hỗn hợp khí B (đktc) gồm các hiđrocacbon thoát ra. Tỉ khối hơi B so với hiđro bằng 117/7 . Giá trị của m là:
Câu 17 :
Cho các chất sau: pentan; hex-1-en, etilen, metan, propen, isobutan. Số các chất làm mất màu dung dịch KMnO4 ở ngay điều kiện thường là
Câu 18 :
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni. Nung nóng bình một thời gian, thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào lượng dư dung dịch AgNO3 trong NH3 đến phản ứng hoàn toàn, thu được hỗn hợp khí Y và 12 gam kết tủa. Hỗn hợp khí Y phản ứng vừa đủ với bao nhiêu mol Br2 trong dung dịch?
Câu 19 :
Công thức đơn giản nhất của một hiđrocacbon là CnH2n+1. Hiđrocacbon đó thuộc dãy đồng đẳng của:
Câu 20 :
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ (xích ma) và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là:
Câu 21 :
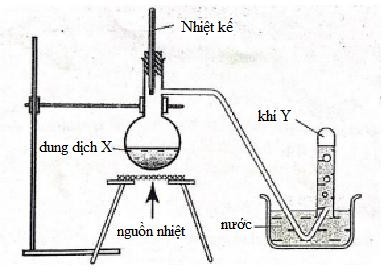
Cho hình vẽ mô tả thí nghiệm điều chế Y từ dung dịch X.
X có thể chứa
Câu 22 :
Một chất có CTĐGN là CH3. CTPT chất đó là
Câu 23 :
Liên kết đôi do những liên kết nào hình thành ?
Câu 24 :
Ứng với công thức phân tử C6H14 có bao nhiêu đồng phân mạch cacbon ?
Câu 25 :
Cho ankan X có CTPT là C6H14, biết rằng khi cho X tác dụng với clo theo tỉ lệ mol 1:1 thu được 2 sản phẩm thế monoclo. CTCT đúng của X là
Câu 26 :
Đốt cháy 4,4 gam hỗn hợp CH4, C2H4, C3H6, C4H10 cần a mol O2 thu được b mol CO2 và 7,2 gam H2O. Giá trị a, b lần lượt là
Câu 27 :
Để điều chế C2H6 có thể nung hỗn hợp chất X với “vôi tôi – xút”, X là
Câu 28 :
Ứng với công thức phân tử C5H10 có bao nhiêu anken ?
Câu 29 :
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp X gồm CH4, C2H4 thu được 0,15 mol CO2 và 0,2 mol H2O. Giá trị của V là
Câu 30 :
Số đồng phân cấu tạo (mạch hở) có công thức phân tử C5H8 là
Câu 31 :
Gọi tên chất: \(C{H_3} - CH(C{H_3}) - C \equiv C - C{H_2} - C{H_3}\)
Câu 32 :
Trong phân tử ankin X, hiđro chiếm 12,2% về khối lượng. Có bao nhiêu ankin phù hợp với X?
Câu 33 :
Hỗn hợp X gồm hai anken là chất khí ở điều kiện thường. Hiđrat hóa X thu được hỗn hợp Y gồm bốn ancol (không có ancol bậc III). Anken trong X là
Câu 34 :
Hỗn hợp X gồm C2H4 và H2 có tỷ lệ mol 1:1. Cho hỗn hợp X qua Ni, t0 thu được hỗn hợp Y. Cho hỗn hợp Y vào dung dịch brom dư thu được hỗn hợp khí Z. Tỷ khối của Z so với H2 là 11,5. Vậy hiệu suất phản ứng hiđro hóa là
Câu 35 :
Trùng hợp propen, sản phẩm thu được có cấu tạo là
Câu 36 :
Cho các phương trình hóa học (1) \(C{H_3} - C \equiv CH + {H_2}O\xrightarrow{{H{g^{2 + }},{t^0}}}C{H_3}C{H_2}CHO\) (spc) (2) \(C{H_3} - C \equiv CH + AgN{O_3} + N{H_3}\xrightarrow{{{t^0}}}C{H_3} - C \equiv CAg + N{H_4}N{O_3}\) (3) \(C{H_3} - C \equiv CH + 2{H_2}\xrightarrow{{Ni,{t^0}}}C{H_3}C{H_2}C{H_3}\) (4) \(3C{H_3} - C \equiv CH\xrightarrow{{xt,{t^0},p}}\) Các phương trình hóa học viết sai là
Câu 37 :
Dãy nào sau đây chứa các chất làm nhạt màu dung dịch nước brom và thuốc tím?
Câu 38 :
Một hiđrocacbon A mạch thẳng có công thức phân tử là C6H6. Khi cho A tác dụng với dung dịch AgNO3/NH3 dư thu được hợp chất hữu cơ B có MB – MA = 214 đvC. Công thức cấu tạo của X có thể là
Câu 39 :
Hiđro hóa hoàn toàn ankin X (xt Pd, PbCO3) thu được anken Y có công thức phân tử là C5H10. Vậy Y không thể là anken nào sau đây?
Câu 40 :
Khi brom hóa một ankan chỉ thu được một dẫn xuất monobrom duy nhất có tỉ khối hơi đối với hiđro là 75,5. Tên của ankan đó là:
Lời giải và đáp án
Câu 1 :
Đốt cháy hoàn toàn ankin A thu được 19,8 gam CO2 và 5,4 gam nước. Ankin A là
Đáp án : B Phương pháp giải :
+) Đốt cháy ankin ta có: nankin = nCO2 – nH2O +) số C trong A = nCO2 / nankin Lời giải chi tiết :
nCO2 = 0,45 mol; nH2O = 0,3 mol Đốt cháy ankin ta có: nankin = nCO2 – nH2O = 0,45 – 0,3 = 0,15 mol => số C trong A = nCO2 / nankin = 0,45 / 0,15 = 3 => ankin A là C3H4
Câu 2 :
Cho chất axetilen (C2H2) và benzen (C6H6), hãy chọn nhận xét đúng trong các nhận xét sau :
Đáp án : B Lời giải chi tiết :
Công thức đơn giản nhất của axetilen: CH Công thức đơn giản nhất của benzen: CH => 2 chất khác nhau về công thức phân tử và giống nhau về công thức đơn giản nhất
Câu 3 :
Sản phẩm của phản ứng thế clo (1:1, ánh sáng) vào 2,2-đimetylpropan là : (1) (CH3)3CCH2Cl (2) CH3C(CH2Cl)2CH3 (3) CH3ClC(CH3)3
Đáp án : D Phương pháp giải :
Xem lại lí thuyết phản ứng halogen hóa của ankan Lời giải chi tiết :
2,2-đimetylpropan: (CH3)3C-CH3 => chỉ có 1 vị trí thế Cl (CH3)3C-CH3 + Cl2 → (CH3)3C-CH2Cl + HCl
Câu 4 :
Kết luận nào sau đây là đúng ?
Đáp án : D Lời giải chi tiết :
Câu đúng là: Các chất khác nhau có cùng công thức phân tử được gọi là các chất đồng phân của nhau.
Câu 5 :
Cho các chất: xiclobutan, 2-metylpropen, but-1-en, cis-but-2-en, 2-metylbut-2-en. Dãy gồm các chất sau khi phản ứng với H2 (dư, xúc tác Ni, to), cho cùng một sản phẩm là:
Đáp án : A Lời giải chi tiết :
Xiclobutan cộng H2 mở vòng tạo butan 2-metylpropen cộng H2 tạo thành 2-metylpropan but-1-en cộng H2 tạo thành butan cis-but-2-en cộng H2 tạo thành butan 2-metylbut-2-en cộng H2 tạp thành 2-metylbutan => Dãy các chất cộng H2 cho cùng 1 sản phẩm là: xiclobutan, but-1-en, cis-but-2-en
Câu 6 :
Cho propen, propin, đivinyl tác dụng với HCl (tỉ lệ 1 : 1), số sản phẩm thu được lần lượt là
Đáp án : B Phương pháp giải :
Xem lại lí thuyết phản ứng cộng ankin, cộng anken và ankađien Lời giải chi tiết :
Propen: CH2=CH-CH3 + HCl → CH3-CHCl-CH3 + CH2Cl-CH2-CH3 Propin: CH≡C-CH3 + HCl → CH2=CCl-CH3 + CHCl=CH-CH3 (có đphh) => propin thu được 3 sản phẩm Đivinyl: CH2=CH-CH=CH2 có 2 kiểu cộng 1,2 và cộng 1,4 (xem lại lí thuyết ankađien) CH2=CH-CH=CH2 + HCl → CH2=CH-CH2-CH2Cl + CH2=CH-CHCl-CH3 CH2=CH-CH=CH2 + HCl → CH3-CH=CH-CHCl (có đphh) => đivinyl thu được 4 sản phẩm
Câu 7 :
Trùng hợp 60 kg propilen thu được m kg polime, biết H = 70%. Giá trị của m là
Đáp án : A Phương pháp giải :
Bảo toàn khối lượng: mpolime lí thuyết = mpropilen => nhân hiệu suất tính mpolime thực tế Lời giải chi tiết :
nCH2=CH-CH3 → (-CH2-CH(CH3)-)n Theo lí thuyết: mpolime = mpropilen = 60 kg => mpolime thực tế = 60.70/100 = 42 kg
Câu 8 :
Có bao nhiêu ankađien có công thức phân tử C4H6 ?
Đáp án : A Phương pháp giải :
+) Đặt 1 nối đôi C=C cố định ở đầu => di chuyển nối đôi còn lại để tạo thành các đồng phân Lời giải chi tiết :
1. CH2=C=CH-CH3 2. CH2=CH-CH=CH2 Mạch nhánh không có đồng phân ankađien vì thừa liên kết hóa trị của C
Câu 9 :
Hỗn hợp X gồm 3 khí C3H4, C2H2 và H2 cho vào bình kín dung tích 8,96 lít (đktc) chứa bột Ni, nung nóng bình một thời gian thu được hỗn hợp khí Y. Biết tỉ khối của X so với Y là 0,75. Số mol H2 tham gia phản ứng là:
Đáp án : C Phương pháp giải :
+) \(\frac{{{{\overline M }_X}}}{{{{\overline M }_Y}}} = \frac{{{n_Y}}}{{{n_X}}}\) +) \({n_{{H_2}}}\)phản ứng = ngiảm = nX – nY Lời giải chi tiết :
nX = 0,4 mol Ta có: \({d_{X/Y}} = \frac{{{{\overline M }_X}}}{{{{\overline M }_Y}}} = \frac{{{n_Y}}}{{{n_X}}} = \frac{{{n_Y}}}{{0,4}} = 0,75 \Rightarrow {n_Y} = 0,3{\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} (mol)\) => \({n_{{H_2}}}\)phản ứng = ngiảm = nX – nY = 0,4 – 0,3 = 0,1 mol
Câu 10 :
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 16,80 lít khí CO2 ; 2,80 lít N2 (các thể tích đo ở đktc) và 20,25 gam H2O. CTPT của X là :
Đáp án : D Phương pháp giải :
+) Bảo toàn nguyên tố C: ${{n}_{C}}={{n}_{C{{O}_{2}}}}$ +) Bảo toàn nguyên tố H: $\,{{n}_{H}}=2.{{n}_{{{H}_{2}}O}}$ +) Bảo toàn nguyên tố N: ${{n}_{N}}=2.{{n}_{{{N}_{2}}}}$ +) Tính $ {{n}_{C}}:{{n}_{H}}:{{n}_{N}}$ => CTPT Lời giải chi tiết :
Bảo toàn nguyên tố C: ${{n}_{C}}={{n}_{C{{O}_{2}}}}=\frac{16,8}{22,4}=0,75\,\,mol$ Bảo toàn nguyên tố H: $\,{{n}_{H}}=2.{{n}_{{{H}_{2}}O}}=2.\frac{20,25}{18}=2,25\,\,mol$ Bảo toàn nguyên tố N: ${{n}_{N}}=2.{{n}_{{{N}_{2}}}}=2.\frac{2,8}{22,4}=0,25\,\,mol$ $\Rightarrow {{n}_{C}}:{{n}_{H}}:{{n}_{N}}=0,75:2,25:0,25=3:9:1$ Căn cứ vào các phương án ta thấy CTPT của X là C3H9N
Câu 11 :
Thực hiện phản ứng đề hiđro hóa một hiđrocacbon M thuộc dãy đồng đẳng của metan thu được một hỗn hợp gồm H2 và 3 hiđrocacbon N, P, Q. Đốt cháy hoàn toàn 4,48 lít khí N hoặc P, hoặc Q đều thu được 17,92 lít CO2 và 14,4 gam H2O (thể tích các khí ở đktc). Công thức cấu tạo của M là
Đáp án : D Phương pháp giải :
+) nH2O = nCO2 => hiđrocacbon đốt cháy là anken CnH2n + O2 → nCO2 + nH2O +) Từ số mol CO2 => tính n => CTPT của anken +) Khi đốt cháy N hoặc P hoặc Q đều cho số mol CO2 và H2O giống nhau CH3-CH2-CH2-CH3 (1) CH3-CH(CH3)-CH3 (2) +) Trong 2 đồng phân trên chỉ có (1) tách hiđro cho 3 sản phẩm là đồng phân của nhau Lời giải chi tiết :
nN = 0,2mol; nCO2 = 0,8 mol ; nH2O = 0,8 mol Ta thấy: nH2O = nCO2 => hiđrocacbon N là anken CnH2n + O2 → nCO2 + nH2O 0,2 0,8 => 0,2n = 0,8 => n = 4 => anken là C4H8 => N, P, Q là các đồng phân của nhau và cùng CTPT là C4H8 CH3-CH2-CH2-CH3 (1) CH3-CH(CH3)-CH3 (2) Trong 2 đồng phân trên chỉ có (1) tách hiđro cho 3 sản phẩm là đồng phân của nhau CH3-CH2-CH2-CH3 à CH3-CH=CH-CH3 + H2 (cis-trans) CH3-CH2-CH2-CH3 à CH2=CH-CH2-CH3 + H2
Câu 12 :
Hỗn hợp khí X gồm axetilen và propilen. Cho V lít hỗn hợp X đi qua dung dịch AgNO3/NH3 dư thu được 96 gam kết tủa. Mặt khác V lít hỗn hợp X phản ứng vừa đủ với 20,16 lít H2. Các thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của V là
Đáp án : A Phương pháp giải :
+) Chỉ có C2H2 phản ứng với dung dịch AgNO3/NH3 => số mol C2H2 +) Từ phản ứng cộng H2 => tính số mol C3H6
Lời giải chi tiết :
$\begin{array}{l}{n_{{C_2}A{g_2}}}\,\, = \,\,\frac{{96}}{{240}}\,\, = \,\,0,4\,\,mol\,\, \to \,\,{n_{{C_2}{H_2}}}\,\, = \,\,0,4\,\,mol\\{n_{{H_2}}}\,\, = \,\,\frac{{20,16}}{{22,4}}\,\, = \,\,0,9\,\,mol\end{array}$ C2H2 + 2H2 → C2H6 0,4 → 0,8 Số mol H2 phản ứng với C3H6: 0,9 – 0,8 = 0,1 mol C3H6 + H2 → C3H8 0,1 ← 0,1 → V = (0,4 + 0,1).22,4 = 11,2 lít
Câu 13 :
Phân tử metan không tan trong nước vì lí do nào sau đây ?
Đáp án : B Phương pháp giải :
Xem lại lí thuyết ankan Lời giải chi tiết :
Phân tử metan không tan trong nước vì phân tử metan không phân cực.
Câu 14 :
Cho hỗn hợp 2 ankan A và B ở thể khí, có tỉ lệ số mol trong hỗn hợp nA : nB = 1 : 4. Khối lượng phân tử trung bình là 52,4. Công thức phân tử của hai ankan A và B lần lượt là :
Đáp án : A Phương pháp giải :
Gọi công thức phân tử trong bình là ${{C}_{{\bar{n}}}}{{H}_{2\bar{n}+2}}$ +) Từ khối lượng phân tử trung bình => tính n trung bình Giả sử A đúng => số mol mỗi chất $=>\,\bar{C}$ Giả sử D đúng => số mol mỗi chất $=>\,\bar{C}$ Lời giải chi tiết :
Gọi công thức phân tử trong bình là ${{C}_{{\bar{n}}}}{{H}_{2\bar{n}+2}}$ $=>14\bar{n}+2=52,4\,\,=>\,\bar{n}=3,6$ => loại B vì 2 chất có số C > 3,6 và loại C vì 2 chất đều có số C < 3,6 Giả sử A đúng => nC2H6 = 1 mol ; nC4H10 = 4 mol $=>\,\,\bar{C}=\frac{2.1+4.4}{1+4}=3,6$ (thỏa mãn) Giả sử D đúng => nC4H10 = 1 mol ; nC3H8 = 4 mol $=>\,\,\bar{C}=\frac{4.1+3.4}{1+4}=3,2$ (loại)
Câu 15 :
Trong bình kín (ở 210oC) đựng hỗn hợp A (gồm 2 ankin X và Y là đồng đẳng liên tiếp, MX < MY). Thêm một lượng không khí vừa đủ (khi đó áp suất trong bình đạt 0,81 atm) rồi bật tia lửa điện để đốt cháy hết X và Y rồi đưa bình về 210oC, thấy áp suất trong bình = 0,836 atm. Biết trong không khí chứa 80% thể tích N2, còn lại là O2. CTPT của Y là
Đáp án : C Phương pháp giải :
+) Gọi nCO2 = a mol; nH2O = b mol +) nankin = nCO2 – nH2O => nankin = a – b +) Bảo toàn O: 2.nO2 = 2.nCO2 + nH2O +) nhh trước pứ = nankin + nO2 + nN2 +) nhh sau phản ứng = nCO2 + nH2O + nN2 Từ công thức $pV = n.R.T{\rm{ }} = > \frac{{{p_t}}}{{{p_s}}} = \frac{{{n_t}}}{{{n_s}}}\,\,$ Lời giải chi tiết :
Ở 210oC, nước ở thể hơi => coi như là 1 khí gây áp suất trong bình Vì lượng không khí dùng vừa đủ => hỗn hợp sau phản ứng gồm CO2, H2O và N2 Gọi nCO2 = a mol; nH2O = b mol => nankin = nCO2 – nH2O => nankin = a – b Bảo toàn O: 2.nO2 = 2.nCO2 + nH2O => nO2 = a + 0,5b Trong không khí: nN2 = 4.nO2 = 4a + 2b => nhh trước pứ = nankin + nO2 + nN2 = a – b + a + 0,5b + 4a + 2b = 6a + 1,5b nhh sau phản ứng = nCO2 + nH2O + nN2 = a + b + 4a + 2b = 5a + 3b Từ công thức $pV = n.R.T{\rm{ }} = > \frac{{{p_t}}}{{{p_s}}} = \frac{{{n_t}}}{{{n_s}}}\,\, = > \,\,\frac{{0,81}}{{0,836}} = \frac{{6a + 1,5b}}{{5a + 3b}}\,\, = > \,a = 1,21b$ => nankin = a – b = 1,21b – b = 0,21b mol => số C trung bình = nCO2 / nankin = 1,21 / 0,21 = 5,76 => 2 ankin X và Y là C5H8 và C6H10
Câu 16 :
Thực hiện phản ứng crackinh m gam isobutan, thu được hỗn hợp A gồm các hiđrocacbon. Dẫn hỗn hợp A qua bình nước brom có hòa tan 6,4 gam brom. Nước brom mất màu hết, có 4,704 lít hỗn hợp khí B (đktc) gồm các hiđrocacbon thoát ra. Tỉ khối hơi B so với hiđro bằng 117/7 . Giá trị của m là:
Đáp án : A Phương pháp giải :
+) Từ \(\bar{M}\)hh khí xét xem khí ra khỏi dung dịch brom là những khí nào +) nC3H6 phản ứng = nBr2 +) Bảo toàn khối lượng ta có: mC4H10 = mC3H6 phản ứng + mhh khí Lời giải chi tiết :
nBr2 = 0,04 mol; nhh khí = 0,21 mol Khi dẫn hỗn hợp A gồm các hiđrocacbon qua dung dịch brom, brom bị mất màu hết => anken trong hỗn hợp A có thể còn dư. \(\bar{M}\)hh khí = $\frac{117}{7}$.2 = $\frac{234}{7}$ ≈ 33,43 < MC3H6 = 42 => khí đi ra khỏi dung dịch brom có C3H6 => nC3H6 phản ứng = nBr2 = 0,04 mol Áp dụng định luật bảo toàn khối lượng ta có: mC4H10 = mC3H6 phản ứng + mhh khí = 0,04.42 + $\frac{234}{7}$.0,21 = 8,7 (g)
Câu 17 :
Cho các chất sau: pentan; hex-1-en, etilen, metan, propen, isobutan. Số các chất làm mất màu dung dịch KMnO4 ở ngay điều kiện thường là
Đáp án : B Lời giải chi tiết :
Các anken phản ứng được với dung dịch KMnO4 ở ngay điều kiện thường => hex-1-en, etilen, propen
Câu 18 :
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni. Nung nóng bình một thời gian, thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào lượng dư dung dịch AgNO3 trong NH3 đến phản ứng hoàn toàn, thu được hỗn hợp khí Y và 12 gam kết tủa. Hỗn hợp khí Y phản ứng vừa đủ với bao nhiêu mol Br2 trong dung dịch?
Đáp án : C Phương pháp giải :
+) Bảo toàn khối lượng: mhh ban đầu = mhh X +) n khí giảm = nH2 phản ứng +) n C2H2 dư = nAg2C2 +) Bảo toàn liên kết π: n π trong Y = np ban đầu – nH2 – 2.nC2H2 dư +) n Br2 pư với Y = nπ trong Y Lời giải chi tiết :
Số mol hỗn hợp ban đầu = 0,35 + 0,65 = 1 mol Khối lượng hỗn hợp ban đầu = 0,35. 26 + 0,65.2 = 10,4 gam Số mol liên kết π = 0,35.2 = 0,7 mol Bảo toàn khối lượng: mhh ban đầu = mhh X =10,4 gam => nX = 10,4/16 = 0,65 mol n khí giảm = nH2 phản ứng = 0,35 mol Ta có: n C2H2 dư = nAg2C2 = 0,05 mol Bảo toàn liên kết π : n π trong Y = np ban đầu – nH2 – 2.nC2H2 dư = 0,7 – 0,35 – 0,05.2 = 0,25 mol => nBr2 pư với Y = nπ trong Y = 0,25 mol Chú ý
+ tính số π trong Y quên không trừ π của C2H2 dư => chọn nhầm A + Trừ nhầm số π của C2H2 dư => chọn nhầm D
Câu 19 :
Công thức đơn giản nhất của một hiđrocacbon là CnH2n+1. Hiđrocacbon đó thuộc dãy đồng đẳng của:
Đáp án : A Phương pháp giải :
+) Gọi công thức phân tử của hiđrocacbon cần tìm là (CnH2n+1)a +) Trong phân tử một hiđrocacbon bất kì luôn chẵn nên k chắn => k có thể là 2 => Công thức phân tử
Lời giải chi tiết :
Gọi CTPT của hidrocacbon là ${({C_n}{H_{2n}}_{ + 1})_{a\,\,\,}}$ Vì số H luôn là số chẵn nên a = 2 => CTPT: C2nH4n+2 Đặt m = 2n => CTPT là CmH2m+2 => Ankan hidrocacbon thuộc dãy đồng đẳng ankan Chú ý
Đề bài cho công thức đơn giản nhất chứ công phải công thức phân tử, các em đừng nhầm lẫn nhé.
Câu 20 :
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ (xích ma) và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là:
Đáp án : C Phương pháp giải :
+) Số nguyên tử $C = \dfrac{{{n_{C{O_2}}}}}{{{n_X}}}$ + X chỉ chứa liên kết σ (xích ma) => CTPT của X +) Trong X có 2 nguyên tử C bậc 3 => CTCT của X Lời giải chi tiết :
X là hiđrocacbon mạch hở chỉ chứa liên kết σ → X là ankan Số nguyên tử $C = \dfrac{{{n_{C{O_2}}}}}{{{n_X}}} = \dfrac{{{V_{C{O_2}}}}}{{{V_X}}} = 6 \to X:{C_6}{H_{14}}$ Trong X có 2 nguyên tử C bậc 3 nên X là: ${(C{H_3})_2}CH - CH{(C{H_3})_2}$ (2,3-đimetylbutan) Ta có: ${(C{H_3})_2}CH - CH{(C{H_3})_2}\,\,\, + \,\,\,C{l_2}\,\,\,\,\xrightarrow[{ - HCl}]{{as}}\,\,\,\left\{ \begin{gathered}C{H_2}Cl - CH(C{H_3}) - CH{(C{H_3})_2} \hfill \\{(C{H_3})_2}CCl - CH{(C{H_3})_2} \hfill \\ \end{gathered} \right.\,\,\,$
Câu 21 :
Cho hình vẽ mô tả thí nghiệm điều chế Y từ dung dịch X.
X có thể chứa
Đáp án : D Phương pháp giải :
Khí Y điều chế bằng phương pháp đẩy nước → Y không tan hoặc ít tan trong nước và không có phản ứng với nước → chọn được phương trình điều chế Y thích hợp Lời giải chi tiết :
Khí Y điều chế bằng phương pháp đẩy nước → Y không tan hoặc ít tan trong nước A. 2KMnO4 + 16HCl đặc 2KCl + 2MnCl2 + 5Cl2 + 8H2O → loại vì Cl2 phản ứng với nước. B. Không có pư C. NH4Cl + NaOH → NH3↑ + NaCl + H2O → loại vì NH3 tan nhiều trong nước. D. C2H5OH \(\buildrel {{H_2}S{O_4}\,đặc,{t^0}} \over\longrightarrow \) C2H4 + H2O → chọn vì C2H4 không tan trong nước và không có pư với H2O
Câu 22 :
Một chất có CTĐGN là CH3. CTPT chất đó là
Đáp án : B Phương pháp giải :
Công thức phân tử của chất có dạng là CnH3n Mặt khác trong hidrocacbon ta luôn có: H ≤ 2C + 2 và H là số chẵn. Tìm điều kiện của n. Lời giải chi tiết :
Công thức phân tử của chất có dạng là CnH3n Mặt khác trong hidrocacbon ta luôn có: H ≤ 2C + 2 => 3n ≤ 2n + 2 => n ≤ 2 Mà số H chẵn nên ta suy ra n = 2 => CTPT C2H6
Câu 23 :
Liên kết đôi do những liên kết nào hình thành ?
Đáp án : C Phương pháp giải :
Xem lại lí thuyết cấu trúc phân tử HCHC Lời giải chi tiết :
Liên kết đôi giữa hai nguyên tử cacbon gồm một liên kết \(\sigma \) và một liên kết p
Câu 24 :
Ứng với công thức phân tử C6H14 có bao nhiêu đồng phân mạch cacbon ?
Đáp án : C Lời giải chi tiết :
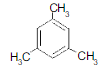
- Đồng phân mạch thẳng: C – C – C – C – C – C - Đồng phân mạch nhánh: + cắt 1C: + cắt 2C:
Câu 25 :
Cho ankan X có CTPT là C6H14, biết rằng khi cho X tác dụng với clo theo tỉ lệ mol 1:1 thu được 2 sản phẩm thế monoclo. CTCT đúng của X là
Đáp án : A Phương pháp giải :
- Viết đồng phân ankan - Xét các vị trí thế clo của mỗi đồng phân Lời giải chi tiết :
Câu 26 :
Đốt cháy 4,4 gam hỗn hợp CH4, C2H4, C3H6, C4H10 cần a mol O2 thu được b mol CO2 và 7,2 gam H2O. Giá trị a, b lần lượt là
Đáp án : A Phương pháp giải :
+) Bảo toàn khối lượng: mankan = mC + mH Lời giải chi tiết :
nH2O = 0,4 mol => BTNT H: nH = 2.nH2O = 0,8 mol BTKL: mankan = mC + mH <=> mC = 4,4 – 0,8 = 3,6 gam => nC = 0,3 mol BTNT C=> nCO2 = nC = 0,3 mol
Câu 27 :
Để điều chế C2H6 có thể nung hỗn hợp chất X với “vôi tôi – xút”, X là
Đáp án : B Lời giải chi tiết :
2C2H5COOK + 2NaOH \(\xrightarrow{{CaO,{t^o}}}\) 2C2H6 + Na2CO3 + K2CO3
Câu 28 :
Ứng với công thức phân tử C5H10 có bao nhiêu anken ?
Đáp án : C Lời giải chi tiết :
Số đồng phân anken bao gồm đồng phân cấu tạo và đồng phân hình học Các đồng phân của C5H10
2,3. H2C-CH=CH-CH2-CH3 (có đồng phân hình học)
Câu 29 :
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp X gồm CH4, C2H4 thu được 0,15 mol CO2 và 0,2 mol H2O. Giá trị của V là
Đáp án : A Phương pháp giải :
Gọi số mol CH4 và C2H4 là a, b BTNT:
Lời giải chi tiết :
Gọi số mol CH4 và C2H4 là a, b BTNT: V= (0,05+ 0,05). 22,4 = 2,24 lít
Câu 30 :
Số đồng phân cấu tạo (mạch hở) có công thức phân tử C5H8 là
Đáp án : D Phương pháp giải :
Đồng phân cấu tạo mạch hở có công thức phân tử C5H8 có thể là ankadien hoặc ankin. Lời giải chi tiết :
Có tất cả 9 đồng phân mạch hở ứng với CTPT C5H8
Câu 31 :
Gọi tên chất: \(C{H_3} - CH(C{H_3}) - C \equiv C - C{H_2} - C{H_3}\)
Đáp án : D Lời giải chi tiết :
Quy tắc: 1. Mạch chính là mạch cacbon dài nhất chứa nối ba. 2. Đánh số Cacbon từ đầu gần nối ba nhất. \(C{H_3} - CH(C{H_3}) - C \equiv C - C{H_2} - C{H_3}\)có tên gọi là 2-metylhex-3-in hoặc etylisopropylaxetilen
Câu 32 :
Trong phân tử ankin X, hiđro chiếm 12,2% về khối lượng. Có bao nhiêu ankin phù hợp với X?
Đáp án : C Phương pháp giải :
Xem lại lí thuyết ankin Lời giải chi tiết :
Gọi công thức phân tử ankin là CnH2n-2 (n ≥ 2) \(\% {m_H} = \dfrac{{2n - 2}}{{14n - 2}}.100\% = 12,2\% \to n \approx 6\) CTPT của ankin X là C6H10 CTCT:
Câu 33 :
Hỗn hợp X gồm hai anken là chất khí ở điều kiện thường. Hiđrat hóa X thu được hỗn hợp Y gồm bốn ancol (không có ancol bậc III). Anken trong X là
Đáp án : B Lời giải chi tiết :
CH2=CH2 + H2O → CH3-CH2-OH CH2=CH-CH3 + H2O → CH2(OH)-CH2-CH3 hoặc CH3-CH(OH)-CH3 CH2=CH-CH2-CH3 + H2O → CH3-CH(OH)-CH2-CH3 hoặc CH2(OH)-CH2-CH2-CH3 CH3-CH=CH-CH3 + H2O → CH3-CH2-CH(OH)-CH3 => hỗn hợp X gồm propilen và but-1-en thỏa mãn.
Câu 34 :
Hỗn hợp X gồm C2H4 và H2 có tỷ lệ mol 1:1. Cho hỗn hợp X qua Ni, t0 thu được hỗn hợp Y. Cho hỗn hợp Y vào dung dịch brom dư thu được hỗn hợp khí Z. Tỷ khối của Z so với H2 là 11,5. Vậy hiệu suất phản ứng hiđro hóa là
Đáp án : D Phương pháp giải :
C2H4 + H2 → C2H6 Ban đầu 1 1 Phản ứng x x x Cân bằng 1-x 1-x x Hỗn hợp Y: C2H4 dư, H2 dư, C2H6 => hỗn hợp Z: C2H6, H2 dư \({d_{Z/H{ _2}}} = 11,5 \to {M_Z} = 23\) Từ đó tính ra x và hiệu suất phản ứng. Lời giải chi tiết :
C2H4 + H2 → C2H6 Ban đầu 1 1 Phản ứng x x x Cân bằng 1-x 1-x x Hỗn hợp Y: C2H4 dư, H2 dư, C2H6 => hỗn hợp Z: C2H6, H2 dư \(\begin{gathered}{d_{Z/H{ _2}}} = 11,5 \to {M_Z} = 23 \hfill \\\frac{{30x + 2(1 - x)}}{{1 - x + x}} = 23 \to x = 0,75 \hfill \\ H = \frac{{0,75}}{1}.100\% = 75\% \hfill \\ \end{gathered} \)
Câu 35 :
Trùng hợp propen, sản phẩm thu được có cấu tạo là
Đáp án : B Phương pháp giải :
Xem lại lý thuyết phản ứng trùng hợp của anken Lời giải chi tiết :
Câu 36 :
Cho các phương trình hóa học (1) \(C{H_3} - C \equiv CH + {H_2}O\xrightarrow{{H{g^{2 + }},{t^0}}}C{H_3}C{H_2}CHO\) (spc) (2) \(C{H_3} - C \equiv CH + AgN{O_3} + N{H_3}\xrightarrow{{{t^0}}}C{H_3} - C \equiv CAg + N{H_4}N{O_3}\) (3) \(C{H_3} - C \equiv CH + 2{H_2}\xrightarrow{{Ni,{t^0}}}C{H_3}C{H_2}C{H_3}\) (4) \(3C{H_3} - C \equiv CH\xrightarrow{{xt,{t^0},p}}\) Các phương trình hóa học viết sai là
Đáp án : B Phương pháp giải :
Xem lại phản ứng hóa học của ankin
Lời giải chi tiết :
Phản ứng (1) viết sai: CH3-C≡CH + H2O \(\xrightarrow{{H{g^{2 + }},{t^o}}}\) CH3-CO-CH3
Câu 37 :
Dãy nào sau đây chứa các chất làm nhạt màu dung dịch nước brom và thuốc tím?
Đáp án : A Phương pháp giải :
Xem lại phản ứng cộng của ankin Lời giải chi tiết :
Các chất làm nhạt màu dung dịch nước brom và thuốc tím là SO2, C2H2, C2H4
Câu 38 :
Một hiđrocacbon A mạch thẳng có công thức phân tử là C6H6. Khi cho A tác dụng với dung dịch AgNO3/NH3 dư thu được hợp chất hữu cơ B có MB – MA = 214 đvC. Công thức cấu tạo của X có thể là
Đáp án : A Phương pháp giải :
C6H6 → C6H6-xAgx MB – MA = 78 + 107x – 78 = 214 => x Lời giải chi tiết :
A mạch thẳng tạo kết tủa với AgNO3 => A có liên kết ba đầu mạch C6H6 → C6H6-xAgx MB – MA = 78 + 107x – 78 = 214 => x = 2
Câu 39 :
Hiđro hóa hoàn toàn ankin X (xt Pd, PbCO3) thu được anken Y có công thức phân tử là C5H10. Vậy Y không thể là anken nào sau đây?
Đáp án : A Phương pháp giải :
Xem lại lí thuyết phản ứng cộng ankin Lời giải chi tiết :
Y không thể là 2-metylbut-1-en vì khi đó X sẽ có công thức là :
Câu 40 :
Khi brom hóa một ankan chỉ thu được một dẫn xuất monobrom duy nhất có tỉ khối hơi đối với hiđro là 75,5. Tên của ankan đó là:
Đáp án : B Phương pháp giải :
Công thức dẫn xuất monobrom là CnH2n+1Br. Từ khối lượng phân tử của dẫn xuất xác định được giá trị của n. Lời giải chi tiết :
M = 75,5.2 = 151 => \({M_{{C_n}{H_{2n + 1}}Br}}\) = 14n + 81 = 151 => n = 5 => CTPT ankan là C5H12 Do brom hóa ankan chỉ thu được 1 dẫn xuất monobrom duy nhất => CTCT thỏa mãn: C(CH3)4 |














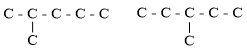
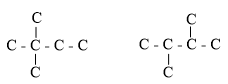
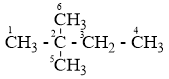
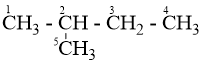
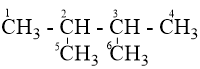
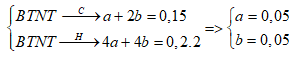





Danh sách bình luận