Đề thi học kì 2 Hóa 11 - Đề số 5Đề bài
Câu 1 :
CTTQ của anđehit no, mạch hở, 2 chức là
Câu 2 :
Trong công nghiệp, HCHO được điều chế từ chất nào sau đây ?
Câu 3 :
Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít khí CO2 (đktc) và x gam H2O. Giá trị của x là :
Câu 4 :
Khi thực hiện phản ứng tách nước đối với ancol X, chỉ thu được 1 anken duy nhất. Oxi hoá hoàn toàn một lượng chất X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O. Có bao nhiêu công thức cấu tạo phù hợp với X?
Câu 5 :
Cho ancol etylic phản ứng với HNO3 thu được hợp chất có công thức:
Câu 6 :
Dầu chuối là este có tên isoamyl axetat, được điều chế từ
Câu 7 :
Cho các chất: CH3CH2CHO (1), CH2=CHCHO (2), (CH3)2CHCHO (3), CH2=CHCH2OH (4). Những chất phản ứng hoàn toàn với lượng dư H2 (Ni, to) thu được cùng một sản phẩm là
Câu 8 :
Tên gọi đúng của hợp chất : (CH3)2CH-C≡CH là
Câu 9 :
Công thức phân tử của ancol không no có 2 liên kết π, mạch hở, 3 chức là
Câu 10 :
Trên một chai rượu có nhãn ghi 25o có nghĩa là
Câu 11 :
Chất nào sau đây không thể là ancol
Câu 12 :
Chất C8H8O2 có mấy đồng phân là axit, chứa vòng benzen:
Câu 13 :
Cho sơ đồ sau: $Axetilen\xrightarrow{+{{H}_{2}},P\text{d},{{t}^{o}}}{{X}_{1}}\xrightarrow{dd\,\,KMn{{O}_{4}}}{{X}_{2}}\xrightarrow{CuO,{{t}^{o}}}$ anđehit X3. CTPT của X3 là
Câu 14 :
Đốt X thu được ${m_{C{O_2}}}:\,\,{m_{{H_2}O}}\,\, = \,\,44\,\,:\,\,9$ . Biết X làm mất màu dung dịch brom. X là :
Câu 15 :
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
Câu 16 :
Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất ?
Câu 17 :
Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với Na dư thu được 2,24 lít khí H2 (đktc). Mặt khác, m gam hỗn hợp X phản ứng vừa đủ với 100 ml dung dịch NaOH 1M. Giá trị của m là
Câu 18 :
Đime hóa 6,72 lít axetilen (nhiệt độ, xúc tác cần thiết) thu được 4,48 lít hỗn hợp X gồm axetilen và vinyl axetilen. Cho toàn bộ X qua dung dịch AgNO3 trong NH3 dư thu được m gam kết tủa. Các thể tích đo ở đktc. Giá trị m là
Câu 19 :
Cho 0,04 mol một hỗn hợp X gồm CH2=CH-COOH, CH3COOH và CH2=CH-CHO phản ứng vừa đủ với dung dịch chứa 6,4 gam brom. Mặt khác, để trung hoà 0,04 mol X cần dùng vừa đủ 40 ml dung dịch NaOH 0,75 M. Khối lượng của CH2=CH-COOH trong X là
Câu 20 :
Cho a gam ankađien X qua dung dịch Br2 dư thấy có 16 gam brom phản ứng. Mặt khác đốt cháy hoàn toàn a gam X cần 7,84 lít O2 (đktc). Công thức của X là
Câu 21 :
Lượng clobenzen thu được khi cho 15,6 gam C6H6 tác dụng hết với Cl2 (xúc tác bột Fe) với hiệu suất phản ứng đạt 80% là :
Câu 22 :
Cho hỗn hợp X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X tác dụng hết với dung dịch brom dư thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là
Câu 23 :
$A{l_4}{C_3} \to X \to Y \to {C_2}{H_6}.$ X, Y lần lượt là:
Câu 24 :
Phản ứng điều chế axit axetic nào sau đây là sai.
Câu 25 :
Hiđro hóa hoàn toàn m gam hỗn hợp X gồm 2 anđehit mạch hở, thu được hỗn hợp Y. Cho Y vào bình đựng Na (dư 25% so với lượng phản ứng), thu được 11,2 lít H2 (đktc) và hỗn hợp rắn Z. Đốt cháy hoàn toàn Z thu được Na2CO3, H2O và 16,5 gam CO2. Mặt khác, cho 0,3 mol X tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được a gam kết tủa. Giá trị của a là
Câu 26 :
Một hỗn hợp X gồm a mol axetilen; 2a mol etilen và 5a mol H2. Cho hỗn hợp X qua Ni nung nóng thu được hỗn hợp Y gồm 4 chất. Đặt k là tỉ khối của hỗn hợp Y so với hỗn hợp X. Hãy cho biết khoảng giá trị của k.
Câu 27 :
A là ancol đơn chức no hở, B là axit cacboxylic no hở đơn chức. Biết MA=MB. Phát biểu đúng là
Câu 28 :
Hỗn hợp X gồm CH4, C2H4, C3H6, C4H6 trong đó CH4 và C4H6 có cùng số mol . Đốt cháy m gam X rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng dung dịch giảm 7,6g. Giá trị của m là :
Câu 29 :
Phản ứng nào sau đây điều chế được CH4 tinh khiết hơn ? \(A{l_4}{C_3} + 12{H_2}O\xrightarrow{{}}4Al{(OH)_3} + 3C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(1)\) \({C_4}{H_{10}}\xrightarrow{{Crackinh}}{C_3}{H_6} \uparrow + C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(2)\) \(C{H_3}COON{a_r} + NaO{H_r}\xrightarrow{{CaO,\,\,{t^o}}}N{a_2}C{O_3} + C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(3)\) \(C{H_2}{(COONa)_2}_{\,\,r} + 2NaO{H_r}\xrightarrow{{CaO,\,\,{t^o}}}2N{a_2}C{O_3} + C{H_4} \uparrow \,\,\,\,\,\,(4)\) \(C + 2{H_2}\xrightarrow{{{t^o}}}C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(5)\)
Câu 30 :
Ứng với công thức phân tử C5H10 có bao nhiêu anken ?
Câu 31 :
Cho các chất: CH2=CH-CH=CH2; CH3-CH2-CH=C(CH3)2; CH3-CH=CH-CH=CH2; CH3-CH=CH2; CH3-CH=CH-COOH. Số chất có đồng phân hình học là :
Câu 32 :
Một hỗn hợp X gồm 2 hiđrocacbon liên tiếp nhau trong dãy đồng đẳng. Đốt cháy hoàn toàn 0,5 mol hỗn hợp X thu được 29,12 lít khí CO2 (đktc) và 23,4 gam H2O. Công thức phân tử và thành phần % khối lượng tương ứng của hai hiđrocacbon là
Câu 33 :
Isopren tham gia phản ứng với dung dịch HBr theo tỷ lệ mol 1:1 tạo ra tối đa bao nhiêu sản phẩm cộng ?
Câu 34 :
Sản phẩm chính của phản ứng nào sau đây có đồng phân hình học?
Câu 35 :
Thực hiện phản ứng để hiđrat hóa ancol etylic thu được anken X. Tên gọi của X là:
Câu 36 :
Hiđrocacbon X có tỷ khối đối với không khí xấp xỉ 3,173. Ở nhiệt độ thường X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4. X là
Câu 37 :
Công thức tổng quát của hiđrocacbon là CnH2n+2-2a. Đối với naphtalen (C10H8), giá trị của n và a lần lượt là
Câu 38 :
Đốt cháy hoàn toàn 0,1mol hỗn hợp hai anđehit là đồng đẳng kế tiếp thu dược 8,064lít CO2 (dktc) và 4,68g H2O. CTCT của 2 anđehit là:
Câu 39 :
Cho các chất : C6H5OH (X) ; C6H5CH2OH (Y) ; HOC6H4OH (Z) ; C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là :
Câu 40 :
Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol, thu được 336 ml khí H2 (đktc). Khối lượng muối natri thu được là:
Lời giải và đáp án
Câu 1 :
CTTQ của anđehit no, mạch hở, 2 chức là
Đáp án : B Lời giải chi tiết :
CTTQ của anđehit no, mạch hở, 2 chức là CnH2n-2O2 (n ≥ 2)
Câu 2 :
Trong công nghiệp, HCHO được điều chế từ chất nào sau đây ?
Đáp án : C Lời giải chi tiết :
Trong công nghiệp, HCHO được điều chế từ CH4 hoặc CH3OH
Câu 3 :
Khi đốt cháy hoàn toàn 7,84 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được 16,8 lít khí CO2 (đktc) và x gam H2O. Giá trị của x là :
Đáp án : D Phương pháp giải :
Áp dụng công thức : nankan = nH2O – nCO2 Lời giải chi tiết :
nankan = 0,35 mol ; nCO2 = 0,75 mol Áp dụng công thức : nankan = nH2O – nCO2 => nH2O = 0,75 + 0,35 = 1,1 mol => mH2O = 1,1.18 = 19,8 gam
Câu 4 :
Khi thực hiện phản ứng tách nước đối với ancol X, chỉ thu được 1 anken duy nhất. Oxi hoá hoàn toàn một lượng chất X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O. Có bao nhiêu công thức cấu tạo phù hợp với X?
Đáp án : D Phương pháp giải :
X bị tách nước tạo 1 anken => X là ancol no, đơn chức và chỉ có 1 hướng tách +) nancol = nH2O – nCO2 +) n =$\frac{{0,25}}{{0,05}}$ = 5 Lời giải chi tiết :
X bị tách nước tạo 1 anken => X là ancol no, đơn chức và chỉ có 1 hướng tách Công thức phân tử của X là CnH2n+1OH ; Có nancol = nH2O – nCO2 = $\frac{{5,4}}{{18}} - \frac{{5,6}}{{22,4}} = {\text{ }}0,05{\text{ }}mol$ Và n = $\frac{{0,25}}{{0,05}}$= 5 . Nên công thức phân tử của X là C5H11OH Công thức cấu tạo của X là CH3 – CH2 – CH2 – CH2 – CH2OH ; CH3 – CH(CH3) – CH2 – CH2OH CH3 – CH2 – CH(CH3) – CH2OH .
Câu 5 :
Cho ancol etylic phản ứng với HNO3 thu được hợp chất có công thức:
Đáp án : B Phương pháp giải :
Xem lại lí thuyết phản ứng của ancol với axit Lời giải chi tiết :
C2H5OH + HNO3 →C2H5ONO2 + H2O
Câu 6 :
Dầu chuối là este có tên isoamyl axetat, được điều chế từ
Đáp án : D Phương pháp giải :
Xem lại lí thuyết phản ứng este hóa Lời giải chi tiết :
Dầu chuối có CTCT: CH3COOCH2-CH2-CH(CH3)2 => được điều chế từ CH3COOH và (CH3)2CH-CH2-CH2OH.
Câu 7 :
Cho các chất: CH3CH2CHO (1), CH2=CHCHO (2), (CH3)2CHCHO (3), CH2=CHCH2OH (4). Những chất phản ứng hoàn toàn với lượng dư H2 (Ni, to) thu được cùng một sản phẩm là
Đáp án : B Phương pháp giải :
Xem lại lí thuyết phản ứng cộng của anđehit Lời giải chi tiết :
Những chất phản ứng hoàn toàn với lượng dư H2 (Ni, to) thu được cùng một sản phẩm là CH3CH2CHO (1), CH2=CHCHO (2), CH2=CHCH2OH (4).
Câu 8 :
Tên gọi đúng của hợp chất : (CH3)2CH-C≡CH là
Đáp án : B Lời giải chi tiết :
(CH3)2CH-C≡CH : 3-metylbut-1-in. Chú ý
Đánh số C ưu tiên vị trí liên kết 3
Câu 9 :
Công thức phân tử của ancol không no có 2 liên kết π, mạch hở, 3 chức là
Đáp án : A Lời giải chi tiết :
ancol không no có 2 liên kết π, mạch hở => độ không no k = 2 => hụt 4H ancol có 3 chức => có 3O trong phân tử CnH2n-2O3
Câu 10 :
Trên một chai rượu có nhãn ghi 25o có nghĩa là
Đáp án : D Lời giải chi tiết :
Trên một chai rượu có nhãn ghi 25o có nghĩa là cứ 1 lít dung dịch thì có 0,25 lít ancol nguyên chất.
Câu 11 :
Chất nào sau đây không thể là ancol
Đáp án : B Lời giải chi tiết :
Chất không thể là ancol là C2H4O vì độ không no k = (2.2 + 2 – 4)/2 = 1 => giữa 2C có nối đôi mà nhóm OH không đính được vào C không no
Câu 12 :
Chất C8H8O2 có mấy đồng phân là axit, chứa vòng benzen:
Đáp án : A Phương pháp giải :
Vẽ vòng benzen sau đó thay đổi vị trí các nhóm thế Lời giải chi tiết :
Các đồng phân là 1. C6H5CH2COOH 2. o-CH3C6H4COOH 3. p- CH3C6H4COOH 4. m- CH3C6H4COOH
Câu 13 :
Cho sơ đồ sau: $Axetilen\xrightarrow{+{{H}_{2}},P\text{d},{{t}^{o}}}{{X}_{1}}\xrightarrow{dd\,\,KMn{{O}_{4}}}{{X}_{2}}\xrightarrow{CuO,{{t}^{o}}}$ anđehit X3. CTPT của X3 là
Đáp án : C Phương pháp giải :
Xem lại lí thuyết điều chế và ứng dụng của anđehit Lời giải chi tiết :
$CH\equiv CH\xrightarrow{+{{H}_{2}},P\text{d},{{t}^{o}}}C{{H}_{2}}=C{{H}_{2}}\xrightarrow{dd\,\,KMn{{O}_{4}}}C{{H}_{2}}OH-C{{H}_{2}}OH\xrightarrow{CuO,{{t}^{o}}}OHC-CHO$ => CTPT của X3 là C2H2O2.
Câu 14 :
Đốt X thu được ${m_{C{O_2}}}:\,\,{m_{{H_2}O}}\,\, = \,\,44\,\,:\,\,9$ . Biết X làm mất màu dung dịch brom. X là :
Đáp án : D Phương pháp giải :
${m_{C{O_2}}}:{\text{ }}{m_{{H_2}O}} = {\text{ }}44{\text{ }}:{\text{ }}9{\text{ }} = > {\text{ }}{n_{C{O_2}}}:{n_{{H_2}O}} = \frac{{44}}{{44}}:\frac{9}{{18}} $ Lời giải chi tiết :
${m_{C{O_2}}}:{\text{ }}{m_{{H_2}O}} = {\text{ }}44{\text{ }}:{\text{ }}9{\text{ }} = > {\text{ }}{n_{C{O_2}}}:{n_{{H_2}O}} = \frac{{44}}{{44}}:\frac{9}{{18}} = 1:0,5$ => nC : nH = 1 : 1 => CTĐGN của X là CH Vì X làm mất màu dung dịch brom => X có liên kết đôi hoặc liên kết 3
Câu 15 :
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
Đáp án : B Lời giải chi tiết :
- Ở điều kiện thường, các axit cacboxylic đều là những chất lỏng hoặc rắn. - HCHO là những chất khí tan tốt trong nước - CH3OH và C2H5HO là những chất lỏng
Câu 16 :
Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất ?
Đáp án : C Phương pháp giải :
Các ankan có nhiệt độ nóng chảy và nhiệt độ sôi tăng dần theo khối lượng phân tử. Lời giải chi tiết :
Chất có nhiệt độ sôi thấp nhất là metan vì có khối lượng phân tử nhỏ nhất.
Câu 17 :
Cho m gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với Na dư thu được 2,24 lít khí H2 (đktc). Mặt khác, m gam hỗn hợp X phản ứng vừa đủ với 100 ml dung dịch NaOH 1M. Giá trị của m là
Đáp án : C Phương pháp giải :
${n_{{C_6}{H_5}OH}}\, + \,{n_{{C_2}{H_5}OH}}\, = \,2{n_{{H_2}}}$ C6H5OH + NaOH $ \to $ C6H5ONa + H2O Từ số mol NaOH => số mol C6H5OH Lời giải chi tiết :
${n_{{H_2}}} = \frac{{2,24}}{{22,4}} = 0,1\,mol$, nNaOH = 1.0,1 = 0,1 mol C6H5OH + Na $ \to $ C6H5ONa + $\frac{1}{2}$ H2 C2H5OH + Na $ \to $ C2H5ONa + $\frac{1}{2}$ H2 → ${n_{{C_6}{H_5}OH}}\, + \,{n_{{C_2}{H_5}OH}}\, = \,2{n_{{H_2}}} = \,2.0,1 = 0,2\,mol$ C6H5OH + NaOH $ \to $ C6H5ONa + H2O 0,1 mol ← 0,1 mol → ${n_{{C_2}{H_5}OH}} = \,0,2 - {n_{{C_6}{H_5}OH}}\, = \,0,2 - 0,1 = 0,1\,mol$ → $m = {m_{{C_6}{H_5}OH}} + {m_{{C_2}{H_5}OH}} = 0,1.94 + 0,1.46 = 14\,\,gam$
Câu 18 :
Đime hóa 6,72 lít axetilen (nhiệt độ, xúc tác cần thiết) thu được 4,48 lít hỗn hợp X gồm axetilen và vinyl axetilen. Cho toàn bộ X qua dung dịch AgNO3 trong NH3 dư thu được m gam kết tủa. Các thể tích đo ở đktc. Giá trị m là
Đáp án : B Phương pháp giải :
+) Đặt số mol của C4H4 trong hỗn hợp X là x mol +) Từ PT: 2CH ≡ CH → CH ≡ C – CH = CH2 => tính số mol của C2H2 phản ứng => số mol C2H2 dư Lời giải chi tiết :
${n_{{C_2}{H_2}}}\,\, = \,\,\frac{{6,72}}{{22,4}}\,\, = \,\,0,3\,\,mol$ Đặt số mol của C4H4 trong hỗn hợp X là x mol 2CH ≡ CH → CH ≡ C – CH = CH2 2x ← x $\begin{array}{l}{n_{{C_2}{H_2}(X)}} = 0,3 - 2{\rm{x}}mol\\{n_X}= \frac{{4,48}}{{22,4}} = 0,2\,mol \to {n_{{C_2}{H_2}(X)}} + {n_{{C_4}{H_4}(X)}} = 0,2 \to 0,3 - 2{\rm{x}}+ x = 0,2 \to x =0,1\\ \to {n_{{C_2}{H_2}(X)}}= 0,3 - 2.0,1= 0,1\,mol;\,{n_{{C_4}{H_4}(X)}} = 0,1\,mol\end{array}$ CH ≡ CH → CAg ≡ CAg 0,1 → 0,1 CH ≡ C – CH = CH2 → CAg ≡ C – CH = CH2 0,1 → 0,1 m↓ = 0,1.240 + 0,1.159 = 39,9 gam Chú ý
+ Tính khối lượng của mỗi kết tủa Ag2C2 => chọn nhầm A + Tính khối lượng của mỗi kết tủa CAg ≡ C – CH = CH2 => chọn nhầm D
Câu 19 :
Cho 0,04 mol một hỗn hợp X gồm CH2=CH-COOH, CH3COOH và CH2=CH-CHO phản ứng vừa đủ với dung dịch chứa 6,4 gam brom. Mặt khác, để trung hoà 0,04 mol X cần dùng vừa đủ 40 ml dung dịch NaOH 0,75 M. Khối lượng của CH2=CH-COOH trong X là
Đáp án : B Phương pháp giải :
+) X phản ứng vừa đủ với 0,04 mol Br2 => nBr2 = nCH2=CH-COOH + 2.nCH2=CH-CHO +) nNaOH = nCH2=CH-COOH + nCH3COOH Lời giải chi tiết :
Gọi n CH2=CH-COOH = x mol; n CH3COOH = y mol và n CH2=CH-CHO = z mol => x + y + z = 0,04 (1) X phản ứng vừa đủ với 0,04 mol Br2 => nBr2 = nCH2=CH-COOH + 2.nCH2=CH-CHO => x + 2z = 0,04 (2) nNaOH = nCH2=CH-COOH + nCH3COOH => x + y = 0,03 mol (3) Từ (1), (2) và (3) => x = 0,02; y = 0,01; z = 0,01 => m CH2=CH-COOH = 0,02.72 = 1,44 gam
Câu 20 :
Cho a gam ankađien X qua dung dịch Br2 dư thấy có 16 gam brom phản ứng. Mặt khác đốt cháy hoàn toàn a gam X cần 7,84 lít O2 (đktc). Công thức của X là
Đáp án : B Phương pháp giải :
+) Ankađien X phản ứng với Br2 dư => phản ứng theo tỉ lệ 1:2 => nX Gọi công thức phân tử của X là CnH2n-2 +) Từ số mol X và số mol O2 => n Lời giải chi tiết :
nBr2 = 0,1 mol; nO2 = 0,35 mol Ankađien X phản ứng với Br2 dư => phản ứng theo tỉ lệ 1:2 => nX = 0,5.nBr2 = 0,05 mol Gọi công thức phân tử của X là CnH2n-2 CnH2n-2 + (3n – 1)/2 O2 → CO2 + (n – 1)H2O 0,05 0,35 mol => 0,05.(3n – 1)/2 = 0,35 => n = 5 Vậy CTPT của X là C5H8
Câu 21 :
Lượng clobenzen thu được khi cho 15,6 gam C6H6 tác dụng hết với Cl2 (xúc tác bột Fe) với hiệu suất phản ứng đạt 80% là :
Đáp án : C Phương pháp giải :
Tính theo PT: C6H6 + Cl2 $\xrightarrow{{{t^o},\,\,Fe}}$ C6H5Cl + HCl (1)
Lời giải chi tiết :
${n_{{C_6}{H_6}\,(pư)}} = \frac{{15,6}}{{78}}.80\% = 0,16\,\,mol.$ Phương trình phản ứng : C6H6 + Cl2 $\xrightarrow{{{t^o},\,\,Fe}}$ C6H5Cl + HCl (1) mol: 0,16 0,16 Vậy khối lượng clobenzen thu được là : 0,16.112,5= 18 gam.
Câu 22 :
Cho hỗn hợp X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X tác dụng hết với dung dịch brom dư thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là
Đáp án : D Phương pháp giải :
Trong 8,6g X chứa a mol C2H4; b mol C2H2; c mol CH4 +) mhh X = PT(1) +) nBr2 phản ứng = nπ trong X = nC2H4 + 2.nC2H2 => PT(2) +) nC2Ag2 = nC2H2 => %nC2H2 trong X => trong 8,6 gam X % số mol C2H2 cũng là 25% => PT(3) Lời giải chi tiết :
Trong 8,6g X chứa a mol C2H4; b mol C2H2; c mol CH4 mhh X = 28a + 26b + 16c = 8,6 (1) nBr2 phản ứng = nπ trong X = nC2H4 + 2.nC2H2 => a + 2b = 0,3 (2) C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3 nC2Ag2 = 0,15 (mol) => nC2H2 = 0,15 (mol) => %nC2H2 trong X = 0,15/0,6 = 25% => trong 8,6 gam X % số mol C2H2 cũng là 25% => b = 25%.(a + b + c) (3) Từ (1), (2) và (3) => a = 0,1; b = 0,1; c = 0,2 ==>%n CH4 trong X = 50%
Câu 23 :
$A{l_4}{C_3} \to X \to Y \to {C_2}{H_6}.$ X, Y lần lượt là:
Đáp án : D Phương pháp giải :
Xem lại phương pháp điều chế và ứng dụng của metan Lời giải chi tiết :
$A{l_4}{C_3} \to C{H_4} \to {C_2}{H_2} \to {C_2}{H_6}$ $A{l_4}{C_3} \to C{H_4} \to {C}{H_3}{Cl} \to {C_2}{H_6}$
Câu 24 :
Phản ứng điều chế axit axetic nào sau đây là sai.
Đáp án : D Lời giải chi tiết :
Phương pháp điều chế không đúng là: 2C2H6 + 3O2 $\xrightarrow{xt,\text{ }{{\text{t}}^{\text{o}}}}$ 2CH3COOH + 2H2O
Câu 25 :
Hiđro hóa hoàn toàn m gam hỗn hợp X gồm 2 anđehit mạch hở, thu được hỗn hợp Y. Cho Y vào bình đựng Na (dư 25% so với lượng phản ứng), thu được 11,2 lít H2 (đktc) và hỗn hợp rắn Z. Đốt cháy hoàn toàn Z thu được Na2CO3, H2O và 16,5 gam CO2. Mặt khác, cho 0,3 mol X tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được a gam kết tủa. Giá trị của a là
Đáp án : D Phương pháp giải :
+) Từ nH2 => nNa phản ứng => nNa dư +) ∑nNa ban đầu = nNa phản ứng + nNa dư +) Bảo toàn Na => ${n_{N{a_2}C{O_3}}} = \dfrac{{{n_{Na\,ban{\text{đ}}ầu}}}}{2}$ +) Bảo toàn C => ${n_C} = {n_{N{a_2}C{O_3}}} + {n_{C{O_2}}}$ Y có dạng: R(OH)a ($\dfrac{1}{a}$ mol) => số C trong Y +) Biện các ancol trong Y => anđehit trong Z Lời giải chi tiết :
nH2 = 0,5 mol => nNa phản ứng = 1 mol => nNa dư = 0,25 mol => ∑nNa ban đầu = 1 + 0,25 = 1,25 mol Bảo toàn Na => ${n_{N{a_2}C{O_3}}} = \dfrac{{{n_{Na\,ban{\text{đ}}ầu}}}}{2} = 0,625{\text{ }}mol$ Bảo toàn C => ${n_C} = {n_{N{a_2}C{O_3}}} + {n_{C{O_2}}} = 1$ Y có dạng: R(OH)a (($\dfrac{1}{a}$ mol) => số C $ = \dfrac{{{n_C}}}{{{n_Y}}} = \dfrac{1}{{\dfrac{1}{a}}} = a$ Vậy Y chứa các ancol có số C = số mol OH Mặt khác, Y tạo ra từ anđehit nên các ancol đều bậc 1 => CH3OH và C2H4(OH)2 => X gồm HCHO và (CHO)2 => nAg = 4.nX = 1,2 => mAg = 129,6
Câu 26 :
Một hỗn hợp X gồm a mol axetilen; 2a mol etilen và 5a mol H2. Cho hỗn hợp X qua Ni nung nóng thu được hỗn hợp Y gồm 4 chất. Đặt k là tỉ khối của hỗn hợp Y so với hỗn hợp X. Hãy cho biết khoảng giá trị của k.
Đáp án : D Phương pháp giải :
4 chất ở đây là ankan, anken, ankin và H2 nên số mol Y < 8a Nếu Y có 2 chất (ankan và H2) thì nY = 4a +) Từ mX = mY => xét khoảng giá trị của l Lời giải chi tiết :
4 chất ở đây là ankan, anken, ankin và H2 nên số mol Y < 8a Nếu Y có 2 chất (ankan và H2) thì nY = 4a Vậy ta có: \({m_X} = {m_Y} \to \frac{{{n_X}}}{{{n_Y}}} = \frac{{{M_Y}}}{{{M_X}}} \to \frac{{8{\rm{a}}}}{{8{\rm{a}}}} = 1 < \frac{{{M_Y}}}{{{M_X}}} < \frac{{8{\rm{a}}}}{{4{\rm{a}}}} = 2\) => 1 < k < 2 hay 2 > k > 1
Câu 27 :
A là ancol đơn chức no hở, B là axit cacboxylic no hở đơn chức. Biết MA=MB. Phát biểu đúng là
Đáp án : C Phương pháp giải :
+) Gọi công thức chung của A là CnH2n+2O và B là CmH2mO2 + Từ MA= MB tìm quan hệ giữa n và m => Nhận định đúng Lời giải chi tiết :
Gọi công thức của A là CnH2n+2O B là CmH2mO2 Vì MA= MB nên 14n + 18 = 14m + 32 → 14n = 14m + 14→ n = m + 1 A sai vì m và n khác nhau B sai vì m ≠ n C đúng D sai vì m = n - 1
Câu 28 :
Hỗn hợp X gồm CH4, C2H4, C3H6, C4H6 trong đó CH4 và C4H6 có cùng số mol . Đốt cháy m gam X rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng dung dịch giảm 7,6g. Giá trị của m là :
Đáp án : B Phương pháp giải :
Qui đổi hỗn hợp thành C2H4 và C3H6 Lời giải chi tiết :
Do CH4 và C4H6 có cùng số mol nên qui đổi hỗn hợp thành C2H4 và C3H6 Khi đốt cháy nCO2 = nH2O = a mol BTNT C: nCO2 = nCaCO3 Mặt khác mCO2 + mH2O = mCaCO3 – 7,6 => 44a+18a= 100a – 7,6 <=> a = 0,2 mol mX = mC +mH = 12.nCO2 + 1. 2nH2O= 2,8 gam
Câu 29 :
Phản ứng nào sau đây điều chế được CH4 tinh khiết hơn ? \(A{l_4}{C_3} + 12{H_2}O\xrightarrow{{}}4Al{(OH)_3} + 3C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(1)\) \({C_4}{H_{10}}\xrightarrow{{Crackinh}}{C_3}{H_6} \uparrow + C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(2)\) \(C{H_3}COON{a_r} + NaO{H_r}\xrightarrow{{CaO,\,\,{t^o}}}N{a_2}C{O_3} + C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(3)\) \(C{H_2}{(COONa)_2}_{\,\,r} + 2NaO{H_r}\xrightarrow{{CaO,\,\,{t^o}}}2N{a_2}C{O_3} + C{H_4} \uparrow \,\,\,\,\,\,(4)\) \(C + 2{H_2}\xrightarrow{{{t^o}}}C{H_4} \uparrow \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(5)\)
Đáp án : C Lời giải chi tiết :
Phản ứng điều chế được CH4 tinh khiết hơn là (1)(3)(4)
Câu 30 :
Ứng với công thức phân tử C5H10 có bao nhiêu anken ?
Đáp án : C Lời giải chi tiết :
Số đồng phân anken bao gồm đồng phân cấu tạo và đồng phân hình học Các đồng phân của C5H10
2,3. H2C-CH=CH-CH2-CH3 (có đồng phân hình học)
Câu 31 :
Cho các chất: CH2=CH-CH=CH2; CH3-CH2-CH=C(CH3)2; CH3-CH=CH-CH=CH2; CH3-CH=CH2; CH3-CH=CH-COOH. Số chất có đồng phân hình học là :
Đáp án : C Lời giải chi tiết :
Những chất có đồng phân là CH3-CH=CH-CH=CH2; CH3-CH=CH-COOH
Câu 32 :
Một hỗn hợp X gồm 2 hiđrocacbon liên tiếp nhau trong dãy đồng đẳng. Đốt cháy hoàn toàn 0,5 mol hỗn hợp X thu được 29,12 lít khí CO2 (đktc) và 23,4 gam H2O. Công thức phân tử và thành phần % khối lượng tương ứng của hai hiđrocacbon là
Đáp án : C Phương pháp giải :
+) nCO2 = nH2O = 1,3 mol => Gọi công thức của 2 hiđrocacbon là: \({C_{\overline n }}{H_{2\overline n }}\) +) \(\overline n = \dfrac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \dfrac{{1,3}}{{0,5}} = 2,6\) +) Gọi số mol C2H4 và C3H6 là a, b (mol) +) Ta có: Lời giải chi tiết :
nCO2 = nH2O = 1,3 mol => Gọi công thức của 2 hiđrocacbon là: \({C_{\overline n }}{H_{2\overline n }}\) \(\overline n = \dfrac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \dfrac{{1,3}}{{0,5}} = 2,6\)=> CTPT của 2 chất là C2H4 và C3H6 Gọi số mol C2H4 và C3H6 là a, b (mol) Ta có:
Câu 33 :
Isopren tham gia phản ứng với dung dịch HBr theo tỷ lệ mol 1:1 tạo ra tối đa bao nhiêu sản phẩm cộng ?
Đáp án : C Lời giải chi tiết :
\({H_2}C = C\left( {C{H_3}} \right) - CH = C{H_2} + HBr \to \left\{ \begin{array}{l}C{H_3} - CBr(C{H_3}) - CH = C{H_2}\\C{H_2}Br - CH(C{H_3}) - CH = C{H_2}\\C{H_2} = C(C{H_3}) - C{H_2} - C{H_2}Br\\C{H_2} = C\left( {C{H_3}} \right) - CHBr - C{H_3}\\C{H_3} - C\left( {C{H_3}} \right) = CH - C{H_2}Br\\C{H_2}Br - C(C{H_3}) = CH - C{H_3}(hình học)\end{array} \right.\) Có 7 sản phẩm cộng
Câu 34 :
Sản phẩm chính của phản ứng nào sau đây có đồng phân hình học?
Đáp án : C Lời giải chi tiết :
CH2=CHCl; CH2=CCl-CH3 không có đphh vì a và b giống nhau ( đều là H) CH3CH2CH2CH3 không có liên kết đôi => không có đphh
Câu 35 :
Thực hiện phản ứng để hiđrat hóa ancol etylic thu được anken X. Tên gọi của X là:
Đáp án : D Lời giải chi tiết :
H3C-CH2-OH → CH2=CH2 + H2O Sản phẩm của phản ứng đề hidrat hóa ancol etylic là Etilen.
Câu 36 :
Hiđrocacbon X có tỷ khối đối với không khí xấp xỉ 3,173. Ở nhiệt độ thường X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4. X là
Đáp án : C Phương pháp giải :
dX/kk= 3,173=> MX = 29. 3,173 = 92 (C7H8) Biện luận để tìm chất X Lời giải chi tiết :
dX/kk= 3,173=> MX = 29. 3,173 = 92 (C7H8) Do nhiệt độ thường X không làm mất màu nước brom. Khi đun nóng, X làm mất màu dung dịch KMnO4 nên X là Toluen
Câu 37 :
Công thức tổng quát của hiđrocacbon là CnH2n+2-2a. Đối với naphtalen (C10H8), giá trị của n và a lần lượt là
Đáp án : C Phương pháp giải :
lập phương trình cho 2 ẩn n và a. Lời giải chi tiết :
\(\left\{ \begin{array}{l}n = 10\\2n + 2 - 2a = 8\end{array} \right. \to \left\{ \begin{array}{l}n = 10\\a = 7\end{array} \right.\)
Câu 38 :
Đốt cháy hoàn toàn 0,1mol hỗn hợp hai anđehit là đồng đẳng kế tiếp thu dược 8,064lít CO2 (dktc) và 4,68g H2O. CTCT của 2 anđehit là:
Đáp án : C Phương pháp giải :
Phương pháp nhanh nhất là loại trừ đáp án. Từ số mol CO2 > số mol H2O suy ra anđehit không no hoặc anđehit 2 chức. Từ số mol CO2, số mol H2O và số mol của hỗn hợp suy ra số nguyên tử C và H trung bình. Từ đó tìm ra công thức phù hợp. Lời giải chi tiết :
nCO2=0,36mol, nH2O=0,26mol. nCO2>nH2O suy ra X,Y là anđehit không no có 1 liên kết đôi hoặc anđehit đa chức. \(n\overline C = \frac{{0,36}}{{0,1}} = 3,6{\text{ n}}\overline H = \frac{{0,26.2}}{{0,1}} = 5,2\) suy ra C2H3CHO, C3H5CHO thỏa mãn
Câu 39 :
Cho các chất : C6H5OH (X) ; C6H5CH2OH (Y) ; HOC6H4OH (Z) ; C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là :
Đáp án : B Phương pháp giải :
Ghi nhớ: Đồng đẳng là các chất hơn kém nhau 1 hay nhiều nhóm –CH2 trong phân tử và có tính chất hóa học tương tự nhau. Lời giải chi tiết :
C6H5CH2OH (Y); C6H5CH2CH2OH (T) cùng thuộc dãy đồng đẳng của ancol thơm Chú ý
C6H5OH là phenol chứ không phải ancol thơm, nó kém C6H5CH2OH 1 nhóm -CH2 nhưng lại có tính chất hóa học khác hoàn toàn so với C6H5CH2OH
Câu 40 :
Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol, thu được 336 ml khí H2 (đktc). Khối lượng muối natri thu được là:
Đáp án : C Phương pháp giải :
Dựa vào định luật bảo toàn khối lượng để xác định khối lượng muối natri thu được. Lời giải chi tiết :
Đặt công thức chung của 3 ancol là R(OH)x R(OH)x + x Na → R(ONa)x + x/2 H2 Theo PTHH: nNa = 2.nH2 = 2. 0,336 : 22,4 = 0,03 mol Áp dụng định luật bảo toàn khối lượng ta có: mmuối natri = mancol + mNa – mH2 = 1,24 + 0,03.23 – 0,015.2 = 1,9 gam |














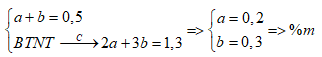
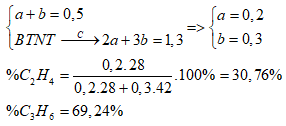





Danh sách bình luận