Bài 4. Ôn tập chương 1 trang 26, 27 Hóa 10 Kết nối tri thứcSố proton, neutron và electron của lần lượt là Nguyên tử của nguyên tố nào sau đây có 3 electron thuộc lớp ngoài cùng Nguyên tử của nguyên tố potassium có 19 electron. Ở trạng thái cơ bản, potassium có số orbital chứa electron là Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
CH tr 27 1
Phương pháp giải:
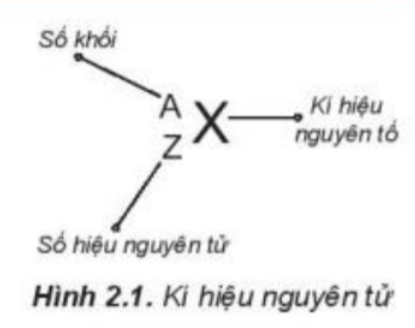
- Kí hiệu một nguyên tử cho biết: + Kí hiệu của nguyên tố đó + Số hiệu nguyên tử = số proton = số electron + Số neutron = số khối – số proton Lời giải chi tiết: Nguyên tử \({}_{19}^{39}K\)cho biết: + Số hiệu nguyên tử = số proton = số electron = 19 + Số khối = 39 => Số neutron = 39 – 19 = 20 => Số proton, neutron và electron của \({}_{19}^{39}K\)lần lượt là 19, 20, 19 CH tr 27 2
Phương pháp giải: Bước 1: Số hiệu nguyên tử = số electron của nguyên tử đó Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng: 1s 2s 2p 3s 3p 4s 3d… Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng Lời giải chi tiết: \({}_{11}^{23}Na\) có Z = 11 => Có 11 electron: 1s22s22p63s1 => Có 1 electron ở lớp ngoài cùng (lớp 3) \({}_7^{14}N\) có Z = 7 => Có 7 electron: 1s22s22p3 => Có 5 electron ở lớp ngoài cùng (lớp 2) \({}_{13}^{27}Al\) có Z = 13 => Có 13 electron: 1s22s22p63s23p1 => Có 3 electron ở lớp ngoài cùng (lớp 3) \({}_6^{12}C\) có Z = 6 => Có 6 electron: 1s22s22p2 => Có 4 electron ở lớp ngoài cùng (lớp 2) => \({}_{13}^{27}Al\) có 3 electron thuộc lớp ngoài cùng Đáp án C CH tr 27 3
Phương pháp giải: Bước 1: Viết cấu hình electron của potassium có 19 electron với thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng: 1s 2s 2p 3s 3p 4s 3d… Bước 2: Viết cấu hình orbital chứa electron => Số orbital chứa electron Lời giải chi tiết: Nguyên tử potassium có 19 electron => Cấu hình electron: 1s22s22p63s23p64s1 => Có 10 orbital chứa electron Đáp án D CH tr 27 4
Phương pháp giải: - Viết cấu hình electron của sodium có 11 electron với thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng: 1s 2s 2p 3s 3p 4s 3d… - Lưu ý: Điền đủ electron vào mức năng lượng thấp rồi mới đến năng lượng cao (s có 2, p có 6, d có 10, f có 14) Lời giải chi tiết: Nguyên tử sodium có 11 electron => Cấu hình electron: 1s22s22p63s1 Đáp án C CH tr 27 5
Phương pháp giải: - Trong nguyên tử + Hạt mang điện là hạt proton và electron + Hạt không mang điện là hạt neutron + Số proton = Số electron B1: Xác định số proton, neutron và electron trong nguyên tử X B2: Dựa vào số proton trong nguyên tử X => X là nguyên tố nào Lời giải chi tiết: - Gọi số hạt proton, electron và neutron trong nguyên tử X lần lượt là p, e, n - Nguyên tử X có tổng số hạt proton, neutron và electron là 58: => p + e + n = 58 (1) - Số hạt mang điện nhiều hơn số hạt không mang điện là 18: => p + e – n = 18 (2) - Mà p = e (3) - Từ (1), (2), (3) => p = e = 19 và n = 20 Vậy X là Kali CH tr 27 6
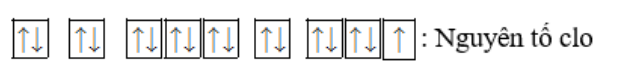
Phương pháp giải: - Trong nguyên tử, các e được sắp xếp thành từng lớp, các lớp được sắp xếp từ gần hạt nhân ra ngoài. Các e có năng lượng gần bằng nhau được sắp xếp trên cùng 1 lớp - Electron độc thân là electron đứng một mình trong orbital nguyên tử mà không hình thành cặp electron Lời giải chi tiết: - Nguyên tố chlorine có Z = 17 => Có 17 electron - Cấu hình e: 1s22s22p63s23p5 - Biểu diễn cấu hình chlorine theo ô orbital: - Nguyên tố Chlorine có: + Số lớp electron: 3 + Số electron thuộc lớp ngoài cùng: 7 + Số electron độc thân: 1 CH tr 27 7
Phương pháp giải: - Nguyên tử khối trung bình của một nguyên tố hóa học ghi trong bảng tuần hoàn là nguyên tử khối trung bình của các đồng vị trong tự nhiên. - Nguyên tử khối trung bình: M = aA+bB+cC+dD+… /100 Trong đó: A, B, C, D… là số khối của các đồng vị a, b, c, d… là phần trăm của các đồng vị tương ứng Lời giải chi tiết: Gọi số khối đồng vị còn lại là x. Ta có: (50.0,25 + 99,75.x)/100 = 50.9975 => x = 51 Vậy số khối đồng vị còn lại của vanadi là 51 CH tr 27 8
Phương pháp giải: a) Số electron của nguyên tử bằng tổng số electron trên các phân lớp s, p, d, f có trong cấu hình electron. b) Số hiệu nguyên tử (Z) hay còn gọi là số proton => Số hiệu nguyên tử = số electron. c) Những e ở lớp trong liên kết với hạt nhân bền chặt hơn những e ở lớp ngoài. Năng lượng của e lớp trong thấp hơn năng lượng e ở lớp ngoài. d) - Lớp electron được đánh số từ 1 đến 7 hoặc kí hiệu tương ứng là K, L, M, N, O, P, Q. - Phân lớp electron gồm 4 loại kí hiệu là s, p, d, f. e) Nguyên tố có: + 1,2,3 e lớp ngoài cùng là kim loại (trừ H, He) + 5,6,7 e lớp ngoài cùng là phi kim. + 8 e lớp ngoài cùng là khí hiếm (trừ He có 2e lớp ngoài cùng nhưng vẫn là khí hiếm). + 4 e ngoài cùng ở chu kì 2,3 là phi kim, còn ở các chu kì khác kim loại. Lời giải chi tiết: a) - Tổng số e trên các phân lớp của nguyên tử X là 19 => Nguyên tử X có 19 e - Tổng số e trên các phân lớp của nguyên tử Y là 16 => Nguyên tử X có 16 e b) - Nguyên tử X có 19 e => Nguyên tử X có số hiệu nguyên tử ZX = 19 - Nguyên tử Y có 16 e => Nguyên tử Y có số hiệu nguyên tử ZY = 16 c) - Trong nguyên tử X lớp electron ở mức năng lượng cao nhất là lớp N (n=4) - Trong nguyên tử Y lớp electron ở mức năng lượng cao nhất là lớp M (n=3) d) - Nguyên tử X có: + 4 lớp electron (n = 1, 2, 3, 4) + 6 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p, 4s) - Nguyên tử Y có: + 3 lớp electron (n= 1, 2, 3) + 5 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p) e) - Nguyên tử X có 1 e lớp ngoài cùng (4s1) => X là nguyên tố kim loại. - Nguyên tử Y có 6 e lớp ngoài cùng (3s23p4) => Y là nguyên tố phi kim. CH tr 27 9
Phương pháp giải: Ta có cấu hình electron kết thúc => cấu hình electron nguyên tử => số electron trong nguyên tử. Dựa vào cấu hình electron => số e lớp ngoài cùng => tính kim loại/phi kim. Lời giải chi tiết: - Nguyên tử nguyên tố X có e cuối cùng điền vào phân lớp 3p1 - Nguyên tử nguyên tố Y có e cuối cùng điền vào phân lớp 3p3 CH tr 27 10
Phương pháp giải: Trong nguyên tử : proton và electron mang điện, neutron không mang điện. Tổng số hạt = số proton + số electron + số neutron = 2Z + N (do số proton = số electron) Số khối A = số proton + số neutron = Z + N Lời giải chi tiết: Ta có Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49: => 2Z + N = 49 (1) Lại có, số hạt không mang điện bằng 53,125% số hạt mang điện: =>N = 2Z x 53,125% = 1716Z <=>17Z – 16N = 0 (2) Từ (1) & (2) ta có: 2Z + N = 49 17Z – 16N = 0 => Z=16 N =17 Vậy nguyên tử nguyên tố X có : điện tích hạt nhân là 16+, 16 proton, 16 electron, 17 neutron và có số khối là 33.
|





















Danh sách bình luận