Đề thi giữa học kì 1 KHTN 7 Chân trời sáng tạo - Đề số 7Tải về Câu 1: Có những hạt nào được tìm thấy trong hạt nhân của nguyên tử? A. Các hạt mang điện tích âm (electron). Tổng hợp đề thi học kì 2 lớp 7 tất cả các môn - Chân trời sáng tạo Toán - Văn - Anh - Khoa học tự nhiên... Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Đề thi I. Trắc nghiệm Câu 1: Có những hạt nào được tìm thấy trong hạt nhân của nguyên tử? A. Các hạt mang điện tích âm (electron). B. Các hạt neutron và hạt proton. C. Các hạt neutron không mang điện. D. Hạt nhân nguyên tử không chứa hạt nào bên trong. Câu 2: Khối lượng nguyên tử của carbon là A. 16 amu. B. 12 amu. C. 6 amu. D. 24 amu. Câu 3: Số hiệu nguyên tử của một nguyên tố là A. số proton trong nguyên tử. B. số neutron trong nguyên tử. C. số electron trong hạt nhân. D. số proton và neutron trong hạt nhân. Câu 4: Khối lượng phân tử Cu(OH)2 bằng bao nhiêu amu? A. 64 B. 17 C. 98 D. 90 Câu 5: Phân tử Al2O3 được hình thành do A. sự kết hợp giữa 2 nguyên tử Al và 3 nguyên tử O B. sự kết hợp giữa 2 ion Al3+ và ion O2- C. sự kết hợp giữa 2 ion Al3+ và 3 ion O2- D. sự kết hợp giữa ion Al3+ và ion O2- Câu 6: Xác định công thức hóa học của potassium oxide. Biết K có hóa trị I và khối lượng phân tử của potassium oxide là 94amu A. KO2 B. K2O C. KO D. KO4 Câu 7: Nguyên tử Fe có hóa trị II trong công thức nào dưới đây? A. FeO. B. Fe2O3. C. Fe2(SO4)3. D. FeCl3. Câu 8: Biết rằng 2 nguyên tử magnesium nặng bằng 3 nguyên tử nguyên tố X. Nguyên tố X là A. He (helium). B. H (hydrogen). C. N (nitrogen). D. O (oxygen). Câu 9: Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo: A. Chiều tăng dần của số electron lớp ngoài cùng của nguyên tử. B. Chiều giảm dần của điện tích hạt nhân của nguyên tử. C. Chiều tăng dần của nguyên tử khối. D. Chiều tăng dần của điện tích hạt nhân của nguyên tử. Câu 10: Nguyên tố X có số hiệu nguyên tử là 11, chu kỳ 3, nhóm IA trong bảng tuần hoàn các nguyên tố hóa học. Phát biểu nào sau đây đúng? A. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 1 electron, kim loại mạnh. B. Điện tích hạt nhân là +11, 1 lớp electron, lớp ngoài cùng có 3 electron, kim loại mạnh. C. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 3 electron, kim loại yếu. D. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 1 electron, kim loại yếu.
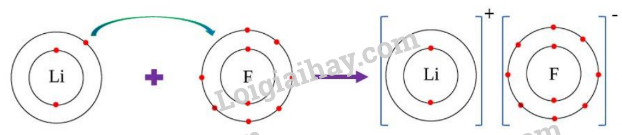
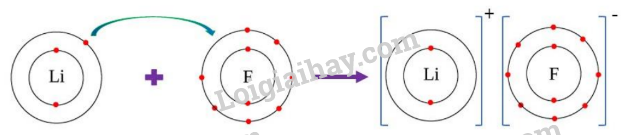
II. Tự luận Câu 1: Hợp kim chứa nguyên tố Aluminium (Al) nhẹ và bền, dùng chế tạo vỏ máy bay,…. nguyên tử nguyên tố Aluminium (Al) có tổng số các loại hạt cơ bản là 40 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Xác định số số hạt proton, neutron, electron, viết kí hiệu nguyên tử của Aluminium (Al). Câu 2: Cho sơ đồ mô tả sự hình thành liên kết ion trong phân tử lithium fluoride như sau: Hãy cho biết: a. Nguyên tử Li và nguyên tử F đã nhường hay nhận bao nhiêu electron. b. Sau khi nhường (nhận) electron để hình thành liên kết ion thì lớp vỏ của nguyên tử Li và nguyên tử F giống với lớp vỏ của nguyên tử khí hiếm nào?
Đáp án Phần trắc nghiệm
Câu 1: Có những hạt nào được tìm thấy trong hạt nhân của nguyên tử? A. Các hạt mang điện tích âm (electron). B. Các hạt neutron và hạt proton. C. Các hạt neutron không mang điện. D. Hạt nhân nguyên tử không chứa hạt nào bên trong. Phương pháp giải: Dựa vào cấu tạo của nguyên tử Lời giải chi tiết: Phát biểu A sai vì hạt electron ở vỏ nguyên tử. Phát biểu B đúng và phát biểu D sai vì hạt nhân nguyên tử được cấu tạo bởi hai loại hạt là proton và neutron (Riêng với nguyên tử hydrogen, hạt nhân chỉ chứa hạt proton). Phát biểu C sai vì trong hạt nhân nguyên tử còn có hạt proton mang điện tích dương và hạt neutron không mang điện tích. ⇨ Chọn B. Câu 2: Khối lượng nguyên tử của carbon là A. 16 amu. B. 12 amu. C. 6 amu. D. 24 amu. Lời giải chi tiết Đáp án B Câu 3: Số hiệu nguyên tử của một nguyên tố là A. số proton trong nguyên tử. B. số neutron trong nguyên tử. C. số electron trong hạt nhân. D. số proton và neutron trong hạt nhân. Lời giải chi tiết Số hiệu nguyên tử của một nguyên tố = số proton trong nguyên tử Câu 4: Khối lượng phân tử Cu(OH)2 bằng bao nhiêu amu? A. 64 B. 17 C. 98 D. 90 Phương pháp giải Khối lượng phân tử = tổng khối lượng các nguyên tử của nguyên tố tạo nên phân tử Lời giải chi tiết Khối lượng phân tử Cu(OH)2 = khối lượng nguyên tử Cu + 2. Khối lượng nguyên tử O + 2. Khối lượng nguyên tử H = 64 + 2.32 + 2 = 98amu Câu 5: Phân tử Al2O3 được hình thành do A. sự kết hợp giữa 2 nguyên tử Al và 3 nguyên tử O B. sự kết hợp giữa 2 ion Al3+ và ion O2- C. sự kết hợp giữa 2 ion Al3+ và 3 ion O2- D. sự kết hợp giữa ion Al3+ và ion O2- Lời giải chi tiết Al2O3 được hình thành do sự kết hợp giữa 2 ion Al3+ và 3 ion O2- Đáp án C Câu 6: Xác định công thức hóa học của potassium oxide. Biết K có hóa trị I và khối lượng phân tử của potassium oxide là 94amu A. KO2 B. K2O C. KO D. KO4 Phương pháp giải Dựa vào hóa trị của K và khối lượng phân tử của potassium oxide để xác định công thức hóa học Lời giải chi tiết Vì K có hóa trị I nên công thức hóa học là: KxO Vì khối lượng phân tử potassium oxide = x. MK + MO = 94amu => x. 39 + 16 = 94 => x = 2 (Với M là kí hiệu khối lượng nguyên tử) Vậy công thức hóa học là: K2O Câu 7: Nguyên tử Fe có hóa trị II trong công thức nào dưới đây? A. FeO. B. Fe2O3. C. Fe2(SO4)3. D. FeCl3. Lời giải chi tiết Đáp án A vì trong FeO nguyên tử O có hóa trị II nên tỉ lệ tối giản là: 1: 1 Câu 8: Biết rằng 2 nguyên tử magnesium nặng bằng 3 nguyên tử nguyên tố X. Nguyên tố X là A. He (helium). B. H (hydrogen). C. N (nitrogen). D. O (oxygen). Phương pháp giải Dựa vào khối lượng của 2 nguyên tử magnesium để xác định nguyên tố X Lời giải chi tiết 2 nguyên tử magnesium nặng: 2.24 = 48 (amu) vì 2 nguyên tử Mg nặng bằng 3 nguyên tố X nên khối lượng nguyên tử X là: 48 : 3 = 16 (amu) (oxygen) Đáp án D Câu 9: Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo: A. Chiều tăng dần của số electron lớp ngoài cùng của nguyên tử. B. Chiều giảm dần của điện tích hạt nhân của nguyên tử. C. Chiều tăng dần của nguyên tử khối. D. Chiều tăng dần của điện tích hạt nhân của nguyên tử. Phương pháp giải Dựa vào nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn Lời giải chi tiết Đáp án D Câu 10: Nguyên tố X có số hiệu nguyên tử là 11, chu kỳ 3, nhóm IA trong bảng tuần hoàn các nguyên tố hóa học. Phát biểu nào sau đây đúng? A. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 1 electron, kim loại mạnh. B. Điện tích hạt nhân là +11, 1 lớp electron, lớp ngoài cùng có 3 electron, kim loại mạnh. C. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 3 electron, kim loại yếu. D. Điện tích hạt nhân là +11, 3 lớp electron, lớp ngoài cùng có 1 electron, kim loại yếu. Phương pháp giải Dựa vào số hiệu nguyên tử, chu kì và nhóm của nguyên tố X để xác định vị trí của X trong bảng tuần hoàn Lời giải chi tiết Đáp án A II. Tự luận Câu 1: Hợp kim chứa nguyên tố Aluminium (Al) nhẹ và bền, dùng chế tạo vỏ máy bay,…. nguyên tử nguyên tố Aluminium (Al) có tổng số các loại hạt cơ bản là 40 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Xác định số số hạt proton, neutron, electron, viết kí hiệu nguyên tử của Aluminium (Al). Lời giải chi tiết Ta có: số e = số p = Z; số n = N \(\left\{ \begin{array}{l}{\rm{2Z + N = 40}}\\{\rm{2Z\;\; - \;N\; = 12}}\end{array} \right. \Leftrightarrow \) \(\left\{ \begin{array}{l}{\rm{Z = 13}}\\{\rm{N\; = 1}}4\end{array} \right.\) số e = số p = Z= 13 và số N=14 kí hiệu nguyên tử: \({}_{27}^{13}Al\) Câu 2: Cho sơ đồ mô tả sự hình thành liên kết ion trong phân tử lithium fluoride như sau:
Hãy cho biết: a. Nguyên tử Li và nguyên tử F đã nhường hay nhận bao nhiêu electron. b. Sau khi nhường (nhận) electron để hình thành liên kết ion thì lớp vỏ của nguyên tử Li và nguyên tử F giống với lớp vỏ của nguyên tử khí hiếm nào? Lời giải chi tiết a) Theo sơ đồ mô tả sự hình thành liên kết ion trong phân tử lithium fluoride ta thấy Nguyên tử Li cho 1 electron lớp ngoài cùng để thành ion dương Li+, nguyên tử fluoride nhận 1 electron từ lithium để có 8 electron lớp ngoài cùng b) Sau khi nhường 1 electron lớp ngoài, nguyên tử lithium còn 2 electron giống với nguyên tử khí hiếm helium,
|




















Danh sách bình luận