Lý thuyết chuyển đổi giữa khối lượng thể tích và lượng chất.Công thức chuyển đổi giữa lượng chất Quảng cáo
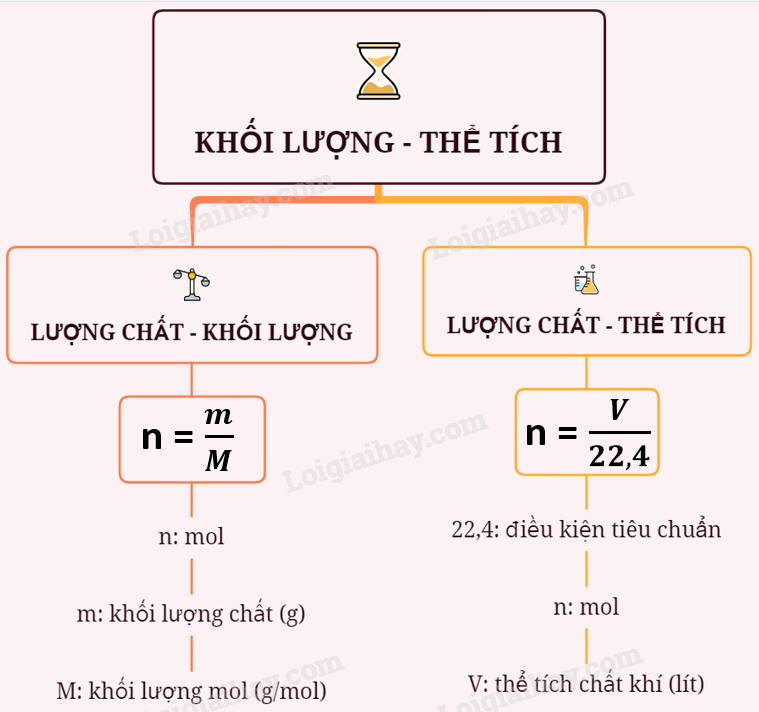
1. Chuyển đổi giữa lượng chất và khối lượng chất Ví dụ: Tính khối lượng của 0,25 mol CO2? Biết khối lượng mol của CO2 là 44 g/mol Hướng dẫn: Khối lượng của 0,25 mol CO2 là : ${{m}_{C{{O}_{2}}}}=0,25.44=11\,gam$ Ta biết: 1 mol phân tử CO2 có khối lượng 44 gam => 0,25 mol phân tử CO2 có khối lượng x gam => x = 0,25.44 = 11 gam hay ${{m}_{C{{O}_{2}}}}=11\,gam$ * Công thức: m = n.M (gam) Trong đó: n là số mol chất (mol) M là khối lượng mol chất (g/mol) m là khối lượng chất (gam) Ta có 2 công thức liên quan sau: $n=\frac{m}{M}\,(mol)$ và $M=\frac{m}{n}\,(g/mol)$ 2. Chuyển đổi giữa lượng chất và thể tích chất khí Ví dụ: 0,25 mol khí CO2 ở điều kiện tiêu chuẩn có thể tích là bao nhiêu lít? Hướng dẫn: 1 mol khí ở điều kiện tiêu chuẩn chiếm 22,4 lít => 0,25 mol ở điều kiện tiêu chuẩn chiếm: 0,25.22,4 = 5,6 lít * Công thức: V = n.22,4 (lít) Trong đó: n là số mol chất (mol) V : Thể tích chất ở điều kiện tiêu chuẩn (lít) Ta có công thức liên quan: $n=\frac{V}{22,4}\,(mol)$ Sơ đồ tư duy: Chuyển đổi giữa khối lượng thể tích và lượng chất.
|




















Danh sách bình luận