Bài 23.6* trang 31 SBT hóa học 8Giải bài 23.6* trang 31 sách bài tập hóa học 8. Đốt cháy hoàn toàn 2,24 g Fe, thu được 3,2 g oxit sắt. Xác định công thức phân tử của oxit sắt. Quảng cáo
Đề bài Đốt cháy hoàn toàn 2,24 g Fe, thu được 3,2 g oxit sắt. Xác định công thức phân tử của oxit sắt. Phương pháp giải - Xem chi tiết Xem lại lí thuyết tính theo phương trình hóa học Tại đây. Lời giải chi tiết + Cách 1: Phương trình hóa học dạng tổng quát: \(2xFe + y{O_2}\buildrel {{t^o}} \over\longrightarrow 2F{e_x}{O_y}\) x.112g 2(56x+16y)g 2,24g 3,2g Theo phương trình hóa học trên, ta có: \(2,24 \times 2(56x + 16y) = 3,2 \times 112x\) Giải ra ta có:\(3x = 2y = > \dfrac{x}{y} = \dfrac{2}{3}\) Do đó công thức phân tử của oxit sắt là \(F{e_2}{O_3}\) . + Cách 2: Cách 2: Khối lượng Oxi trong oxit là: 3,2 – 2,24 = 0,96 g Tỉ lệ nFe : nO = 0,04 : 0,06 = 2:3 ⇒ Trong 1 phân tử oxit có 2 nguyên tử Fe, 3 nguyên tử O ⇒ CT oxit là: Fe2O3. Loigiaihay.com
|














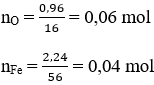






Danh sách bình luận