Đề thi giữa kì 1 KHTN 8 Cánh diều - Đề số 1Tải về Công dụng của ống đong là A. đo khối lượng B. đo thể tích C. bảo quản hóa chất D. đun nóng Câu 2: Trong các quá trình sau, quá trình nào xảy ra biến đổi vật lí? Tổng hợp đề thi học kì 2 lớp 8 tất cả các môn - Cánh diều Toán - Văn - Anh - Khoa học tự nhiên Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Đề thi I. Trắc nghiệm ( 7,5 điểm) Câu 1: Công dụng của ống đong là A. đo khối lượng B. đo thể tích C. bảo quản hóa chất D. đun nóng Câu 2: Trong các quá trình sau, quá trình nào xảy ra biến đổi vật lí? A. Nước hồ bị bốc hơi khi trời nắng. B. Diêm bị cháy khi quẹt vào vỏ hộp diêm. C. Thịt bị cháy khi nướng. D. Pháo hoa có nhiều màu sắc sặc sỡ. Câu 3: Sản phẩm của phản ứng: natri (sodium) + oxygen → sodium oxide là A. natri (sodium). B. oxygen. C. sodium oxide. D. natri (sodium) và oxygen. Câu 4: Phản ứng nào sau đây là phản ứng toả nhiệt? A. Phản ứng nung đá vôi CaCO3. B. Phản ứng đốt cháy khí gas. C. Phản ứng hòa tan viên C sủi vào nước. D. Phản ứng phân hủy đường. Câu 5: Chọn phát biểu đúng trong các phát biểu sau đây: A. Mol là lượng chất có chứa NA nguyên tử hoặc phân tử đó B. Mol là khối lượng của chất có chứa NA nguyên tử hoặc phân tử chất đó C. Mol là thể tích của chất có chứa NA nguyên tử hoặc phân tử chất đó D. Mol là nồng độ của chất có chứa NA nguyên tử hoặc phân tử chất đó Câu 6: Cho 20 gam muối ăn vào cố chứa 100g nước, dùng đũa khuấy đều cho đến khi muối ăn tan hết. Khối lượng nước muối thu được trong cốc nước là: A. 100g B. 20g C. 80g D. 120g Câu 7: Khối lượng của CuSO4 có trong 100ml dung dịch CuSO4 0,5 M là A. 80 gam B. 160 gam C. 16 gam. D. 8 gam. Câu 8: Đốt cháy hoàn toàn 1,24 gam phosphorus trong bình chứa 1,92 gam khí oxygen (ở dktc) tạo thành phosphorus pentoxide ( P2O5). Khối lượng chất còn dư sau phản ứng là A. 0,68gam. B. 0,64 gam. C. 0,16 gam. D. 0,32 gam. Câu 9: Phát biểu nào dưới đây là đúng? A. Bất cứ phản ứng nào cũng chỉ cần vận dụng một yếu tố ảnh hưởng đến tốc độ của phản ứng để làm tăng tốc độ của phản ứng. B. Bất cứ phản ứng nào cũng phải vận dụng đủ các yếu tố ảnh hưởng đến tốc độ của phản ứng mới tăng được tốc độ của phản ứng. C. Tùy theo phản ứng mà vận dụng một, một số hay tất cả các yếu tố ảnh hưởng đến tốc độ của phản ứng để làm tăng tốc độ của phản ứng. D. Bất cứ phản ứng nào cũng cần chất xúc tác để làm tăng tốc độ của phản ứng. Câu 10: Dung dịch nào sau đây không làm đổi màu quỳ tím thành đỏ? A. Nước muối. B. Giấm ăn. C. Nước chanh. D. Nước ép quả khế. Câu 11: Dãy chất nào sau đây chỉ gồm các base? A. NaOH, CaO, KOH, Mg(OH)2. B. NaOH, Ca(OH)2,KOH, Mg(OH)2. C. NaOH, CaSO4, KOH, Mg(OH)2. D. NaOH, Ca(OH)2, KOH, MgO Câu 12: Tên gọi carbon dioxide ứng với công thức nào sau đây? A. CO2. B. CO. C. C2O. D. H2CO3. Câu 13: Hợp chất X được tạo thành từ sự thay thế ion H+ của acid bằng ion kim loại hoặc ion ammonium (NH4+). Chất X thuộc loại chất gì? A. Muối. B. Acid. C. Base. D. Oxide. Câu 14: Thang pH thường dùng có giá trị A. từ 7 đến 14. B. từ 0 đến 14. C. từ 3 đến 14. D. từ 1 đến 7. Câu 15: Một trong các nguyên tố hóa học cần cung cấp cho cây trồng với một lượng nhỏ (vi lượng) dưới dạng hợp chất là. A. N. B. Zn. C. P. D. K. II. Tự luận (2,5 điểm) Câu 1 (1 điểm): Hoàn thành dãy chuyển hóa sau:
Câu 2 (1,5 điểm): Cho 200ml dung dịch Na2SO4 0,1M tác dụng vừa đủ với dung dịch BaCl2 thu được m gam kết tủa a) Viết phương trình hóa học b) Tính khối lượng m (g) c) Tính nồng độ dung dịch BaCl2, biết thể tích dung dịch BaCl2 đã dùng là 50ml Đáp án Phần trắc nghiệm
Câu 1: Công dụng của ống đong là A. đo khối lượng B. đo thể tích C. bảo quản hóa chất D. đun nóng Phương pháp giải Công dụng của ống đong để đo thể tích Lời giải chi tiết Đáp án B Câu 2: Trong các quá trình sau, quá trình nào xảy ra biến đổi vật lí? A. Nước hồ bị bốc hơi khi trời nắng. B. Diêm bị cháy khi quẹt vào vỏ hộp diêm. C. Thịt bị cháy khi nướng. D. Pháo hoa có nhiều màu sắc sặc sỡ. Phương pháp giải Biến đổi vật lí chỉ thay đổi về trạng thái, kích thức màu sắc nhưng không thay đổi về chất Lời giải chi tiết Đáp án A: nước dạng lỏng chuyển thành dạng hơi Câu 3: Sản phẩm của phản ứng: natri (sodium) + oxygen → sodium oxide là A. natri (sodium). B. oxygen. C. sodium oxide. D. natri (sodium) và oxygen. Phương pháp giải Sản phẩm là chất được tạo thành từ phản ứng Lời giải chi tiết Đáp án C Câu 4: Phản ứng nào sau đây là phản ứng toả nhiệt? A. Phản ứng nung đá vôi CaCO3. B. Phản ứng đốt cháy khí gas. C. Phản ứng hòa tan viên C sủi vào nước. D. Phản ứng phân hủy đường. Phương pháp giải Phản ứng tỏa nhiệt là phản ứng tỏa ra năng lượng dưới dạng nhiệt Lời giải chi tiết Đáp án B Câu 5: Chọn phát biểu đúng trong các phát biểu sau đây: A. Mol là lượng chất có chứa NA nguyên tử hoặc phân tử đó B. Mol là khối lượng của chất có chứa NA nguyên tử hoặc phân tử chất đó C. Mol là thể tích của chất có chứa NA nguyên tử hoặc phân tử chất đó D. Mol là nồng độ của chất có chứa NA nguyên tử hoặc phân tử chất đó Phương pháp giải Dựa vào định nghĩa về mol chất Lời giải chi tiết Đáp án A Câu 6: Cho 20 gam muối ăn vào cố chứa 100g nước, dùng đũa khuấy đều cho đến khi muối ăn tan hết. Khối lượng nước muối thu được trong cốc nước là: A. 100g B. 20g C. 80g D. 120g Phương pháp giải Khối lượng dung dịch = khối lượng chất tan + khối lượng nước Lời giải chi tiết Khối lượng nước muối = 20 + 100 = 120g Câu 7: Khối lượng của CuSO4 có trong 100ml dung dịch CuSO4 0,5 M là A. 80 gam B. 160 gam C. 16 gam. D. 8 gam. Phương pháp giải Dựa vào công thức CM = \(\frac{n}{V}\)để tính được số mol của CuSO4 Lời giải chi tiết \(\begin{array}{l}{n_{CuSO4}} = {C_M}.V = 0,5.0,1 = 0,05mol\\{m_{CuSO4}} = 0,05.160 = 8g\end{array}\) Đáp án D Câu 8: Đốt cháy hoàn toàn 1,24 gam phosphorus trong bình chứa 1,92 gam khí oxygen (ở dktc) tạo thành phosphorus pentoxide ( P2O5). Khối lượng chất còn dư sau phản ứng là A. 0,68gam. B. 0,64 gam. C. 0,16 gam. D. 0,32 gam. Phương pháp giải Tính số mol của P, O2. Viết phương trình phản ứng, tính chất hết chất dư Lời giải chi tiết \(\begin{array}{l}{n_P} = \frac{{1,24}}{{31}} = 0,04;{n_{O2}} = \frac{{1,92}}{{32}} = 0,06\\4P + 5{O_2} \to 2{P_2}{O_5}\\0,04...0,06\\{n_{O2}} > {n_P}\end{array}\) Phosphorus hết, oxygen dư n O2 dư = 0,06 – 0,05 = 0,01 mol m O2 dư = 0,01 . 32= 0,32g Đáp án D Câu 9: Phát biểu nào dưới đây là đúng? A. Bất cứ phản ứng nào cũng chỉ cần vận dụng một yếu tố ảnh hưởng đến tốc độ của phản ứng để làm tăng tốc độ của phản ứng. B. Bất cứ phản ứng nào cũng phải vận dụng đủ các yếu tố ảnh hưởng đến tốc độ của phản ứng mới tăng được tốc độ của phản ứng. C. Tùy theo phản ứng mà vận dụng một, một số hay tất cả các yếu tố ảnh hưởng đến tốc độ của phản ứng để làm tăng tốc độ của phản ứng. D. Bất cứ phản ứng nào cũng cần chất xúc tác để làm tăng tốc độ của phản ứng. Phương pháp giải Các yếu tố ảnh hưởng đến tốc độ phản ứng tùy thuộc vào từng loại phản ứng để làm tăng hoặc giảm tốc độ Lời giải chi tiết Đáp án C Câu 10: Dung dịch nào sau đây không làm đổi màu quỳ tím thành đỏ? A. Nước muối. B. Giấm ăn. C. Nước chanh. D. Nước ép quả khế. Phương pháp giải Dung dịch không làm quỳ tím hóa đỏ là muối hoặc dung dịch base Lời giải chi tiết Đáp án A Câu 11: Dãy chất nào sau đây chỉ gồm các base? A. NaOH, CaO, KOH, Mg(OH)2. B. NaOH, Ca(OH)2,KOH, Mg(OH)2. C. NaOH, CaSO4, KOH, Mg(OH)2. D. NaOH, Ca(OH)2, KOH, MgO Phương pháp giải Dựa vào phân loại base Lời giải chi tiết Đáp án B Câu 12: Tên gọi carbon dioxide ứng với công thức nào sau đây? A. CO2. B. CO. C. C2O. D. H2CO3. Lời giải chi tiết Đáp án A Câu 13: Hợp chất X được tạo thành từ sự thay thế ion H+ của acid bằng ion kim loại hoặc ion ammonium (NH4+). Chất X thuộc loại chất gì? A. Muối. B. Acid. C. Base. D. Oxide. Lời giải chi tiết Đáp án A Câu 14: Thang pH thường dùng có giá trị A. từ 7 đến 14. B. từ 1 đến 14. C. từ 3 đến 14. D. từ 1 đến 7. Lời giải chi tiết Đáp án B Câu 15: Một trong các nguyên tố hóa học cần cung cấp cho cây trồng với một lượng nhỏ (vi lượng) dưới dạng hợp chất là. A. N. B. Zn. C. P. D. K. Phương pháp giải Dựa vào kiến thức về phân bón hóa học Lời giải chi tiết Đáp án B II. Tự luận (2,5 điểm) Câu 1 (1 điểm): Hoàn thành dãy chuyển hóa sau: Lời giải chi tiết \(\begin{array}{l}(1)C + {O_2} \to C{O_2}\\(2)C{O_2} + NaOH \to N{a_2}C{O_3} + {H_2}O\\(3)N{a_2}C{O_3} + Ca{(OH)_2} \to CaC{O_3} + 2Na{\rm{OH}}\end{array}\) Câu 2 (1,5 điểm): Cho 200ml dung dịch Na2SO4 0,1M tác dụng vừa đủ với dung dịch BaCl2 thu được m gam kết tủa a) Viết phương trình hóa học b) Tính khối lượng m (g) c) Tính nồng độ dung dịch BaCl2, biết thể tích dung dịch BaCl2 đã dùng là 50ml Lời giải chi tiết a) Na2SO4 + BaCl2 \( \to \)2NaCl + BaSO4 b) n Na2SO4 = 0,2. 0,1 = 0,02 mol Na2SO4 + BaCl2 \( \to \)2NaCl + BaSO4 0,02 0,02 0,02 m BaSO4 = 0,02.233 = 4,66g c) V dung dịch BaCl2 = 0,05L CM BaCl2 = 0,02 : 0,05 = 0,4M
|














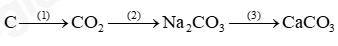
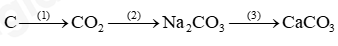






Danh sách bình luận