Bài 18. Cấu tạo và liên kết trong tinh thể kim loại trang 63, 64, 65 SBT Hóa 12 Kết nối tri thứcCho biết số thứ tự của Mg trong bảng tuần hoàn là 12. Vị trí của Mg trong bảng tuần hoàn là Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
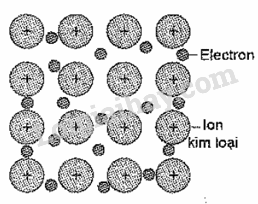
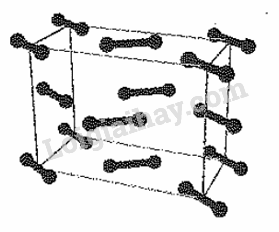
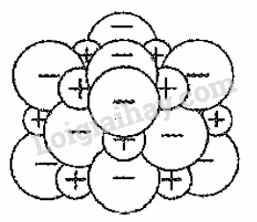
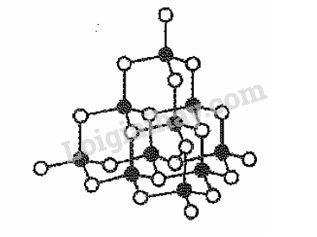
18.1 Cho biết số thứ tự của Mg trong bảng tuần hoàn là 12. Vị trí của Mg trong bảng tuần hoàn là A. chu kì 3, nhóm IIIA B. chu kì 3, nhóm IIB. C. chu kì 3, nhóm IIA D. chu kì 2, nhóm IIA Phương pháp giải: Dựa vào vị trí của Mg trong bảng tuần hoàn. Lời giải chi tiết: Cấu hình electron của Mg là: 1s2 2s22p6 3s2 Vị trí của Mg trong bảng tuần hoàn là chu kì 3, nhóm IIA. Đáp án C 18.2 Cho biết số thứ tự của Al trong bảng tuần hoàn là 13. Số electron lớp ngoài cùng của Al là A. 1 B. 2 C. 3 D. 4 Phương pháp giải: Dựa vào cấu hình electron của Al. Lời giải chi tiết: Cấu hình của Al là: 1s2 2s22p6 3s23p1 Số electron lớp ngoài cùng là 3. Đáp án C 18.3 Hình vẽ nào sau đây có thể được dùng để mô tả cấu trúc tinh thể kim loại? A. B. C. D. Phương pháp giải: Dựa vào cấu tạo tinh thể kim loại. Lời giải chi tiết: Trong tinh thể kim loại. lực hút tĩnh điện giữa các ion dương ở nút mạng với các electron hóa trị chuyển động tự do tạo nên liên kết kim loại.
Đáp án A 18.4 Trong định nghĩa về liên kết kim loại: “ Liên kết kim loại là liên kết hình thành do lực hút tĩnh điện giữa các electron...(1)... với các ion...(2)... kim loại ở các nút mạng. Các từ cần điền vào vị trí (1), (2) là A. ngoài cùng, dương B. tự do, dương. C. hóa trị, lưỡng cực. D. hóa trị, âm. Phương pháp giải: Dựa vào khái niệm về tinh thể kim loại. Lời giải chi tiết: Trong tinh thể kim loại. lực hút tĩnh điện giữa các ion dương ở nút mạng với các electron hóa trị chuyển động tự do tạo nên liên kết kim loại. (1) tự do, (2) dương. Đáp án B 18.5 Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên bởi A. các electron tự do trong mạng tinh thể kim loại. B. kiểu cấu tạo mạng tinh thể kim loại. C. khối lượng riêng của kim loại. D. tính chất của kim loại. Phương pháp giải: Dựa vào tính chất vật lí của kim loại. Lời giải chi tiết: Những tính chất vật lí gây nên bởi các electron tự do trong mạng tinh thể kim loại. Đáp án A 18.6 Cho các phát biểu sau đây về vị trí và cấu tạo của kim loại: (1) Hầu hết các kim loại chỉ có từ 1 electron đến 3 electron lớp ngoài cùng. (2) Tất cả các nguyên tố phân nhóm B (phân nhóm phụ) đều là kim loại. (3) Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể. (4) Các kim loại đều có bán kính nhỏ hơn các phi kim thuộc cùng 1 chu kì. (5) Liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion dương kim loại trong mạng tinh thể do sự tham gia của các electron tự do. Những phát biểu đúng là A. (1), (2), (3), (5). B. (1), (2), (3),(4), (5). C. (1), (2), (3). D. (1), (3), (5). Phương pháp giải: Dựa vào cấu tạo của kim loại. Lời giải chi tiết: (1), (2), (3), (5) là những phát biểu đúng về vị trí và cấu tạo của kim loại. (4) sai, vì các kim loại IA có bán kính lớn hơn phi kim thuộc cùng một chu kì. Đáp án A 18.7 Phát biểu nào sau đây đúng? Trong tinh thể kim loại A. các ion dương kim loại nằm ở các nút mạng tinh thể và các electron hóa trị chuyển động tự do xung quanh. B. các electron hóa trị ở các nút mạng và các ion dương kim loại chuyển động tự do. C.các electron hóa trị và các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể. D. các electron hóa trị nằm ở giữa các nguyên tử kim loại cạnh nhau. Phương pháp giải: Dựa vào khái niệm của tinh thể kim loại. Lời giải chi tiết: Trong tinh thể kim loại các ion dương kim loại nằm ở các nút mạng tinh thể và các electron hóa trị chuyển động tự do xung quanh. Đáp án A 18.8 Phát biểu nào sau đây đúng? Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do A. sự góp chung electron của các nguyên tử kim loại cạnh nhau. B. lực hút tĩnh điện giữa các electron hóa trị ở các nút mạng với các ion dương kim loại chuyển động tự do. C. lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể. D. lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng. Phương pháp giải: Dựa vào sự hình thành liên kết kim loại. Lời giải chi tiết: Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở nút mạng. Đáp án D 18.9 Hãy chọn đúng hoặc sai cho mỗi ý a,b,c,d ở các câu 18.9 – 18.11. a) Nguyên tử kim loại thường có 1,2, hoặc 3 electron ở lớp ngoài cùng. b) Trong bảng tuần hoàn, các nhóm A bao gồm các nguyên tố s và nguyên tố p. c) Trong 1 chu kì, kim loại có bán kính nhỏ hơn phi kim. d) Kim loại có ánh kim do các electron tự do phản xạ ánh sáng nhìn thấy được. Phương pháp giải: Dựa vào vị trí của kim loại trong bảng tuần hoàn. Lời giải chi tiết: a) đúng b) đúng c) sai, trong 1 chu kì kim loại có bán kính lớn hơn phi kim. d) đúng 18.10 a) Nguyên tử của hầu hết các nguyên tố kim loại đều có ít electron ở lớp ngoài cùng. b) Những tính chất vật lí chung của kim loại chủ yếu do các electron tự do trong mạng tinh thể kim loại gây ra. c) Tính chất hóa học chung của kim loại là tính oxi hóa. d) Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử. Phương pháp giải: Dựa vào tính chất của kim loại. Lời giải chi tiết: a) đúng b) đúng c) sai, tính chất hóa học chung của kim loại là tính khử. d) đúng 18.11 a) Liên kết kim loại là liên kết cộng hóa trị đều có sự tham gia của các electron. b) Liên kết kim loại khác với liên kết cộng hóa trị ở số electron dùng chung c) Liên kết kim loại và liên kết ion đều sinh ra bởi lực hút tĩnh điện. d) Liên kết kim loại khác với liên kết ion ở loại hạt mang điện tham gia. Phương pháp giải: Dựa vào liên kết kim loại. Lời giải chi tiết: a) Đúng b) Đúng c) Đúng d) Đúng
|




















Danh sách bình luận