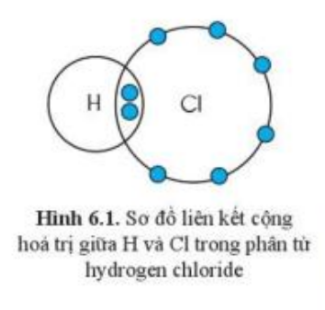
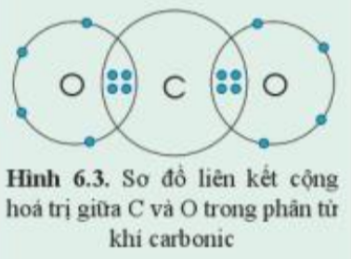
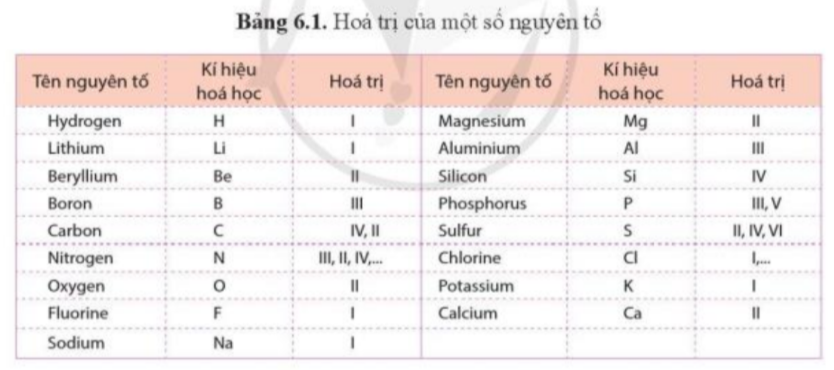
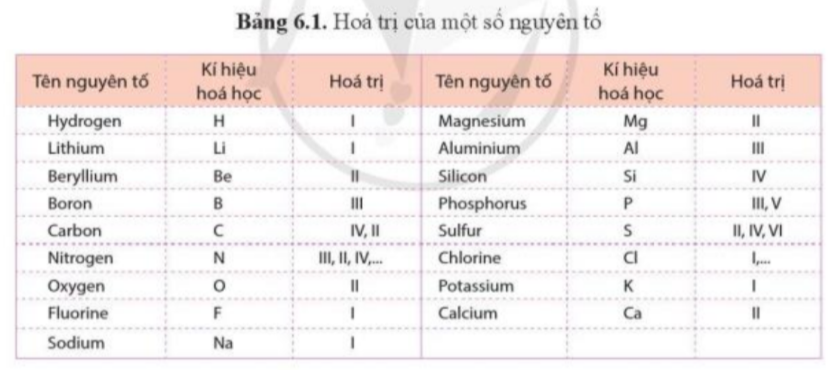
Bài 6. Hóa trị, công thức hóa học trang 39, 40, 41, 42, 43, 44, 45 Khoa học tự nhiên 7 Cánh diềuTải vềCho các miếng bìa ghi kí hiệu hóa học của các nguyên tố C, O, Cl, H như hình dưới đây Quan sát hình 6.1, hãy so sánh hóa trị của nguyên tố và số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết Quan sát hình 6.3 và xác định hóa trị của C và O trong khí carbonic Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Tải về
CH tr 39 MĐ
Lời giải chi tiết: - 1 nguyên tử C ghép được tối đa 4 nguyên tử H => CH4 - 1 nguyên tử O ghép được tối đa 2 nguyên tử H => H2O - 1 nguyên tử Cl ghép được tối đa 1 nguyên tử H => HCl CH tr 39 CH
Phương pháp giải: H và Cl đều có hóa trị I Lời giải chi tiết: - Trong hình 6.1, mỗi nguyên tử H và Cl góp 1 electron tạo ra đôi electron dùng chung giữa 2 nguyên tử - H và Cl đều có hóa trị I => Hóa trị của nguyên tố = số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết CH tr 40 LT
Phương pháp giải: Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác Lời giải chi tiết: - Mỗi nguyên tử O góp chung 2 electron - Nguyên tử C góp chung 4 electron => Nguyên tử C liên kết với 2 nguyên tử O bằng 4 cặp đôi electron chung => C có hóa trị IV và O có hóa trị II CH tr 40 LT
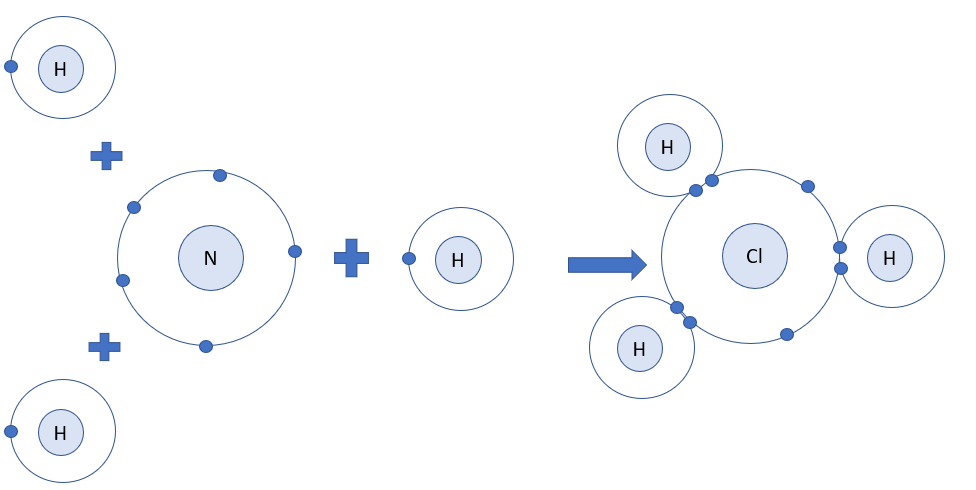
Phương pháp giải: - Nguyên tử N có 5 electron ở lớp ngoài cùng => Cần thêm 3 electron để đạt cấu hình electron của khí hiếm Ne - Nguyên tử H có 1 electron ở lớp ngoài cùng => Cần nhận thêm 1 electron để đạt cấu hình electron của khí hiếm He - Trong hợp chất cộng hóa trị, hóa trị của nguyên tố = số electron mà nguyên tử nguyên tố đó góp chung với nguyên tử khác Lời giải chi tiết: - Nguyên tử N có 5 electron ở lớp ngoài cùng => Cần thêm 3 electron để đạt cấu hình electron của khí hiếm Ne - Nguyên tử H có 1 electron ở lớp ngoài cùng => Cần nhận thêm 1 electron để đạt cấu hình electron của khí hiếm He => Khi 3 nguyên tử H và 1 nguyên tử N liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử N góp ra 3 electron để tạo ra 3 đôi electron dùng chung => Sơ đồ tạo thành phân tử hydrogen chloride từ nguyên tử H và N:
=> Hợp chất NH3 là liên kết cộng hóa trị - Mỗi nguyên tử H góp chung 1 electron, nguyên tử N góp chung 3 electron => H có hóa trị I, N có hóa trị III CH tr 41 CH
Phương pháp giải: Quy tắc hóa trị: Khi các nguyên tử của 2 nguyên tố A, B liên kết với nhau, tích giữa hóa trị và số nguyên tử của A bằng tích giữa hóa trị và số nguyên tử của B Lời giải chi tiết:
=> Tích hóa trị và số nguyên tử của nguyên tố Si = tích hóa trị và số nguyên tử của nguyên tố O CH tr 41 LT
Phương pháp giải: 1. Quy tắc hóa trị: Khi các nguyên tử của 2 nguyên tố A, B liên kết với nhau, tích giữa hóa trị và số nguyên tử của A bằng tích giữa hóa trị và số nguyên tử của B 2. Bước 1: Gọi số nguyên tử của nguyên tố A, B lần lượt là x và y Bước 2: Áp dụng quy tắc hóa trị Bước 3: Tính tỉ lệ Lời giải chi tiết: 1. - Gọi số nguyên tử của nguyên tố Mg (II), Cl (I) lần lượt là x và y - Áp dụng quy tắc hóa trị ta có: II.x = I.y
2. - Gọi số nguyên tử của nguyên tố A (III), B (II) lần lượt là x và y
CH tr 41 CH
Phương pháp giải: - Công thức hóa học gồm 2 phần: + Phần chữ: kí hiệu hóa học của các nguyên tố tạo thành chất + Phần số: số được ghi dưới chân kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong 1 phân tử Lời giải chi tiết: a) N2: Nguyên tố tạo thành là N, có 2 nguyên tử N b) NaCl gồm: + Nguyên tố Na, có 1 nguyên tử Na + Nguyên tố Cl, có 1 nguyên tử Cl c) MgSO4 gồm: + Nguyên tố Mg, có 1 nguyên tử Mg + Nguyên tố S, có 1 nguyên tử S + Nguyên tố O, có 4 nguyên tử O CH tr 42 LT
Phương pháp giải: - Phần chữ: kí hiệu hóa học của các nguyên tố tạo thành chất - Phần số: số được ghi dưới chân (bên phải) kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong 1 phân tử Lời giải chi tiết: a) Sodium sulfide: 2 nguyên tử Na, 1 nguyên tử S => Na2S b) Phosphoric acid: 3 nguyên tử H, 1 nguyên tử P, 4 nguyên tử O => H3PO4 CH tr 42 LT
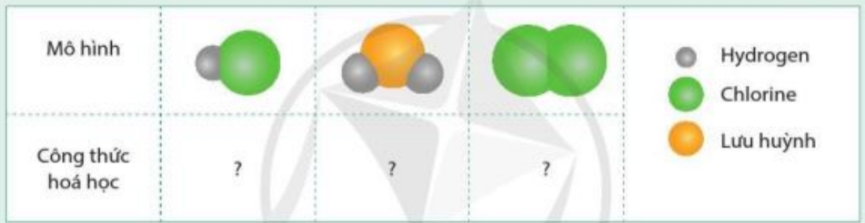
Phương pháp giải: - Phần chữ: kí hiệu hóa học của các nguyên tố tạo thành chất - Phần số: số được ghi dưới chân (bên phải) kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong 1 phân tử + Hydrogen: H + Chlorine: Cl + Lưu huỳnh: S Lời giải chi tiết: - Mô hình 1: 1 nguyên tử H, 1 nguyên tử Cl => HCl - Mô hình 2: 2 nguyên tử H, 1 nguyên tử S => H2S - Mô hình 3: 2 nguyên tử Cl => Cl2 CH tr 42 LT
Phương pháp giải: a) Phần chữ của công thức hóa học: kí hiệu hóa học của các nguyên tố tạo thành chất b) Khối lượng mỗi nguyên tố = khối lượng nguyên tử x chỉ số của nguyên tố đó c) Khối lượng phân tử = tổng khối lượng của các nguyên tố tạo nên phân tử Lời giải chi tiết: a) Glucose được tạo thành từ những nguyên tố: C, H và O b) - Nguyên tố C: Có 6 nguyên tử C (khối lượng nguyên tử: 12 amu) => Khối lượng nguyên tố C trong 1 phân tử glucose = 12 amu x 6 = 72 amu - Nguyên tố H: Có 12 nguyên tử H (khối lượng nguyên tử: 1 amu) => Khối lượng nguyên tố H trong 1 phân tử glucose = 1 amu x 12 = 12 amu - Nguyên tố O: Có 6 nguyên tử O (khối lượng nguyên tử: 16 amu) => Khối lượng nguyên tố O trong 1 phân tử glucose = 16 amu x 6 = 96 amu c) Khối lượng phân tử glucose = khối lượng nguyên tố C + khối lượng nguyên tố H + khối lượng nguyên tố O = 72 amu + 12 amu + 96 amu = 180 amu CH tr 43 CH
Phương pháp giải: Bước 1: Tính khối lượng mỗi nguyên tố có trong 1 phân tử hợp chất Bước 2: Tính khối lượng phân tử Bước 3: Tính phần trăm khối lượng của nguyên tố theo công thức: Lời giải chi tiết: Trong phân tử nước gồm: 1 nguyên tử O và 2 nguyên tử H Ta có: Khối lượng của nguyên tố O trong nước là: mO = 1 x 16 amu = 16 amu Khối lượng của nguyên tố H trong nước là: mH = 2 x 1 amu = 2 amu => Khối lượng phân tử nước là: Mnước = 16 + 2 = 18 amu
=> Ý kiến: Phần trăm khối lượng của H trong nước gấp 2 lần phần trăm khối lượng O là sai CH tr 43 LT
Phương pháp giải: Bước 1: Tính khối lượng mỗi nguyên tố có trong 1 phân tử hợp chất Bước 2: Tính khối lượng phân tử Bước 3: Tính phần trăm khối lượng của nguyên tố theo công thức: Lời giải chi tiết: 1. Calcicum carbonate gồm: 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O Ta có: Khối lượng của nguyên tố Ca trong CaCO3 là: mCa = 1 x 40 amu = 40 amu Khối lượng của nguyên tố C trong CaCO3 là: mC = 1 x 12 amu = 12 amu Khối lượng của nguyên tố O trong CaCO3 là: mO = 3 x 16 amu = 48 amu => Khối lượng phân tử CaCO3 là: MCaCO3 = 40 + 12 + 48 = 100 amu
2. Citric acid gồm: 6 nguyên tử C, 8 nguyên tử H và 7 nguyên tử O Ta có: Khối lượng của nguyên tố C trong C6H8O7 là: mC = 6 x 12 amu = 72 amu Khối lượng của nguyên tố H trong C6H8O7 là: mH = 1 x 8 amu = 8 amu Khối lượng của nguyên tố O trong C6H8O7 là: mO = 7 x 16 amu = 112 amu => Khối lượng phân tử C6H8O7 là: MC6H8O7 = 72 + 8 + 112 = 192 amu
CH tr 43 VD
Phương pháp giải: Tính phần trăm của K trong 2 hợp chất là KCl và K2SO4 Bước 1: Tính khối lượng nguyên tố K có trong 1 phân tử hợp chất Bước 2: Tính khối lượng phân tử Bước 3: Tính phần trăm khối lượng của nguyên tố theo công thức: Lời giải chi tiết: - Xét hợp chất KCl: Ta có: Khối lượng của nguyên tố K trong KCl là: mK = 1 x 39 amu = 39 amu Khối lượng phân tử KCl là: MKCl = 1 x 39 amu + 1 x 35,5 amu = 74,5 amu
- Xét hợp chất K2SO4: Ta có: Khối lượng của nguyên tố K trong K2SO4 là: mK = 2 x 39 amu = 78 amu Khối lượng phân tử K2SO4 là: MK2SO4 = 2 x 39 amu + 1 x 32 amu + 4 x 16 amu = 174 amu
=> Hàm lượng K trong KCl nhiều hơn trong K2SO4 => Người trồng muốn sử dụng loại phân bón có hàm lượng K cao hơn thì nên chọn phân bón potassium sulfate CH tr 44 LT
Phương pháp giải: Bước 1: Đặt hóa trị của nguyên tố chưa biết là a Bước 2: Xác định a dựa vào quy tắc hóa trị Lời giải chi tiết: - Xét hợp chất HBr: + Gọi hóa trị của Br trong hợp chất là a + Vì H có hóa trị I nên ta có biểu thức: a x 1 = I x 1 => a = I => Vậy H có hóa trị I và Br có hóa trị I - Xét hợp chất BaO + Gọi hóa trị của Ba trong hợp chất là a + Vì O có hóa trị II nên ta có biểu thức: a x 1 = II x 1 => a = II => Vậy O có hóa trị II và Ba có hóa trị II CH tr 45 LT
Phương pháp giải: Bước 1: Đặt công thức hóa học của chất là FexOy Bước 2: Tính khối lượng của Fe và O trong 1 phân tử chất Bước 3: Tìm x, y Lời giải chi tiết: Đặt công thức hóa học của X là FexOy Khối lượng của nguyên tố Fe trong 1 phân tử X là: Khối lượng của nguyên tố O trong 1 phân tử X là: 160 – 112 = 48 amu Ta có: 56 amu . x = 112 amu => x = 2 16 amu . y = 48 amu => y = 3 Vậy công thức hóa học của X là Fe2O3
|
|||||||||||||||||||||||||||
























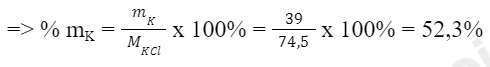
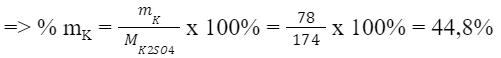







Danh sách bình luận