Đề thi học kì 1 Hóa 12 - Đề số 4Đề bài
Câu 1 :
Amin là hợp chất khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3
Câu 2 :
Polime có mạch phân nhánh là
Câu 3 :
Đipeptit mạch hở X và tripeptit mạch hở Y đều được tạo ra từ một loại amino axit no, mạch hở có một nhóm NH2 và một nhóm COOH. Đốt cháy hoàn toàn 0,1 mol Y thu được sản phẩm gồm CO2, H2O, và N2 trong đó tổng khối lượng CO2 và H2O bằng 54,9 gam. Nếu đốt cháy hoàn toàn 0,2 mol X, sản phẩm thu được cho lội qua dung dịch nước vôi trong dư thì thu được m gam kết tủa. Giá trị của m là
Câu 4 :
Chất nào sau đây không có nhóm –OH hemiaxetal ?
Câu 5 :
Amin X có công thức đơn giản nhất là CH5N. Công thức phân tử của X là :
Câu 6 :
Cho sơ đồ chuyển hóa sau: C3H4O2 + NaOH → X + Y X + H2SO4 loãng → Z + T Biết Y và Z đều có phản ứng tráng gương. Hai chất Y, Z tương ứng là
Câu 7 :
Khi thủy phân hoàn toàn 65 gam một oligopeptit X thu được 22,25 gam alanin và 56,25 gam glyxin. X thuộc loại nào?
Câu 8 :
Đốt cháy hoàn toàn 0,5 mol hỗn hợp X gồm 2 chất H2NR(COOH)x và CnH2n+1COOH, thu được 52,8 gam CO2 và 24,3 gam H2O. Mặt khác, 0,1 mol X phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
Câu 9 :
Amin nào sau đây tồn tại ở trạng thái khí ở điều kiện thường ?
Câu 10 :
Tính chất của glucozơ là : kết tinh (1), có vị ngọt (2), thủy phân trong nước (3), thể hiện tính chất của poliancol (4), thể hiện tính chất của axit (5), thể hiện tính chất của anđehit (6), thể hiện tính chất của ete (7). Những tính chất đúng là :
Câu 11 :
Đốt cháy hoàn toàn 2,01 gam hỗn hợp X gồm axit acrylic, vinyl axetat, metyl metacrylat. Toàn bộ sản phẩm cháy cho qua dung dịch Ca(OH)2 dư, sau phản ứng thu được 9 gam kết tủa và dung dịch X. Vậy khối lượng dung dịch X đã thay đổi so với dung dịch Ca(OH)2 ban đầu là:
Câu 12 :
Hai chất hữu cơ X, Y là đồng phân của nhau và có công thức phân tử là C3H7O2N. X tác dụng với NaOH thu được muối X1 có công thức phân tử là C2H4O2NNa ; Y tác dụng với NaOH thu được muối Y1 có công thức phân tử là C3H3O2Na. Tìm công thức cấu tạo của X, Y?
Câu 13 :
Công thức hóa học nào sau đây là của nước Svayde, dùng để hòa tan xenlulozơ trong quá trình sản xuất tơ nhân tạo ?
Câu 14 :
Hỗn hợp X gồm một ancol và một axit cacboxylic đều no, đơn chức, mạch hở, có cùng số nguyên tử cacbon trong phân tử. Đốt cháy hoàn toàn 51,24 gam X, thu được 101,64 gam CO2. Đun nóng 51,24 gam X với xúc tác H2SO4 đặc, thu được m gam este (hiệu suất phản ứng este hóa bằng 60%). Giá trị m gần nhất với giá trị nào sau đây?
Câu 15 :
Cho sơ đồ phản ứng : Thuốc súng không khói $\leftarrow $ X $\to $ Y $\to $ Sobitol Tên gọi X, Y lần lượt là
Câu 16 :
Khi thủy phân HCOOC6H5 trong môi trường kiềm dư thì thu được:
Câu 17 :
Nhận xét nào sau đây không đúng ?
Câu 18 :
Để phản ứng este hóa chuyển dịch ưu tiên theo chiều nghịch, cần dùng các giải pháp nào sau đây?
Câu 19 :
Để phản ứng hết với một lượng hỗn hợp gồm 2 chất hữu cơ X và Y ( MX < MY) càn vừa đủ 100 ml dung dịch NaOH 1,5M. Sau khi phản ứng xảy ra hoàn toàn thu được 10,2 gam muối của môt axit hữu cơ và m gam một ancol. Đốt cháy hoàn toàn lượng ancol trên thu được 1,12 lít khí CO2 (đktc) và 1,8 gam nước. Công thức của X là
Câu 20 :
Cho các đồng phân của amin bậc 1 của C3H9N tác dụng với dung dịch HCl thì có thể tạo ra tối đa bao nhiêu muối?
Câu 21 :
Cho các phát biểu sau:
Số phát biểu đúng là?
Câu 22 :
Cho các chất sau: HCl, FeCl2, NaNO2/HCl, Br2. Số chất chất tác dụng với metylamin là?
Câu 23 :
Đốt cháy hoàn toàn một hỗn hợp X (glucozơ, fructozơ, metanal và etanoic) cần 22,4 lít O2 (điều kiện chuẩn). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Giá trị của m là
Câu 24 :
Thủy phân 6,84 gam mantozơ với hiệu suất 60%. Dung dịch thu được sau phản ứng cho tác dụng với dd AgNO3/ NH3 dư. Khối lượng Ag kết tủa là:
Câu 25 :
Aminoaxit X trong phân tử chỉ chứa hai loại nhóm chức. Cho 0,1 mol X tác dụng vừa đủ với 0,2 mol NaOH, thu được 16,3 gam muối. Số nguyên tử hiđro trong phân tử X là
Câu 26 :
Tripeptit X có công thức cấu tạo sau: Lys-Gly-Ala. Khối lượng muối thu được khi thủy phân hoàn toàn 0,15 mol X trong trong dung dịch HCl loãng (vừa đủ) là
Câu 27 :
Chất nào sau đây trùng hợp tạo PVC
Câu 28 :
X là một loại tơ. Một mắt xích cơ bản của X có khối lượng 226u (hay đvC). X có thể là:
Câu 29 :
Đốt cháy hoàn toàn amin X bậc 2 no đơn chức, mạch hở, thu được 0,45 mol H2O và 0,05 mol N2. Công thức phân tử của X là
Câu 30 :
Xà phòng hóa hoàn toàn triglyxerit X trong dung dịch NaOH vừa đủ, thu được glyxerol, natri oleat (a mol) và natri panmitat (2a mol). Phân tử khối của X (theo đvC) là
Câu 31 :
Cho các chất sau: etyl fomat, anilin, glucozo, Gly – Ala. Số chất bị thủy phân trong môi trường kiềm là:
Câu 32 :
Nguyên nhân amin có tính bazơ là :
Câu 33 :
Phản ứng nào dưới đây không thể hiện tính bazơ của amin
Câu 34 :
Chất nào sau đây có thể tham gia phản ứng trùng hợp?
Câu 35 :
Trong môi trường kiềm, tripeptit tác dụng với Cu(OH)2 cho hợp chất màu
Câu 36 :
Có hai loại len có bề ngoài giống nhau, một loại là len lông cừu và một loại len sản xuất từ tơ nhân tạo (có bản chất là xenlulozơ). Cách đơn giản để phân biệt hai loại len trên là
Câu 37 :
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2 thu được 6,384 lít CO2 và 4,77 g H2O. Mặt khác m gam X phản ứng vừa đủ với x gam Brom (trong dung môi CCl4). Biết thể tích các khí đo ở đktc. Giá trị của x là:
Câu 38 :
Cho các phát biểu sau: (1) Khi để rớt H2SO4 đậm đặc vào quần áo bằng vải sợi bông, chỗ vải đó bị đen lại và thủng ngay. (2) Khi nhỏ vài giọt dung dịch HCl đặc vào vải sợi bông, chỗ vải đó dần mủn ra rồi mới bục. (3) Từ xenlulozơ và tinh bột có thể chế tạo thành sợi thiên nhiên và sợi nhân tạo. (4) Khi thuỷ phân hoàn toàn hỗn hợp gồm tinh bột và xenlulozơ trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất. (5) Cả xenlulozơ và tinh bột đều có phản ứng tráng gương. (6) Khi ăn mía ta thường thấy phần gốc ngọt hơn phần ngọn. (7) Trong nhiều loại hạt cây cối thường có nhiều tinh bột. Số phát biểu đúng là
Câu 39 :
Xà phòng hóa hoàn toàn triglixerit X trong dung dịch NaOH dư, thu được glyxerol, natri oleat, natri stearat và natri panmitat. Phân tử khối của X là
Câu 40 :
Phát biểu nào sau đây sai?
Lời giải và đáp án
Câu 1 :
Amin là hợp chất khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3
Đáp án : B Lời giải chi tiết :
Xem lại phần khái niệm amin : Khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon ta được amin.
Câu 2 :
Polime có mạch phân nhánh là
Đáp án : D Lời giải chi tiết :
Polime có mạch phân nhánh là glicogen (xem lại lí thuyết đại cương polime)
Câu 3 :
Đipeptit mạch hở X và tripeptit mạch hở Y đều được tạo ra từ một loại amino axit no, mạch hở có một nhóm NH2 và một nhóm COOH. Đốt cháy hoàn toàn 0,1 mol Y thu được sản phẩm gồm CO2, H2O, và N2 trong đó tổng khối lượng CO2 và H2O bằng 54,9 gam. Nếu đốt cháy hoàn toàn 0,2 mol X, sản phẩm thu được cho lội qua dung dịch nước vôi trong dư thì thu được m gam kết tủa. Giá trị của m là
Đáp án : B Phương pháp giải :
+) Quy đổi Y gồm CONH: 0,1.3 = 0,3 mol; CH2: y mol; H2O: 0,1 mol +) Bảo toàn C: nCO2 = nCONH + nCH2 = 0,3 + y +) Bảo toàn H: nH2O = 0,5.nCONH + nCH2 + nH2O = 0,25 + y Vì Y là tripeptit => số C của a.a tạo ra X và Y = 3 X là đipeptit => số C trong X = 2.3 = 6 Lời giải chi tiết :
Cách 1: Quy đổi Y gồm CONH: 0,1.3 = 0,3 mol; CH2: y mol; H2O: 0,1 mol Bảo toàn C: nCO2 = nCONH + nCH2 = 0,3 + y Bảo toàn H: nH2O = 0,5.nCONH + nCH2 + nH2O = 0,25 + y => mCO2 + mH2O = 44.(0,3 + y) + 18.(0,25 + y) = 54,9 => y = 0,6 => số C trong Y = (0,3 + 0,6) / 0,1 = 9 Vì Y là tripeptit => số C của a.a tạo ra X và Y = 3 X là đipeptit => số C trong X = 2.3 = 6 => nCO2 = 6.nX = 6.0,2 = 1,2 mol => nCaCO3 = 1,2 mol => m = 120 gam
Câu 4 :
Chất nào sau đây không có nhóm –OH hemiaxetal ?
Đáp án : A Lời giải chi tiết :
Saccarozơ bị khóa bởi liên kết 1, 2 - glicozit. Do vậy không còn nhóm –OH hemiaxetal.
Câu 5 :
Amin X có công thức đơn giản nhất là CH5N. Công thức phân tử của X là :
Đáp án : D Lời giải chi tiết :
CTĐGN CH5N → CTCT: (CH5N)n hay CnH5nNn → 5n ≤ 2n + 3 → n = 1
Câu 6 :
Cho sơ đồ chuyển hóa sau: C3H4O2 + NaOH → X + Y X + H2SO4 loãng → Z + T Biết Y và Z đều có phản ứng tráng gương. Hai chất Y, Z tương ứng là
Đáp án : C Phương pháp giải :
- Xem lại các phản ứng thường gặp của este và điều chế este - Viết các phản ứng theo sơ đồ để xác định các chất Lời giải chi tiết :
${C_3}{H_4}{O_2}:{\text{ }}HCOOCH{\text{ }} = {\text{ }}C{H_2}$ $HCOOCH{\text{ }} = {\text{ }}C{H_2} + NaOH\xrightarrow{{}}HCOONa + C{H_3}CHO$ $\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(X)\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(Y)$ $HCOONa + {H_2}S{O_4}{\,_{loang}}\xrightarrow{{}}HCOOH + N{a_2}S{O_4}$ $\,\,\,\,\,\,\,\,(X)\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(Z)\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(T)$
Câu 7 :
Khi thủy phân hoàn toàn 65 gam một oligopeptit X thu được 22,25 gam alanin và 56,25 gam glyxin. X thuộc loại nào?
Đáp án : B Phương pháp giải :
+) nAla = 22,25 / 89 = 0,25 mol; nGly = 56,25 / 75 = 0,75 mol → trong X có tỉ lệ Ala : Gly là 1 : 3 +) X có dạng (Ala)a(Gly)3a → MX = 89a + 75.3a – (4a – 1).18 +) Bảo toàn mắt xích Ala : nX = nAla / a = 0,25 / a Lời giải chi tiết :
nAla = 22,25 / 89 = 0,25 mol; nGly = 56,25 / 75 = 0,75 mol → trong X có tỉ lệ Ala : Gly là 1 : 3 X có dạng (Ala)a(Gly)3a → MX = 89a + 75.3a – (4a – 1).18 = 242a + 18 Bảo toàn mắt xích Ala : nX = nAla / a = 0,25 / a \(\begin{gathered}\to \,\,{M_X} = \dfrac{{65}}{{\dfrac{{0,25}}{a}}} = 260a = 242a + 18 \hfill \\\to a = 1 \hfill \\\end{gathered} \) → X thuộc loại tetrapeptit
Câu 8 :
Đốt cháy hoàn toàn 0,5 mol hỗn hợp X gồm 2 chất H2NR(COOH)x và CnH2n+1COOH, thu được 52,8 gam CO2 và 24,3 gam H2O. Mặt khác, 0,1 mol X phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
Đáp án : D Phương pháp giải :
nH2O > nCO2 → amino axit là no, đơn chức (vì axit có nCO2 = nH2O) Đặt công thức chung là amino axit là CmH2m+1O2N CmH2m+1O2N + xO2 → mCO2 + (2m+1)/2 H2O a mol ma (2m+1)a/2 => 2(nH2O – nCO2) = (2m+1)a – 2ma = a => Số mol amino axit là: naa = 2.(1,35 – 1,2) = 0,3 mol => chiếm 3/5 số mol hỗn hợp Với 0,1 mol X phản ứng thì có 0,06 mol amino axit nHCl = naminoaxit Lời giải chi tiết :
nH2O = 1,35 mol > nCO2 = 1,2 mol → amino axit là no, có 1 nhóm COOH, 1 nhóm NH2 (vì axit có nCO2 = nH2O) Đặt công thức chung là amino axit là CmH2m+1O2N Phương trình đốt cháy: CmH2m+1O2N + xO2 → mCO2 + (2m+1)/2 H2O a mol ma (2m+1)a/2 => 2.(nH2O – nCO2) = (2m + 1).a – 2ma = a => Số mol amino axit là: naa = 2.(1,35 – 1,2) = 0,3 mol => chiếm 3/5 số mol hỗn hợp => Với 0,1 mol X phản ứng thì có 0,06 mol amino axit => nHCl = 0,06 mol Chú ý
+ nhầm lẫn không đổi số mol X, lấy luôn 0,3 mol amino axit tác dụng với HCl (chọn nhầm đáp án B)
Câu 9 :
Amin nào sau đây tồn tại ở trạng thái khí ở điều kiện thường ?
Đáp án : D Lời giải chi tiết :
Metyl-, đimetyl-, trimetyl- và etylamin là những chất khí ở điều kiện thường (4 amin đầu dãy)
Câu 10 :
Tính chất của glucozơ là : kết tinh (1), có vị ngọt (2), thủy phân trong nước (3), thể hiện tính chất của poliancol (4), thể hiện tính chất của axit (5), thể hiện tính chất của anđehit (6), thể hiện tính chất của ete (7). Những tính chất đúng là :
Đáp án : A Lời giải chi tiết :
Glucozơ là monnosaccarit do vậy không có phản ứng thủy phân
Câu 11 :
Đốt cháy hoàn toàn 2,01 gam hỗn hợp X gồm axit acrylic, vinyl axetat, metyl metacrylat. Toàn bộ sản phẩm cháy cho qua dung dịch Ca(OH)2 dư, sau phản ứng thu được 9 gam kết tủa và dung dịch X. Vậy khối lượng dung dịch X đã thay đổi so với dung dịch Ca(OH)2 ban đầu là:
Đáp án : A Phương pháp giải :
- Tính số mol hỗn hợp X Qui đổi hỗn hợp thành CnH2n-2O2 $\begin{array}{*{20}{l}}{{n_{C{O_2}}}{\rm{ }} = {\rm{ }}{n_{CaC{O_3}}}}\\{BTNT{\rm{ }}C:{n_X} = \frac{{{n_{C{O_2}}}}}{n}}\end{array}$ - Tính n - Kết luận sự thay đổi khối lượng dung dịch: +) Tính $\Sigma \left( {{m}_{C{{O}_{2}}}}+{{m}_{{{H}_{2}}O}} \right)$ +) ∆mdd sau pư =$\left( {{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}} \right)$ – (m kết tủa + m khí (nếu có)) · ∆mdd sau pư > 0 → khối lượng dung dịch sau phản ứng tăng
· ∆mdd sau pư < 0 → khối lượng dung dịch sau phản ứng giảm Lời giải chi tiết :
Các chất trong hỗn hợp đều chứa 2 liên kết pi và 2 nguyên tử oxi. \(\left. \begin{array}{l}axit{\rm{ }}acrylic:C{H_2} = CH - COOH\\vinyl{\rm{ }}axetat:C{H_3}COOCH = C{H_2}\\metyl{\rm{ }}metacrylat:C{H_2} = C(C{H_3})C{\rm{O}}O - C{H_3}\end{array} \right\rangle = > X:{C_n}{H_{2n - 2}}{O_2}\) \({{C}_{n}}{{H}_{2n-2}}{{O}_{2}}:\dfrac{2,01}{14n+30}\xrightarrow{+{{O}_{2}}}\left\{ \begin{align}& C{{O}_{2}} \\ & {{H}_{2}}O \\ \end{align} \right.\xrightarrow{+\text{dd}\,\,Ca{{(OH)}_{2}}\,\,}9gam\,\,CaC{{O}_{3}}\) \(\begin{array}{l}BTNT\,\,C:{n_{CO2}} = {n_{CaCO3}} = {n_{C(X)}} = \dfrac{9}{{100}} = 0,09mol\\ = > {n_{hhX}} = \dfrac{{0,09}}{n}\\ \dfrac{{0,09}}{n}.(14n + 30) = 2,01 < = > n = 3,6\\X:{C_{3,6}}{H_{5,2}}{O_2}:0,025mol\\ = > {n_{{H_2}O}} = 0,065mol\\ {m_{C{O_2}}} + {m_{{H_2}O}} = 0,09.44 + 0,065.18 = 5,13gam\\{\Delta _{mdd{\rm{ }}sau{\rm{ }}pu}} = {\rm{ }}\left( {{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}} \right){\rm{ }}-{\rm{ m}} \downarrow = 5,13 - 9 = - 3,87gam\end{array}\) ∆mdd sau pư < 0 => Khối lượng dung dịch giảm 3,87gam
Câu 12 :
Hai chất hữu cơ X, Y là đồng phân của nhau và có công thức phân tử là C3H7O2N. X tác dụng với NaOH thu được muối X1 có công thức phân tử là C2H4O2NNa ; Y tác dụng với NaOH thu được muối Y1 có công thức phân tử là C3H3O2Na. Tìm công thức cấu tạo của X, Y?
Đáp án : B Lời giải chi tiết :
Khi X + NaOH => thay thế 1 gốc CH3 thành 1 gốc Na => X là H2N-CH2-COOCH3 Khi Y + NaOH => thay thế 1 gốc NH4 thành 1 gốc Na => Y là CH3-CH2-COONH4
Câu 13 :
Công thức hóa học nào sau đây là của nước Svayde, dùng để hòa tan xenlulozơ trong quá trình sản xuất tơ nhân tạo ?
Đáp án : A Lời giải chi tiết :
Xenlulozo tan được trong dung dịch Cu(OH)2 trong amoniac có tên là "nước Svayde", trong đó Cu2+ tồn tại chủ yếu ở dạng phức chất Cu(NH3)n(OH)2
Câu 14 :
Hỗn hợp X gồm một ancol và một axit cacboxylic đều no, đơn chức, mạch hở, có cùng số nguyên tử cacbon trong phân tử. Đốt cháy hoàn toàn 51,24 gam X, thu được 101,64 gam CO2. Đun nóng 51,24 gam X với xúc tác H2SO4 đặc, thu được m gam este (hiệu suất phản ứng este hóa bằng 60%). Giá trị m gần nhất với giá trị nào sau đây?
Đáp án : A Phương pháp giải :
S/d CT: nH2O = nCO2 + nancol BTNT O: 2.nO2 + nancol + 2naxit = 2.nCO2 + nH2O => nO2 Bảo toàn khối lượng : mX + mO2 = mCO2 + mH2O Biện luận tìm số nguyên tử cacbon trong axit và ancol. Bước 2: Tính khối lượng este theo hiệu suất \(m\,{\,_{thuc.te}} = m\,{\,_{ly\,thuyet}}.\dfrac{{H\% }}{{100}}\) Lời giải chi tiết :
Gọi số mol ancol và axit lần lượt là x và y Vì 2 chất đều no đơn chức nên khi đốt cháy : nH2O = nCO2 + nancol = 2,31 + x Bảo toàn O : 2.nO2 + nancol + 2naxit = 2.nCO2 + nH2O => nO2= (3,465 – y) mol Bảo toàn khối lượng : mX + mO2 = mCO2 + mH2O => 9x + 16y = 9,45 => 9(x+y) < 9,45 < 16(x+y) => 0,59 < (x + y) < 1,05 Gọi số C trong mỗi chất là n => nCO2 = 2,31 = n.(x + y) => (x + y) = 2,31/n => 2,2 < n < 3,9 =>n = 3 => x = 0,41 ; y = 0,36 mol C2H5COOH + C3H7OH → C2H5COOC3H7 + H2O 0,36 0,41 →0,36 => Tính theo chất phản ứng thiếu (axit) => neste = naxit = 0,36 mol => \(m\,{\,_{thuc.te}} = m\,{\,_{ly\,thuyet}}.\dfrac{{H\% }}{{100}} = 25,056gam\)
Câu 15 :
Cho sơ đồ phản ứng : Thuốc súng không khói $\leftarrow $ X $\to $ Y $\to $ Sobitol Tên gọi X, Y lần lượt là
Đáp án : A Lời giải chi tiết :
Thuốc súng không khói $\xleftarrow{+HN{{O}_{3}};xt:{{H}_{2}}S{{O}_{4}}d}Xenlulozo\xrightarrow{+{{H}_{2}}O,{{H}^{+}},{{t}^{0}}}glucozo\xrightarrow{+{{H}_{2}}}Sobitol$
Câu 16 :
Khi thủy phân HCOOC6H5 trong môi trường kiềm dư thì thu được:
Đáp án : B Lời giải chi tiết :
Este có dạng: R – COO –C6H4– R’ (este của phenol) khi thủy phân thu được 2 muối + H2O
Câu 17 :
Nhận xét nào sau đây không đúng ?
Đáp án : B Lời giải chi tiết :
A. Đúng, Chất béo nhẹ hơn nước và không tan trong nước. B.Sai, Chất béo là trieste của glixerol và các axit béo. C. Đúng, Phản ứng: $\left| \begin{align}& {{({{C}_{17}}{{H}_{33}}COO)}_{3}}{{C}_{3}}{{H}_{5}}+3{{H}_{2}} \\ & {{({{C}_{17}}{{H}_{31}}COO)}_{3}}{{C}_{3}}{{H}_{5}}+6{{H}_{2}} \\ \end{align} \right.\xrightarrow{Ni,{{t}^{o}}}{{({{C}_{17}}{{H}_{35}}COO)}_{3}}{{C}_{3}}{{H}_{5}}$ D. Đúng, Dầu mỡ động thực vật bị ôi thiu do nối đôi C=C ở gốc axitkhông no của chất béo bị oxihóa chậmbởi oxi không khí tạo thành peoxit chất này bị thủy phân thành các sản phẩm có mùi khó chịu
Câu 18 :
Để phản ứng este hóa chuyển dịch ưu tiên theo chiều nghịch, cần dùng các giải pháp nào sau đây?
Đáp án : B Phương pháp giải :
Sử dụng nguyên lí chuyển dịch cân bằng Lơ Sa-tơ-li-e: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó. Lời giải chi tiết :
\(RCOOH + R'OHRCOOR' + {H_2}O\) A: H2SO4 đặc hút nước (mất nước) làm cân bằng chuyển dịch theo chiều tạo ra nước – chiều thuận. B: Tăng nồng độ este bằng cách cho thêm este – chiều nghịch C: Tăng nồng độ axit hoặc ancol => cân bằng chuyển dịch theo chiều làm giảm nồng độ của chúng – chiều thuận D: Tăng áp suất của hệ cân bằng không chuyển dịch
Câu 19 :
Để phản ứng hết với một lượng hỗn hợp gồm 2 chất hữu cơ X và Y ( MX < MY) càn vừa đủ 100 ml dung dịch NaOH 1,5M. Sau khi phản ứng xảy ra hoàn toàn thu được 10,2 gam muối của môt axit hữu cơ và m gam một ancol. Đốt cháy hoàn toàn lượng ancol trên thu được 1,12 lít khí CO2 (đktc) và 1,8 gam nước. Công thức của X là
Đáp án : C Phương pháp giải :
nCO2 < nH2O → ancol no hở, đơn chức => n ancol = nH2O-nCO2 =>C=nCO2 : nancol => ancol Vì nNaOH > nCH4O X là axit còn Y là este tạo bởi CH3OH và axit X nRCOONa = nNaOH => CT muối Lời giải chi tiết :
nCO2 < nH2O → ancol no hở, đơn chức => n ancol = nH2O-nCO2 = 0,05 =>C=nCO2 : nancol = 1 => ancol là CH4O Vì nNaOH > nCH4O X là axit còn Y là este tạo bởi CH3OH và axit X nRCOONa = nNaOH = 0,15 → M = 68 → MR=1 → HCOONa
Câu 20 :
Cho các đồng phân của amin bậc 1 của C3H9N tác dụng với dung dịch HCl thì có thể tạo ra tối đa bao nhiêu muối?
Đáp án : B Phương pháp giải :
Viết các đồng phân amin bậc I Bản chất của phản ứng là nhóm chức amin phản ứng với ion H+ tạo ra muối amoni –NH2 + \({H^ + }\)\( \to \)\( - N{H_3}^ + \)(Phản ứng xảy ra tương tự với amin bậc 2 và bậc 3). Lời giải chi tiết :
C3H9N có các đồng phân amin bậc I là CH3-CH2-CH2NH2 CH3-CH(NH2)-CH3 Mỗi đồng phân tác dụng với dung dịch HCl tạo ra 1 muối → có thể tạo ra tối đa 2 muối
Câu 21 :
Cho các phát biểu sau:
Số phát biểu đúng là?
Đáp án : B Lời giải chi tiết :
1 sai vì Aminoaxit là những chất rắn, kết tinh, tan tốt trong nước và có vị ngọt. 2 sai vì Cách gọi tên bán hệ thống : axit + vị trí chữ cái Hi Lạp (α, β, γ, δ, ε, ω) + amino + tên thường của axit cacboxylic tương ứng. 3 đúng 4 đúng
Câu 22 :
Cho các chất sau: HCl, FeCl2, NaNO2/HCl, Br2. Số chất chất tác dụng với metylamin là?
Đáp án : C Lời giải chi tiết :
Metylamin tác dụng được với HCl, FeCl2, NaNO2/HCl.
Câu 23 :
Đốt cháy hoàn toàn một hỗn hợp X (glucozơ, fructozơ, metanal và etanoic) cần 22,4 lít O2 (điều kiện chuẩn). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Giá trị của m là
Đáp án : A Phương pháp giải :
+Quy đổi các chất thành CTTQ: Cn(H2O)m \(\begin{array}{*{20}{l}}{ + {\rm{ }}{n_{{O_2}}}\;{\rm{ }} = {\rm{ }}{n_{C{O_2}}}}\\{ + {\rm{ }}BTNT{\rm{ }}C{\rm{ }}:{\rm{ }}{n_{CaC{O_3}}} = {\rm{ }}{n_{C{O_2}}}}\end{array}\) Lời giải chi tiết :
- Glucozơ và fructozơ đều có CTPT: C6H12O6 Metanal: CH2O Etanoic: C2H4O2 Tất cả các chất trên đều có dạng CTTQ chung: Cn(H2O)n \(\begin{array}{*{20}{l}}{ - {\rm{ }}{n_{{O_2}}}\;{\rm{ }} = {\rm{ }}{n_{C{O_2}}} = \frac{{22,4}}{{22,4}} = 1mol}\\\begin{array}{l} - {\rm{ }}BTNT{\rm{ }}C{\rm{ }}:{\rm{ }}{n_{CaC{O_3}}} = {\rm{ }}{n_{C{O_2}}} = 1mol\\ = > {m_{CaC{O_3}}} = 100g\end{array}\end{array}\)
Câu 24 :
Thủy phân 6,84 gam mantozơ với hiệu suất 60%. Dung dịch thu được sau phản ứng cho tác dụng với dd AgNO3/ NH3 dư. Khối lượng Ag kết tủa là:
Đáp án : B Phương pháp giải :
\( + H\% = \dfrac{{{m_{thuc\,te}}}}{{{m_{ly\,thuyet}}}}.100\% = \dfrac{{{n_{thuc\,te}}}}{{{n_{ly\,thuyet}}}}.100\% \) + nAg = 2nglu (thu được) + 2nman dư Lời giải chi tiết :
nman = 6,84 : 342 = 0,02 (mol) => nglu (lí thuyết) = 2nman = 0,04 (mol). \(H\% = \dfrac{{{n_{thuc\,te}}}}{{{n_{ly\,thuyet}}}}.100\% = > {n_{glu\,thuc\,te}} = 0,04.\,60\% = 0,024mol\) nman dư = 0,02 – 0,012 = 0,008 (mol) nAg = 2nglu (thu được)+ 2nman dư = 0,064 (mol) => mAg = 0,064 . 108 = 6,912 (g) Chú ý
Sai lầm cần chú ý: Học sinh quên mất mantozo có tráng gương => nAg = 2nGlu thực tế = 0,04mol => Đáp án A
Câu 25 :
Aminoaxit X trong phân tử chỉ chứa hai loại nhóm chức. Cho 0,1 mol X tác dụng vừa đủ với 0,2 mol NaOH, thu được 16,3 gam muối. Số nguyên tử hiđro trong phân tử X là
Đáp án : D Phương pháp giải :
X tác dụng với NaOH theo tỉ lệ 1 : 2 → X có dạng (NH2)xR(COOH)2 nmuối = naa Maa + 22.2= Mmuối Lời giải chi tiết :
X tác dụng với NaOH theo tỉ lệ 1 : 2 → X có dạng (NH2)xR(COOH)2 nmuối = naa = 0,1 mol → Mmuối = 163 Maa + 22.2= Mmuối→ Maa = 163 – 44 = 119 → 16x + R = 29 → x = 1 và R = 13 (CH) R là H2N-CH(COOH)2→ trong R có 5H
Câu 26 :
Tripeptit X có công thức cấu tạo sau: Lys-Gly-Ala. Khối lượng muối thu được khi thủy phân hoàn toàn 0,15 mol X trong trong dung dịch HCl loãng (vừa đủ) là
Đáp án : B Phương pháp giải :
+) MLys-Gly-Ala = 146 + 75 + 89 – 2.18 +) Lys-Gly-Ala + 2H2O + 4HCl→ hỗn hợp muối +) BTKL : mmuối = mX + mH2O + mHCl Lời giải chi tiết :
MLys-Gly-Ala = 146 + 75 + 89 – 2.18 = 274 Lys-Gly-Ala + 2H2O + 4HCl → hỗn hợp muối BTKL : mmuối = mX + mH2O + mHCl = 0,15.274 + 2.0,15.18 + 4.0,15.36,5 = 68,4 gam
Câu 27 :
Chất nào sau đây trùng hợp tạo PVC
Đáp án : A Phương pháp giải :
Xem lại bài polime SGK hóa 12 Lời giải chi tiết :
PVC là poli vinyl clorua được tạo thành từ phản ứn trùng hợp vinyl clorua CH2=CHCl
Câu 28 :
X là một loại tơ. Một mắt xích cơ bản của X có khối lượng 226u (hay đvC). X có thể là:
Đáp án : B Phương pháp giải :
Xem lại CTPT của các tơ và tính phân tử khối của chúng Lời giải chi tiết :
Xét các phương án A. Tơ nitron(hay olon) có CT là (-CH2=CHCN-)n → M = 53u B. Tơ nilon – 6,6 có CT là –( OC – (CH2)4 – CONH – (CH2)6 – NH)-n → M = 226u C. Xenlulozo triaxetat có CT là [C6H7O2(OCOCH3)3]n → M = 288 u D. Poli metyl metacrylat có CT là
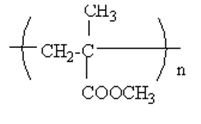 → M = 100u
Câu 29 :
Đốt cháy hoàn toàn amin X bậc 2 no đơn chức, mạch hở, thu được 0,45 mol H2O và 0,05 mol N2. Công thức phân tử của X là
Đáp án : C Phương pháp giải :
Bào toàn nguyên tố N có nX = 2nN2 CTPT của X có dạng CnH2n+3N : 0,1 mol → n Lời giải chi tiết :
Ta có nX = 2nN2 (vì X là amin đơn chức) → nX = 0,1 mol X có số H = 2nH2O : nX = 2.0,45 : 0,1 = 9 Vì X là amin no bậc 2 đơn chức nên X có CTPT dạng CnH2n+3N → 2n + 3 = 9 → n = 3 X là C3H9N
Câu 30 :
Xà phòng hóa hoàn toàn triglyxerit X trong dung dịch NaOH vừa đủ, thu được glyxerol, natri oleat (a mol) và natri panmitat (2a mol). Phân tử khối của X (theo đvC) là
Đáp án : A Phương pháp giải :
X được tạo bởi 1 gốc axit C17H35COOH và 2 gốc axit C15H31COOH với glixerol. Từ đó viết CTCT của X và tính được phân tử khối Lời giải chi tiết :
triglyxerit X + 3NaOH → C17H33COONa + C15H31COONa + C3H5(OH)3 a (mol) a (mol) 2a (mol) => X được tạo bởi 1 gốc axit C17H33COOH và 2 gốc axit C15H31COOH với glixerol => Phân tử khối của X là 832
Câu 31 :
Cho các chất sau: etyl fomat, anilin, glucozo, Gly – Ala. Số chất bị thủy phân trong môi trường kiềm là:
Đáp án : B Phương pháp giải :
Chất bị thủy phân trong môi trường kiềm là những chất tác dụng với dung dịch kiềm như : este, peptit, axit, phenol Lời giải chi tiết :
Chất bị thủy phân trong môi trường kiềm là: etyl fomat, Gly – Ala
Câu 32 :
Nguyên nhân amin có tính bazơ là :
Đáp án : B Lời giải chi tiết :
Trên nguyên tử N của amin và amoniac đều có chứa đôi e, nên dễ dàng nhận H+
Câu 33 :
Phản ứng nào dưới đây không thể hiện tính bazơ của amin
Đáp án : C Phương pháp giải :
Tính bazơ của amin thể hiện ở khả năng tác dụng với axit, phản ứng thủy phân trong nước hay dung dịch muối có tính axit Lời giải chi tiết :
Đáp án A, B, D đều là phản ứng thể hiện tính bazơ của amin Chỉ có đáp án C là phản ứng oxi hóa - khử, không phải là phản ứng axit - bazơ
Câu 34 :
Chất nào sau đây có thể tham gia phản ứng trùng hợp?
Đáp án : A Lời giải chi tiết :
Chất hữu cơ có khả năng tham gia phản ứng trùng hợp là chất có chứa liên kết pi hoặc vòng kém bền trong CTCT
Câu 35 :
Trong môi trường kiềm, tripeptit tác dụng với Cu(OH)2 cho hợp chất màu
Đáp án : A Phương pháp giải :
Dựa vào tính chất hóa học của các peptit: Các tripeptit trở lên tác dụng với Cu(OH)2 cho hợp chất màu tím (phản ứng màu biure). Lời giải chi tiết :
Trong môi trường kiềm, tripeptit tác dụng với Cu(OH)2 cho hợp chất màu tím.
Câu 36 :
Có hai loại len có bề ngoài giống nhau, một loại là len lông cừu và một loại len sản xuất từ tơ nhân tạo (có bản chất là xenlulozơ). Cách đơn giản để phân biệt hai loại len trên là
Đáp án : C Lời giải chi tiết :
Len lông cừu có bản chất protein nên khi đốt cháy có mùi khét. Sợi xenlulozơ khi cháy không tạo ra mùi khét. Vì vậy đốt cháy hai loại sợi len đó, có thể phân biệt được chúng.
Câu 37 :
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2 thu được 6,384 lít CO2 và 4,77 g H2O. Mặt khác m gam X phản ứng vừa đủ với x gam Brom (trong dung môi CCl4). Biết thể tích các khí đo ở đktc. Giá trị của x là:
Đáp án : A Phương pháp giải :
- Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) => nX - Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k => số mol Br2 => x Lời giải chi tiết :
- Gọi công thức của X là (RCOO)3C3H5 có k liên kết pi nO2 = 9,016 : 22,4 = 0,4025 mol ; nCO2 = 6,384 : 22,4 = 0,285 mol ; nH2O = 0,265 mol Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) = 0,03 mol = 6n(X) => nX = 0,005 mol Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k = 5 Có 3 pi trong 3 gốc COO => 2 pi còn lại sẽ nằm trong gốc hidrocacbon (Có thể phản ứng được với Br2/CCl4) => nBr2 = 2.nX = 2.0,005 = 0,01 mol => mBr2 = x = 0,01.160 = 1,6g
Câu 38 :
Cho các phát biểu sau: (1) Khi để rớt H2SO4 đậm đặc vào quần áo bằng vải sợi bông, chỗ vải đó bị đen lại và thủng ngay. (2) Khi nhỏ vài giọt dung dịch HCl đặc vào vải sợi bông, chỗ vải đó dần mủn ra rồi mới bục. (3) Từ xenlulozơ và tinh bột có thể chế tạo thành sợi thiên nhiên và sợi nhân tạo. (4) Khi thuỷ phân hoàn toàn hỗn hợp gồm tinh bột và xenlulozơ trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất. (5) Cả xenlulozơ và tinh bột đều có phản ứng tráng gương. (6) Khi ăn mía ta thường thấy phần gốc ngọt hơn phần ngọn. (7) Trong nhiều loại hạt cây cối thường có nhiều tinh bột. Số phát biểu đúng là
Đáp án : A Lời giải chi tiết :
Trong các phát biểu đã cho, có phát biểu đúng: (1), (2), (4), (6), (7). (1) và (2) đúng. Khi để rớt H2SO4 đậm đặc vào quần áo bằng vải sợi bông (có thành phần là xenlulozơ), chỗ vải đó bị đen lại và thủng ngay là do H2SO4 đặc có tính háo nước và làm xenlulozơ bị than hóa. Còn khi rớt HCl vào vải sợi bông, xenlulozơ bị thủy phân dưới xúc tác axit vô cơ nên dần mủn ra sau đó mới bị bục. (3) sai. Tinh bột không dùng để chế tạo sợi thiên nhiên và nhân tạo. (4) đúng. Khi thủy phân hỗn hợp tinh bột và xenlulozơ trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất là glucozơ. (5) sai. Trong phân tử của tinh bột và xenlulozơ không có nhóm –CHO (hoặc nhóm có thể chuyển hóa thành nhóm –CHO trong môi trường kiềm) nên tinh bột và xenlulozơ không tham gia phản ứng tráng bạc. (6) đúng. (7) đúng. Tinh bột có rất nhiều trong các loại hạt (gạo, mì, ngô, ...), củ, quả. Tinh bột chứa trong hạt là nguồn dự trữ nguyên liệu và năng lượng cho hạt nảy mầm thành cây con.
Câu 39 :
Xà phòng hóa hoàn toàn triglixerit X trong dung dịch NaOH dư, thu được glyxerol, natri oleat, natri stearat và natri panmitat. Phân tử khối của X là
Đáp án : D Phương pháp giải :
Xác định các gốc axit trong chất béo, xây dựng công thức và kết luận. Lời giải chi tiết :
X là (C17H33COO)(C17H35COO)(C15H31COO)C3H5 → MX = 860
Câu 40 :
Phát biểu nào sau đây sai?
Đáp án : A Phương pháp giải :
Dựa vào tính chất vật lí, tính chất hóa học và công thức chung của chất béo, este để chọn phát biểu sai. Lời giải chi tiết :
Phát biểu A sai vì sản phẩm của phản ứng xà phòng hoá chất béo là muối của axit béo và glixerol. Phát biểu B đúng vì ancol có liên kết hidro nên có nhiệt độ sôi cao hơn rất nhiều este có cùng phân tử khối. Phát biểu C đúng vì trong công nghiệp có thể chuyển hoá chất béo lỏng thành chất béo rắn bằng phản ứng hiđro hóa. Phát biểu D đúng vì công thức chung của este là CnH2n+2-2kO2m nên số nguyên tử hiđro trong phân tử este đơn và đa chức luôn là một số chẵn. |



















Danh sách bình luận