Đề thi giữa kì 2 Hóa 11 Chân trời sáng tạo - Đề số 4Tổng hợp đề thi học kì 2 lớp 11 tất cả các môn - Chân trời sáng tạo Toán - Văn - Anh - Lí - Hóa - Sinh Alkane (CH3)2CH–CH3 có tên theo danh pháp thay thế làĐề bài
Câu 1 :
Alkane (CH3)2CH–CH3 có tên theo danh pháp thay thế là
Câu 2 :
Hiện nay, nhiều nơi ở nông thôn đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
Câu 4 :
Tên thay thế của hydrocarbon có công thức cấu tạo (CH3)3CCH2CH2CH3 là
Câu 5 :
Tên thay thế của (CH3)3C–CH2–CH(CH3)2 là
Câu 6 :
Khi thế chlorine (1:1) vào phân tử 2 – methylbutane thì sản phẩm thu được nhiều nhất là
Câu 7 :
Cracking hoàn toàn một alkane thu được hỗn hợp khí có tỉ khối so với He bằng 9. CTPT của alkane đó là
Câu 8 :
Sản phẩm chính của phản ứng cộng hợp nước vào 2-methylpropene là
Câu 9 :
Cho alkyne A tác dụng với H2 dư trên xúc tác Ni/to. Sau khi phản ứng xảy ra hoàn toàn thu được một sản phẩm hữu cơ duy nhất là pentane. Khi A tác dụng với H2, Lindlar thì thu được alkene C có đồng phân hình học. Tên gọi của A là
Câu 10 :
Cho 3-methylbut-1-yne tác dụng với H2 (xúc tác Lindlar) tới khi phản ứng hoàn toàn thu được hỗn hợp Y chỉ có hai hydrocarbon. Công thức cấu tạo của hai hydrocarbon lần lượt là:
Câu 11 :
Công thức cấu tạo của 4-methylpent-2-yne là
Câu 12 :
Alkene X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên gọi của X theo danh pháp thay thế là
Câu 13 :
Cho 0,25mol alkane A phản ứng với bromine thu được duy nhất 37,75gam dẫn xuất bromine B. Tên gọi của A theo danh pháp IUPAC là
Câu 14 :
Đốt cháy hoàn toàn hỗn hợp X gồm hai alkane kế tiếp trong dãy đồng đẳng, thu được 24,2 gam CO2 và 12,6 gam H2O. Công thức phân tử 2 alkane là :
Câu 15 :
Để phân biệt but-2-yne (CH3C≡CCH3) với but-l-yne (CH≡CCH2CH3) có thể dùng thuốc thử nào sau đây?
Câu 16 :
Cho các alkene: CH2=CH-CH3 (X); CH3-CH=CH-CH3 (Y); (CH3)2C=CH2 (Z). Alkene nào có đồng phân hình học?
Câu 17 :
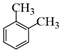
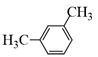
Hợp chất nào sau đây là m-xylene?
Câu 19 :
Cho phản ứng: C6H5-CH=CH2 + KMnO4 → C6H5-COOK + K2CO3 + MnO2 + KOH + H2O Tổng hệ số (nguyên, tối giản) tất cả các chất trong phương trình hóa học của phản ứng trên là
Câu 20 :
Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là
Câu 21 :
Cho dẫn xuất halogen có công thức cấu tạo sau: Danh pháp thay thế của dẫn xuất halogen trên là
Câu 22 :
Cho các thí nghiệm: (a) Đun nóng C6H5CH2Cl trong dung dịch NaOH (b) Đung nóng hỗn hợp CH3CH2CH2Cl, KOH và C2H5OH (c) Đun nóng CH3CH2CH2Cl trong dung dịch NaOH (d) Đun nóng hỗn hợp CH3CHClCH=CH2, KOH và C2H5OH Có bao nhiêu thí nghiệm tạo sản phẩm chính là alcohol?
Câu 23 :
Bình “ga” sử dụng trong hộ gia đình Y có chứa 10,92 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 3 : 4. Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Trung bình, lượng nhiệt tiêu thụ từ’ đốt khí “ga” của hộ gia đình Y tương ứng với bao nhiêu số điện? (Biết hiệu suất sử dụng nhiệt là 50% và 1 số điện = 1 kWh = 3600 kJ)
Câu 25 :
Cho 8,0 gam hỗn hợp X gồm acetylene và ethylene (tỉ lệ mol 2 : 1) lội qua dung dịch nước bromine dư thấy có m gam phản ứng. Giá trị của m là
Lời giải và đáp án
Câu 1 :
Alkane (CH3)2CH–CH3 có tên theo danh pháp thay thế là
Đáp án : A Phương pháp giải :
Dựa vào quy tắc đọc tên của alkane Lời giải chi tiết :
(CH3)2CH–CH3: 2 – methylpropane Đáp án A
Câu 2 :
Hiện nay, nhiều nơi ở nông thôn đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
Đáp án : B Phương pháp giải :
Dựa vào ứng dụng của alkane Lời giải chi tiết :
Các hầm biogas có chứa CH4 là chất dễ cháy sử dụng cho việc cung cấp nhiên liệu việc đun nấu Đáp án B
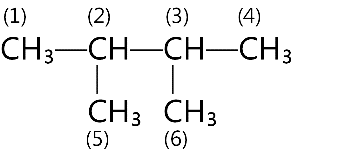
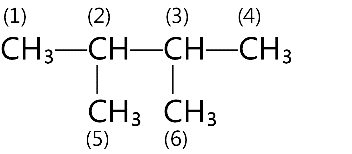
Đáp án : C Phương pháp giải :
Xác định trục đối xứng của alkane Lời giải chi tiết :
Vậy ta có: (1), (4) giống nhau, (5), (6) giống nhau 1, 4, 5, 6 giống nhau; 2 và 3 giống nhau.
Câu 4 :
Tên thay thế của hydrocarbon có công thức cấu tạo (CH3)3CCH2CH2CH3 là
Đáp án : A Phương pháp giải :
Dựa vào quy tắc đọc tên của alkane Lời giải chi tiết :
(CH3)3CCH2CH2CH3: 2,2 – dimethylpentane Đáp án A
Câu 5 :
Tên thay thế của (CH3)3C–CH2–CH(CH3)2 là
Đáp án : C Phương pháp giải :
Dựa vào quy tắc đọc tên của alkane Lời giải chi tiết :
(CH3)3C–CH2–CH(CH3)2: 2,2,4 – trimethylpentane Đáp án C
Câu 6 :
Khi thế chlorine (1:1) vào phân tử 2 – methylbutane thì sản phẩm thu được nhiều nhất là
Đáp án : A Phương pháp giải :
Cl2 ưu tiên thế H ở carbon bậc cao Lời giải chi tiết :
Đáp án A
Câu 7 :
Cracking hoàn toàn một alkane thu được hỗn hợp khí có tỉ khối so với He bằng 9. CTPT của alkane đó là
Đáp án : C Phương pháp giải :
Phản ứng cracking là phản ứng bẻ gãy mạch carbon thành các alkene và alkane tương ứng Lời giải chi tiết :
M hỗn hợp khí = 9.4 = 36 Giả sử có 1 mol alkane => n khí tăng = n alkane cracking = 1 mol => n hỗn hợp khí = 2 mol => M alkane = 2.36 = 72 => CTPT: C5H12
Câu 8 :
Sản phẩm chính của phản ứng cộng hợp nước vào 2-methylpropene là
Đáp án : A Phương pháp giải :
Dựa vào quy tắc cộng Markovikop Lời giải chi tiết :
Đáp án A
Câu 9 :
Cho alkyne A tác dụng với H2 dư trên xúc tác Ni/to. Sau khi phản ứng xảy ra hoàn toàn thu được một sản phẩm hữu cơ duy nhất là pentane. Khi A tác dụng với H2, Lindlar thì thu được alkene C có đồng phân hình học. Tên gọi của A là
Đáp án : A Phương pháp giải :
Dựa vào tính chất hóa học của alkyne Lời giải chi tiết :
Alkyne A tác dụng hoàn toàn với H2 dư xác tác Ni/t thu được pentane => Alkyne có 5C Alkyne A tác dụng với H2, xúc tác lindlar thu được alkene có đồng phân hình học => alkene có 5C và có đồng phân hình học => Công thức của alkene: H3C – CH = CH – CH2 – CH3 => Công thức alkyne: H3C – C \( \equiv \)C – CH2 – CH3 Đáp án A
Câu 10 :
Cho 3-methylbut-1-yne tác dụng với H2 (xúc tác Lindlar) tới khi phản ứng hoàn toàn thu được hỗn hợp Y chỉ có hai hydrocarbon. Công thức cấu tạo của hai hydrocarbon lần lượt là:
Đáp án : C Phương pháp giải :
Dựa vào tính chất hóa học của alkyne Lời giải chi tiết :
Vì phản ứng thu được 2 hydrocarbon => alkyne còn dư Đáp án C
Câu 11 :
Công thức cấu tạo của 4-methylpent-2-yne là
Đáp án : B Phương pháp giải :
Dựa vào tên gọi của công thức cấu tạo Lời giải chi tiết :
4 – methylpent – 2 – yne: (CH3)2CH-C≡CH-CH3 Đáp án B
Câu 12 :
Alkene X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên gọi của X theo danh pháp thay thế là
Đáp án : C Phương pháp giải :
Dựa vào quy tắc đọc tên của alkene Lời giải chi tiết :
CH3–CH2–C(CH3)=CH–CH3: 3 – methylpent – 2 – ene Đáp án C
Câu 13 :
Cho 0,25mol alkane A phản ứng với bromine thu được duy nhất 37,75gam dẫn xuất bromine B. Tên gọi của A theo danh pháp IUPAC là
Đáp án : A Phương pháp giải :
Dựa vào tính chất hóa học của alkane Lời giải chi tiết :
n alkane = n dẫn xuất = 0,25 mol => M dẫn xuất = 37,75 : 0,25 = 151 Gọi CTTQ của dẫn xuất là: CnH2n+1Br M CnH2n+1Br = 151 => n = 5 => alkane A có CTPT: C5H12 Vì chỉ thu được 1 sản phẩm duy nhất => CTCT A: 2,2 - dimethylpropane Đáp án A
Câu 14 :
Đốt cháy hoàn toàn hỗn hợp X gồm hai alkane kế tiếp trong dãy đồng đẳng, thu được 24,2 gam CO2 và 12,6 gam H2O. Công thức phân tử 2 alkane là :
Đáp án : C Phương pháp giải :
Dựa vào phản ứng đốt cháy của alkane Lời giải chi tiết :
n CO2 = 24,2 : 44 = 0,55 mol; n H2O = 12,6 : 18 = 0,7 mol => n alkane = n H2O – n CO2 = 0,7 – 0,55 = 0,15 mol Số C trung bình = 0,55 : 0,15 = 3,67 => Hỗn hợp X gồm: C3H8 và C4H10 Đáp án C
Câu 15 :
Để phân biệt but-2-yne (CH3C≡CCH3) với but-l-yne (CH≡CCH2CH3) có thể dùng thuốc thử nào sau đây?
Đáp án : B Phương pháp giải :
Dựa vào phản ứng đặc trưng của alk – 1 – yne Lời giải chi tiết :
Dùng dung dịch AgNO3/NH3 phân biệt được but – 1 – yne tạo kết tủa vàng vì but – 2 – yne không phản ứng Đáp án B
Câu 16 :
Cho các alkene: CH2=CH-CH3 (X); CH3-CH=CH-CH3 (Y); (CH3)2C=CH2 (Z). Alkene nào có đồng phân hình học?
Đáp án : C Phương pháp giải :
Dựa vào đặc điểm của đồng phân hình học Lời giải chi tiết :
(Y) có đồng phân hình học Đáp án C
Câu 17 :
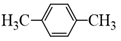
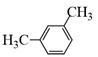
Hợp chất nào sau đây là m-xylene?
Đáp án : B Phương pháp giải :
Dựa vào cách đọc tên của arene Lời giải chi tiết :
m – xylene: Đáp án B
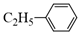
Đáp án : B Phương pháp giải :
Dựa vào quy tắc đọc tên của arene Lời giải chi tiết :
Câu 19 :
Cho phản ứng: C6H5-CH=CH2 + KMnO4 → C6H5-COOK + K2CO3 + MnO2 + KOH + H2O Tổng hệ số (nguyên, tối giản) tất cả các chất trong phương trình hóa học của phản ứng trên là
Đáp án : D Phương pháp giải :
Dựa vào phương pháp thăng bằng electron Lời giải chi tiết :
\(\begin{array}{l}\mathop C\limits^{ - 1} H = \mathop C\limits^{ - 2} {H_2} \to \mathop C\limits^{ + 3} OOK + {K_2}\mathop C\limits^{ + 4} {O_3} + 10e|x3\\\mathop {Mn}\limits^{ + 7} + 3e \to \mathop {Mn}\limits^{ + 4} |x10\end{array}\) 3C6H5 – CH = CH2 + 10KMnO4 \( \to \)3C6H5COOK + 3K2CO3 + 10MnO2 + KOH + 4H2O Tổng hệ số tất cả chất trong phương trình hóa học: 3 + 10 + 3 + 3 + 10 + 1 + 4 = 34 Đáp án D
Câu 20 :
Dẫn xuất halogen bậc II có tên và công thức cấu tạo phù hợp là
Đáp án : B Phương pháp giải :
Dẫn xuất halogen bậc II khi halogen liên kết với carbon bậc II Lời giải chi tiết :
2 – iodopropane: CH3 – CHI – CH3. Là dẫn xuất halogen bậc II Đáp án B
Câu 21 :
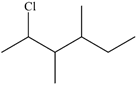
Cho dẫn xuất halogen có công thức cấu tạo sau: Danh pháp thay thế của dẫn xuất halogen trên là
Đáp án : B Phương pháp giải :
Dựa vào tên gọi của dẫn xuất halogen Lời giải chi tiết :
Đáp án B
Câu 22 :
Cho các thí nghiệm: (a) Đun nóng C6H5CH2Cl trong dung dịch NaOH (b) Đung nóng hỗn hợp CH3CH2CH2Cl, KOH và C2H5OH (c) Đun nóng CH3CH2CH2Cl trong dung dịch NaOH (d) Đun nóng hỗn hợp CH3CHClCH=CH2, KOH và C2H5OH Có bao nhiêu thí nghiệm tạo sản phẩm chính là alcohol?
Đáp án : D Phương pháp giải :
Dựa vào tính chất hóa học của dẫn xuất halogen Lời giải chi tiết :
Câu 23 :
Bình “ga” sử dụng trong hộ gia đình Y có chứa 10,92 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 3 : 4. Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Trung bình, lượng nhiệt tiêu thụ từ’ đốt khí “ga” của hộ gia đình Y tương ứng với bao nhiêu số điện? (Biết hiệu suất sử dụng nhiệt là 50% và 1 số điện = 1 kWh = 3600 kJ)
Đáp án : C Lời giải chi tiết :
Gọi số mol của propane là 3x; butane là 4x Ta có: khối lượng bình gas = m C3H8 + m C4H10 = 3x.44 + 4x.58 = 10,92 .103 => x = 30,67 mol => n C3H8 = 92,01 mol; n C4H10 = 122,68 mol Nhiệt lượng tỏa ra khi đốt cháy bình gas hoàn toàn là: 92,01 . 2220 + 122,68 . 2850 = 550220 KJ. Vì hiệu suất sử dụng nhiệt là 50% => lượng nhiệt tiêu thụ từ đốt khí gas của hộ gia đình tương đương với số điện là: \(\frac{{550220}}{{3600}}.50\% = 76\)số điện Đáp án C
Đáp án : A Phương pháp giải :
Dựa vào điều chế của alkane và alkene Lời giải chi tiết :
(1) Al4C3 + 12H2O \( \to \)4Al(OH)3 + 3CH4 hoặc Al4C3 + 12HCl \( \to \)4AlCl3 + 3CH4 Đáp án A
Câu 25 :
Cho 8,0 gam hỗn hợp X gồm acetylene và ethylene (tỉ lệ mol 2 : 1) lội qua dung dịch nước bromine dư thấy có m gam phản ứng. Giá trị của m là
Đáp án : B Phương pháp giải :
Dựa vào tính chất hóa học của acetylene và ethylene Lời giải chi tiết :
m C2H2 + m C2H4 = 2a.26 + 28a = 8 => a = 0,1 mol => n C2H2 = 0,2 mol; n C2H4 = 0,1 mol \(\begin{array}{l}{C_2}{H_2} + 2B{r_2} \to {C_2}{H_2}B{r_4}\\0,2{\rm{ 0,4}}\\{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{4}}}{\rm{ + B}}{{\rm{r}}_{\rm{2}}}{\rm{ }} \to {\rm{ }}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{4}}}{\rm{B}}{{\rm{r}}_{\rm{2}}}\\{\rm{0,1 0,1}}\\{n_{Br2}} = 0,4 + 0,1 = 0,5mol\end{array}\) m Br2 = 0,5 . 160 = 80g
|














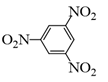
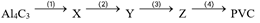
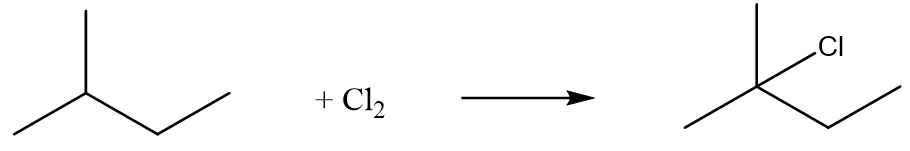
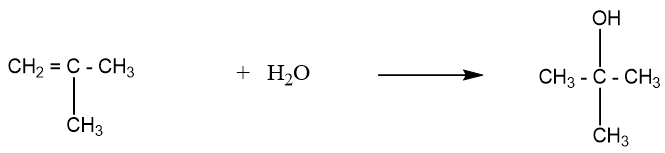
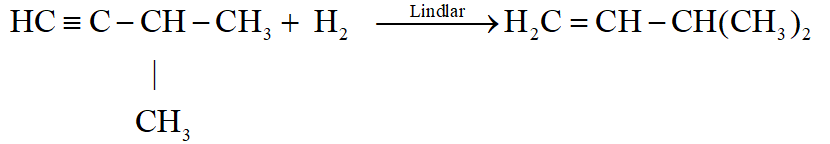
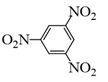 : 1,3,5 – trinitrobenzene
: 1,3,5 – trinitrobenzene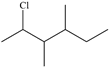 : 2 – chloro – 3,4 – dimethylhexane
: 2 – chloro – 3,4 – dimethylhexane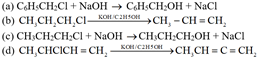









Danh sách bình luận