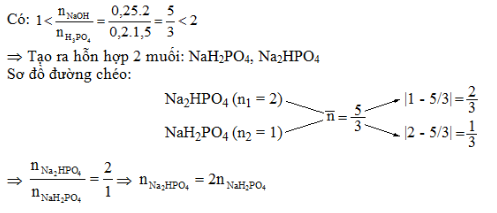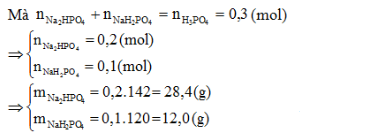Đề thi giữa kì 1 Hóa 9 - Đề số 5Tổng hợp đề thi học kì 2 lớp 9 tất cả các môn Toán - Văn - Anh - Lí - Hóa - Sinh - Sử - Địa - GDCD Đề bài
Câu 1 :
Dãy muối cacbonat bị nhiệt phân ở nhiệt độ cao
Câu 2 :
Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là:
Câu 3 :
Lưu huỳnh đioxit được tạo thành từ cặp chất nào sau đây?
Câu 4 :
Kim loại nào sau đây có khả năng tự tạo ra màng oxit cứng bảo vệ khi để ngoài không khí?
Câu 5 :
Kim loại vonfam được dùng làm dây tóc bóng đèn vì những nguyên nhân nào sau đây?
Câu 6 :
Gang là hợp kim của sắt với cacbon và một lượng nhỏ các nguyên tố khác như: Si, Mn, S,… trong đó hàm lượng cacbon chiếm:
Câu 7 :
Nhóm kim loại nào có thể tác dụng với nước ở nhiệt độ thường:
Câu 8 :
Phản ứng hoá học nào sau đây tạo ra oxit bazơ ?
Câu 9 :
Trong các kim loại sau: Cu, Fe, Pb, Al người ta thường dùng kim loại nào để làm vật liệu dẫn điện hay dẫn nhiệt?
Câu 10 :
Tính chất vật lí nào sau đây của sắt khác với các kim loại khác?
Câu 11 :
Quặng nào sau đây chứa thành phần chính là Al2O3:
Câu 12 :
Trong các oxit sau, oxit nào tác dụng được với nước?
Câu 13 :
Có thể dung CaO để làm khô khí nào trong các khí dưới đây:
Câu 14 :
Nhôm bền trong không khí là do
Câu 15 :
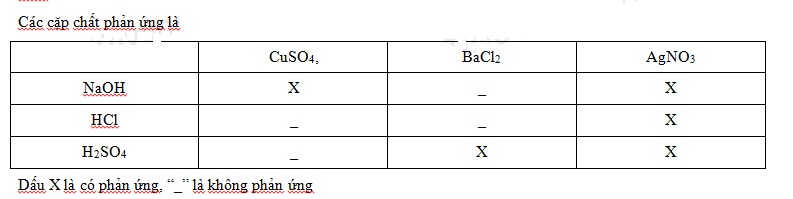
Dãy A gồm các dung dịch : NaOH, HCl, H2SO4; Dãy B gồm các dung dịch: CuSO4, BaCl2, AgNO3. Cho lần lượt các chất ở dãy A phản ứng đôi một với các chất ở dãy B. Số phản ứng thu xảy ra thu được kết tủa là:
Câu 16 :
Hóa chất nào sau đây dùng để khử chua đất trong công nghiệp?
Câu 17 :
Nhiệt phân sắt (III) hiđroxit thu được sản phẩm là:
Câu 18 :
Trong các loại phân bón sau, phân bón hoá học kép là:
Câu 19 :
Cho hỗn hợp bột gồm: Al, Fe, Mg và Cu vào dung dịch HCl dư, sau phản ứng thu được chất rắn T không tan. Vậy T là:
Câu 20 :
Dung dịch có độ bazơ mạnh nhất trong các dung dịch có giá trị pH sau:
Câu 21 :
Một oxit được tạo bởi 2 nguyên tố là sắt và oxi, trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3. Công thức hoá học của oxit sắt là:
Câu 22 :
Khối lượng Al2O3 phản ứng vừa hết với 200 ml dung dịch KOH 1M là:
Câu 23 :
Dẫn 1,12 lít khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 0,1M. Khối lượng của muối thu được sau phản ứng là
Câu 24 :
Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit clohidric. Thể tích khí Hiđro thu được ở đktc là:
Câu 25 :
Cho 8 gam Mg, Al vào dung dịch \(HCl\) vừa đủ. Sau phản ứng thu được dung dịch X, 2,36 (g) chất rắn và 6,272 (l) khí ở đktc. Phần trăm khối lượng mỗi kim loại có trong hỗn hợp lần lượt là.
Câu 26 :
Thêm 250 ml dung dịch NaOH 2M vào 200 ml dung dịch H3PO4 1,5M. Muối tạo thành và khối lượng tương ứng là:
Câu 27 :
Thành phần phần trăm của Na và Ca trong hợp chất NaOH và Ca(OH)2 lần lượt là:
Câu 28 :
Khi phân hủy bằng nhiệt 14,2 gam CaCO3 và MgCO3 ta thu được 3,36 lít CO2 ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu lần lượt là:
Câu 29 :
Cho 0,1 mol Ba(OH)2 vào dung dịch NH4NO3 dư thì thể tích thoát ra ở đktc là :
Câu 30 :
Khi làm nguội 1026,4 gam dung dịch bão hòa R2SO4. nH2O (trong đó R là kim loại kiềm và n nguyên, thỏa mãn điều kiện 7< n< 12) từ 800C xuống 100C thì có 395,4 gam tinh thể R2SO4. nH2O tách ra khỏi dung dịch. Biết độ tan của R2SO4 ở 800C và 100C lần lượt là 28,3 gam và 9 gam. Công thức phân tử của hiđrat nói trên là:
Câu 31 :
Một loại phân dùng để bón cho cây được một người sử dụng với khối lượng là 500 gam, phân này có thành phần hóa học là (NH4)2SO4. Cho các phát biểu sau về loại phân bón trên: (1) Loại phân này được người đó sử dụng nhằm cung cấp đạm và lân cho cây. (2) Thành phần phần trăm nguyên tố dinh dưỡng có trong 200 gam phân bón trên là 21,21% (3) Khối lượng của nguyên tố dinh dưỡng có trong 500 gam phân bón trên là 106,06 gam. (4) Loại phân này khi hòa tan vào nước thì chỉ thấy một phần nhỏ phân bị tan ra, phần còn lại ở dạng rắn dẻo. (5) Nếu thay 500 gam phân urê bằng 500 gam phân bón trên thì sẽ có lợi hơn. Số phát biểu đúng là
Câu 32 :
Biết khối lượng riêng của nhôm là 2,7g/cm3. Vậy thể tích 1 mol của nhôm là:
Câu 33 :
Hòa tan 5,1g oxit của một kim loại hóa trị III bằng dung dịch HCl, số mol axit cần dùng là 0,3 mol. Công thức phân tử của oxit đó là :
Câu 34 :
Cho 5,4 gam bột nhôm vào 200 ml dung dịch NaOH, sau phản ứng thấy khối lượng dung dịch tăng 3,6 gam. Nồng độ mol/lít của dung dịch NaOH là
Câu 35 :
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Fe2O3 và Al trong điều kiện không có không khí thu được hỗn hợp chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2. Mặt khác nếu cho Y tác dụng với dung dịch HCl dư sẽ thu được 0,4 mol H2. Số mol Al trong X là
Câu 36 :
Cho 11,2 gam kim loại sắt tác dụng hết với dd H2SO4 loãng, thể tích khí H2 thu được ở đktc là
Câu 37 :
Cho dung dịch AgNO3 dư tác dụng với hỗn hợp có hòa tan 12,5 gam hai muối KCl và KBr thu được 20,78 gam hỗn hợp AgCl và AgBr. Thành phần % của muối AgCl trong hỗn hợp thu được sau phản ứng là.
Câu 38 :
Hòa tan 7,74 gam hỗn hợp 2 kim loại Mg, Al trong 500ml dung dịch hỗn hợp chứa HCl 1M và H2SO4 0,38M loãng. Thu được dung dịch A và 8,736 lít khí H2 (đktc). Khối lượng muối có trong dung dịch A là
Câu 39 :
Hòa tan 2,8 gam một kim loại R có hóa trị II bằng một hỗn hợp gồm 80 ml dung dịch H2SO4 0,5M và 200 ml dung dịch HCl 0,2M thu được dung dịch A và V lít khí H2(ở đktc). Để trung hòa dung dịch A thì cần 100 ml dung dịch KOH 0,2M. Phát biểu nào dưới đây về bài toán trên là chưa đúng?
Câu 40 :
Tiến hành hai thí nghiệm: -Thí nghiệm 1: Cho 650 ml dung dịch NaOH 2M vào 400 ml dung dịch AlCl3 aM thu được 3b gam kết tủa. -Thí nghiệm 2: Cho 700 ml dung dịch NaOH 2M vào 400 ml dung dịch AlCl3 aM thu được 2b gam kết tủa. Giá trị của a, b là:
Lời giải và đáp án
Câu 1 :
Dãy muối cacbonat bị nhiệt phân ở nhiệt độ cao
Đáp án : C Lời giải chi tiết :
Ghi nhớ: Na2CO3 và K2CO3 không bị nhiệt phân hủy => loại A, B, D => Chọn C CaCO3 \(\xrightarrow{{{t^0}}}\) CaO + CO2↑ Ca(HCO3)2 \(\xrightarrow{{{t^0}}}\) CaCO3 + CO2 + H2O
Câu 2 :
Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là:
Đáp án : B Lời giải chi tiết :
Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là: Có xuất hiện kết tủa trắng AgNO3 + NaCl → AgCl(↓ trắng) + NaNO3
Câu 3 :
Lưu huỳnh đioxit được tạo thành từ cặp chất nào sau đây?
Đáp án : D Lời giải chi tiết :
Công thức hóa học của lưu huỳnh đioxit là SO2 A, B, C đều không xảy ra phản ứng hóa học D. Na2SO3 + 2H2SO4 → Na2SO4 + SO2↑ + H2O
Câu 4 :
Kim loại nào sau đây có khả năng tự tạo ra màng oxit cứng bảo vệ khi để ngoài không khí?
Đáp án : A Phương pháp giải :
Cần nắm được tính chất hóa học của kim loại tác dụng với oxi trong không khí Lời giải chi tiết :
Kim loại có khả năng tự tạo ra màng oxit cứng bảo vệ khi để ngoài không khí là Al. Al trong không khí thường có lớp màng oxit Al2O3 bảo vệ.
Câu 5 :
Kim loại vonfam được dùng làm dây tóc bóng đèn vì những nguyên nhân nào sau đây?
Đáp án : C Lời giải chi tiết :
Kim loại vonfam được dùng làm dây tóc bóng đèn vì Là kim loại có nhiệt độ nóng chảy rất cao
Câu 6 :
Gang là hợp kim của sắt với cacbon và một lượng nhỏ các nguyên tố khác như: Si, Mn, S,… trong đó hàm lượng cacbon chiếm:
Đáp án : C Lời giải chi tiết :
Từ 0,01 – 2% khối lượng C là thép và từ 2 – 5% khối lượng C là gang
Câu 7 :
Nhóm kim loại nào có thể tác dụng với nước ở nhiệt độ thường:
Đáp án : D Lời giải chi tiết :
Nhóm kim loại tác dụng với nước ở nhiệt độ thường là: K, Na, Ca, Ba
Câu 8 :
Phản ứng hoá học nào sau đây tạo ra oxit bazơ ?
Đáp án : D Lời giải chi tiết :
A. Cho dd Ca(OH)2 phản ứng với SO2 Ca(OH)2 + SO2 → CaSO3 + H2O => không tạo ra oxit bazơ B. Cho dd NaOH phản ứng với dd H2SO4 2NaOH + H2SO4 → Na2SO4 + H2O => không tạo ra oxit bazơ C. Cho Cu(OH)2 phản ứng với HCl Cu(OH)2 + 2HCl → CuCl2 + 2H2O => không tạo ra oxit bazơ D. Nung nóng Cu(OH)2 Cu(OH)2 $\xrightarrow{{{t}^{o}}}$ CuO + H2O => tạo ra oxit bazơ là CuO
Câu 9 :
Trong các kim loại sau: Cu, Fe, Pb, Al người ta thường dùng kim loại nào để làm vật liệu dẫn điện hay dẫn nhiệt?
Đáp án : B Lời giải chi tiết :
Trong thực tế người ta thường sử dụng 2 kim loại để làm vật liệu dẫn điện và dẫn nhiệt là Cu và Al.
Câu 10 :
Tính chất vật lí nào sau đây của sắt khác với các kim loại khác?
Đáp án : B Lời giải chi tiết :
Tính chất vật lí của sắt khác với các kim loại khác là: tính nhiễm từ
Câu 11 :
Quặng nào sau đây chứa thành phần chính là Al2O3:
Đáp án : A Phương pháp giải :
Ghi nhớ phản ứng điều chế Al trong công nghiệp Lời giải chi tiết :
Thành phần chính của quặng boxit là Al2O3 Thành phần chính của quặng Pirit là FeS2 Thành phần chính của quặng Đolomit là: MgCO3. CaCO3 Thành phần chính của quặng Apatit là: Ca3(PO4)2
Câu 12 :
Trong các oxit sau, oxit nào tác dụng được với nước?
Đáp án : A Phương pháp giải :
Ghi nhớ: oxit của kim loại kiềm, kiềm thổ (trừ BeO, MgO) tác dụng được với nước ở điều kiện thường. Lời giải chi tiết :
CaO + H2O → Ca(OH)2
Câu 13 :
Có thể dung CaO để làm khô khí nào trong các khí dưới đây:
Đáp án : C Lời giải chi tiết :
CaO không tác dụng với CO nên có thể dung để làm khô khí CO
Câu 14 :
Nhôm bền trong không khí là do
Đáp án : D Phương pháp giải :
Dựa vào tính chất hóa học của nhôm: tác dụng với phi kim Lời giải chi tiết :
Ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp Al2O3 mỏng bền vững. Lớp oxit này bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng với oxi trong không khí và nước
Câu 15 :
Dãy A gồm các dung dịch : NaOH, HCl, H2SO4; Dãy B gồm các dung dịch: CuSO4, BaCl2, AgNO3. Cho lần lượt các chất ở dãy A phản ứng đôi một với các chất ở dãy B. Số phản ứng thu xảy ra thu được kết tủa là:
Đáp án : B Lời giải chi tiết :
Câu 16 :
Hóa chất nào sau đây dùng để khử chua đất trong công nghiệp?
Đáp án : D Lời giải chi tiết :
Đất chua là đất có môi trường axit => dùng hóa chất có tính bazơ để trung hòa bớt độ chua của đất CaO + H2O → Ca(OH)2 (môi trường bazơ) Ca(OH)2 trung hòa lượng H+ trong đất làm đất bớt chua
Câu 17 :
Nhiệt phân sắt (III) hiđroxit thu được sản phẩm là:
Đáp án : C Phương pháp giải :
Bazo không tan nhiệt phân tạo thành oxit tương ứng và nước Lời giải chi tiết :
2Fe(OH)3 \(\buildrel {{t^0}} \over\longrightarrow \)Fe2O3 + 3H2O
Câu 18 :
Trong các loại phân bón sau, phân bón hoá học kép là:
Đáp án : D Lời giải chi tiết :
Phân bón hoá học kép là phân bón có chứa 2, 3 nguyên tố N, P, K: KNO3
Câu 19 :
Cho hỗn hợp bột gồm: Al, Fe, Mg và Cu vào dung dịch HCl dư, sau phản ứng thu được chất rắn T không tan. Vậy T là:
Đáp án : D Phương pháp giải :
HCl chỉ tác dụng được với các kim loại đứng trước H trong dãy điện hóa của kim loại Lời giải chi tiết :
Cu là kim loại đứng sau H trong dãy điện hóa nên không tan trong dd HCl => chất rắn T là Cu
Câu 20 :
Dung dịch có độ bazơ mạnh nhất trong các dung dịch có giá trị pH sau:
Đáp án : D Lời giải chi tiết :
pH > 7: dung dịch có tính bazơ, pH càng lớn độ bazơ càng lớn => pH = 14 có độ bazơ mạnh nhất
Câu 21 :
Một oxit được tạo bởi 2 nguyên tố là sắt và oxi, trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3. Công thức hoá học của oxit sắt là:
Đáp án : B Phương pháp giải :
Tỉ lệ khối lượng giữa Fe và O là 7/3 => Đặt khối lượng của Fe là 7 thì khối lượng của O là 3 Gọi công thức của oxit là: FexOy (x,y € N*) Áp dụng công thức ta có: \(\begin{gathered} => x, y = ? Lời giải chi tiết :
Tỉ lệ khối lượng giữa Fe và O là 7/3 => Đặt khối lượng của Fe là 7 thì khối lượng của O là 3 Gọi công thức của oxit là: FexOy (x,y € N*) Áp dụng công thức ta có: \(\begin{gathered} Vậy công thức của oxit là Fe2O3
Câu 22 :
Khối lượng Al2O3 phản ứng vừa hết với 200 ml dung dịch KOH 1M là:
Đáp án : B Phương pháp giải :
Bước 1: Đổi số mol KOH = VKOH.CM Bước 2: Tính số mol Al2O3 theo mol KOH dựa vào PTHH: Al2O3 + 2KOH → 2KAlO2 + H2O Lời giải chi tiết :
200 ml = 0,2 (lít) ⟹ nKOH = V.CM = 0,2.1 = 0,2 (mol) PTHH: Al2O3 + 2KOH → 2KAlO2 + H2O (mol) 0,1 ← 0,2 Theo PTHH ta có: nAl2O3 = 1/2 nKOH = 1/2.0,2 = 0,1 (mol) ⟹ mAl2O3 = nAl2O3. MAl2O3 = 0,1.102 = 10,2 (g)
Câu 23 :
Dẫn 1,12 lít khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 0,1M. Khối lượng của muối thu được sau phản ứng là
Đáp án : C Phương pháp giải :
+) Xét tỉ lệ: $\dfrac{{{n_{S{O_2}}}}}{{{n_{Ca{{(OH)}_2}}}}}$ => phản ứng tạo muối CaSO3 +) Viết PTHH và tính khối lượng CaSO3 theo SO2 Lời giải chi tiết :
${n_{S{O_2}}} = 0,05{\text{ }}mol;{\text{ }}{n_{Ca{{\left( {OH} \right)}_2}}} = 0,07{\text{ }}mol$ Xét tỉ lệ: $\dfrac{{{n_{S{O_2}}}}}{{{n_{Ca{{(OH)}_2}}}}} = \dfrac{{0,05}}{{0,07}} < 1$ => SO2 hết, Ca(OH)2 dư, phản ứng tạo muối CaSO3 SO2 + Ca(OH)2 → CaSO3 + H2O 0,05 → 0,05 → 0,05 => mCaSO3 = 0,05.120 = 6 gam
Câu 24 :
Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit clohidric. Thể tích khí Hiđro thu được ở đktc là:
Đáp án : B Phương pháp giải :
Đổi số mol của Mg: nMg = mMg : MMg = ? (mol) Viết PTHH xảy ra: Mg + 2HCl → MgCl2 + H2 Tính số mol của H2 theo số mol của Mg: nH2 = nMg = ? (mol) => VH2(đktc) = nH2×22,4 = ? (lít) Lời giải chi tiết :
nMg = mMg : MMg = 4,8 : 24 = 0,2mol PTHH: Mg + 2HCl → MgCl2 + H2 1mol 2mol 1mol 0,2mol ? mol VH2 = nH2 . 22,4 = 0,2 . 22,4 = 4,48l
Câu 25 :
Cho 8 gam Mg, Al vào dung dịch \(HCl\) vừa đủ. Sau phản ứng thu được dung dịch X, 2,36 (g) chất rắn và 6,272 (l) khí ở đktc. Phần trăm khối lượng mỗi kim loại có trong hỗn hợp lần lượt là.
Đáp án : C Phương pháp giải :
TH1: Giả sử chỉ có phản ứng, Al chưa phản ứng TH2: Giả sử có cả Mg và Al đều phản ứng. Biện luận chất rắn thu được theo tính toán với theo đề bài cho mỗi trường hợp để xem trường hợp nào thỏa mãn. Lời giải chi tiết :
- Khí tạo thành sau phản ứng là \({H_2}\) \({n_{{H_2}}} = \frac{{6,272}}{{22,4}} = 0,28(mol)\) - Giả sử chỉ có \(Mg\)phản ứng, Al chưa phản ứng PTHH: Mg + 2HCl → MgCl2 + H2↑ ⟹ nMg = nH2 = 0,28 (mol) ⟹ mMg = 0,28.24 = 6,72 (g) ⟹ Khối lượng kim loại còn lại là: mKL = 8 - 6,72 = 1,28 (g) # 2,36 (g) ⟹ loại. - Giả sử có cả Mg và Al đều phản ứng. Do Mg là kim loại hoạt động mạnh hơn Al nên Mg pư hết trước, sau đó mới đến Al pư. ⟹ Chất rắn còn dư là Al mMg + mAl pu = 8 - 2,36 = 5,64 (g) Đặt nMg = x (mol); nAl pư = y (mol) PTHH: Mg + 2HCl → MgCl2 + H2↑ (mol) x → x 2Al + 6HCl → AlCl3 + 3H2↑ (mol) y → 1,5y Theo bài ra ta có hệ phương trình sau: \(\left\{ \begin{array}{l}\sum {{n_{{H_2}}} = \,} x + 1,5y = 0,28\\\sum {m{\,_{hh}} = \,} 24x + 27y = 5,64\end{array} \right. \Leftrightarrow \left\{ \begin{array}{l}x = 0,1(mol) = {n_{Mg}}\\y = 0,12(mol) = {n_{Al\,pu}}\end{array} \right.\) Phần trăm khối lượng mỗi kim loại có trong hỗn hợp là: \(\left\{ \begin{array}{l}\% {m_{Mg}} = \frac{{{m_{Mg}}}}{{{m_{hh}}}}.100\% = \frac{{0,1.24}}{8}.100\% = 30\% \\\% {m_{Al}} = 100\% - 30\% = 70\% \end{array} \right.\)
Câu 26 :
Thêm 250 ml dung dịch NaOH 2M vào 200 ml dung dịch H3PO4 1,5M. Muối tạo thành và khối lượng tương ứng là:
Đáp án : C Phương pháp giải :
Lập tỉ lệ \(k = \dfrac{{{n_{NaOH}}}}{{{n_{{H_3}P{O_4}}}}}\) PTHH có thể xảy ra: NaOH + H3PO4 → NaH2PO4 + H2O (1) 2NaOH + H3PO4 → Na2HPO4 + 2H2O (2) 3NaOH + H3PO4 → Na3PO4 + 3H2O (3) Nếu k ≤ 1 chỉ xảy ra (1) Nếu 1 < k < 2 xảy ra cả (1); (2) Nếu 2 < k < 3 xảy ra của (2); (3) Nếu k ≥ 3 xảy ra (3) Nếu k = 2 thì chỉ xảy ra (2) Sau khi xác định được phản ứng xảy ra theo phương trình nào thì dựa vào phương trình đó để giải bài toán. Lời giải chi tiết :
Câu 27 :
Thành phần phần trăm của Na và Ca trong hợp chất NaOH và Ca(OH)2 lần lượt là:
Đáp án : D Phương pháp giải :
Công thức tính phần trăm khối lượng của nguyên tố trong hợp chất: $\% {m_R} = \frac{{n.{M_R}}}{{{M_{hop\,\,chat}}}}.100\% $ với n là số nguyên tử R có trong 1 phân tử hợp chất đó Lời giải chi tiết :
Công thức tính phần trăm khối lượng của nguyên tố trong hợp chất: $\% {m_R} = \frac{{n.{M_R}}}{{{M_{hop\,\,chat}}}}.100\% $ với n là số nguyên tử R có trong 1 phân tử hợp chất đó Ta có: $\% {m_{Na}} = \frac{{{M_{Na}}}}{{{M_{NaOH}}}}.100\% = \frac{{23}}{{40}}.100\% = 57,5\% $ $\% {m_{Ca}} = \frac{{{M_{Ca}}}}{{{M_{Ca{{(OH)}_2}}}}}.100\% = \frac{{40}}{{74}}.100\% = 54,1\% $
Câu 28 :
Khi phân hủy bằng nhiệt 14,2 gam CaCO3 và MgCO3 ta thu được 3,36 lít CO2 ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu lần lượt là:
Đáp án : B Phương pháp giải :
Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y => mhỗn hợp = PT(1) Phương trình hóa học: CaCO3 $\xrightarrow{{{t^o}}}$ CaO + CO2 x mol → x mol MgCO3 $\xrightarrow{{{t^o}}}$ MgO + CO2 y mol → y mol $ = > {n_{C{O_2}}} = PT(2)$ Lời giải chi tiết :
${n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15\,\,mol$ Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y mol => mhỗn hợp = 100x + 84y = 14,2 (1) Phương trình hóa học: CaCO3 $\xrightarrow{{{t^o}}}$ CaO + CO2 x mol → x mol MgCO3 $\xrightarrow{{{t^o}}}$ MgO + CO2 y mol → y mol $ = > {n_{C{O_2}}} = x + y = 0,15\,\,mol\,\,(2)$ Từ (1) và (2) => x = 0,1 mol; y = 0,05 mol $ = > \% {m_{CaC{{\text{O}}_3}}} = \frac{{100.0,1}}{{14,2}}.100\% = 70,42\% ;\,\,\% {m_{MgC{O_3}}} = 29,58\% $
Câu 29 :
Cho 0,1 mol Ba(OH)2 vào dung dịch NH4NO3 dư thì thể tích thoát ra ở đktc là :
Đáp án : B Lời giải chi tiết :
PTHH: Ba(OH)2 + 2NH4NO3 → Ba(NO3)2 + 2NH3 + 2H2O Tỉ lê: 1 2 Pứ: 0,1 ? mol Từ PTHH ta có n NH3 = 2 n Ba(OH)2 = 0,2 mol => V NH3 = n NH3 . 22,4 = 0,2 . 22,4 = 44,8 lít
Câu 30 :
Khi làm nguội 1026,4 gam dung dịch bão hòa R2SO4. nH2O (trong đó R là kim loại kiềm và n nguyên, thỏa mãn điều kiện 7< n< 12) từ 800C xuống 100C thì có 395,4 gam tinh thể R2SO4. nH2O tách ra khỏi dung dịch. Biết độ tan của R2SO4 ở 800C và 100C lần lượt là 28,3 gam và 9 gam. Công thức phân tử của hiđrat nói trên là:
Đáp án : B Phương pháp giải :
Phương pháp : - Một chất có độ tan S thì m của chất tan là: \(\begin{array}{l}{m_{ct}}\, = \,\frac{{{m_{dd}}}}{{100 + S}}.S\\\end{array}\), ta tính được: + Tính khối lượng R2SO4 ở 800C → Khối lượng dd R2SO4 ở 100C + Tính khối lượng R2SO4 ở 100C - Tính khối lượng H2O: \({m_{{H_2}O}}\, = \,{m_{tinh\,the\,{R_2}S{O_4}}}\, - \,{m_{{R_2}S{O_4}\,({{10}^o}C)}}\) => \({n_{{H_2}O}}\) - Tính số mol R2SO4 : \({n_{{R_2}S{O_4}}}\, = \,{n_{{H_2}O}}:n\) mol - Với 7 <n< 12 => Biện luận tìm n và R => CTPT của hiđrat Lời giải chi tiết :
Độ tan của R2SO4 ở 800C là 28,3 gam → trong 1026,4 g dd có: \({m_{{R_2}S{O_4}\,}} = \,\,\frac{{1026,4}}{{100 + 28,3}}.28,3 = \,226,4(g)\) Khi làm lạnh thì mdd =1026,4 -395,4= 631g → dd có: \({m_{{R_2}S{O_4}({{10}^o}C)}}\,\, = \,\,\frac{{631}}{{100 + 9}}.9\, = \,52,1g\) Ta có: \({m_{{R_2}S{O_4}(tinh{\text{ }}thể)}} = 226,4{\text{ }}-{\text{ }}52,1{\text{ }} = {\text{ }}174,3g\) → \({m_{{H_2}O}}\, = \,395,4\, - \,174,3\, = \,221,1g\ → \({n_{{H_2}O}}{\mkern 1mu} = {\mkern 1mu} \,\frac{{737}}{{60}}mol\) → \({n_{{R_2}S{O_4}}}\, = \frac{{737}}{{60n}} \to {M_{{R_2}S{O_4}}} = 2R + 96 = \frac{{174,3}}{{{n_{{R_2}S{O_4}}}}} = 14,19n\) Với 7 <n< 12 thỏa mãn n=10 và R =23 Vậy CTPT của hiđrat là: Na2SO4.10H2O
Câu 31 :
Một loại phân dùng để bón cho cây được một người sử dụng với khối lượng là 500 gam, phân này có thành phần hóa học là (NH4)2SO4. Cho các phát biểu sau về loại phân bón trên: (1) Loại phân này được người đó sử dụng nhằm cung cấp đạm và lân cho cây. (2) Thành phần phần trăm nguyên tố dinh dưỡng có trong 200 gam phân bón trên là 21,21% (3) Khối lượng của nguyên tố dinh dưỡng có trong 500 gam phân bón trên là 106,06 gam. (4) Loại phân này khi hòa tan vào nước thì chỉ thấy một phần nhỏ phân bị tan ra, phần còn lại ở dạng rắn dẻo. (5) Nếu thay 500 gam phân urê bằng 500 gam phân bón trên thì sẽ có lợi hơn. Số phát biểu đúng là
Đáp án : D Phương pháp giải :
Dựa vào kiến thức về phân bón hóa học được học ở SGK hóa 9 –trang 37 để trả lời Lời giải chi tiết :
(1) Sai :(NH4)2SO4 chứa nguyên tố N nên dùng để cung cấp phân đạm cho cây, không chứa Photpho \( \to\) không dùng để cung cấp phân lân (2) Đúng: Phần trăm khối lượng N có trong phân hóa học là: \(\% N = \dfrac{{{M_N}}}{{{M_{{{(N{H_4})}_2}S{O_4}}}}}.100\% = \dfrac{{14.2}}{{132}}.100\% = 21,21\% \) (3) Đúng \({n_{{{(N{H_4})}_2}S{O_4}}} = \dfrac{{500}}{{132}}\,\,mol \to {n_N} = 2{n_{{{(N{H_4})}_2}S{O_4}}} = \dfrac{{250}}{{33}}\,\,mol \to {m_N} = \dfrac{{250}}{{33}}.14 = 106,06\,\,gam\) (4) Sai vì phân này tan hoàn toàn trong nước (5) Sai vì phân ure (NH2)2CO có hàm lượng N cao hơn phân (NH4)2SO4 \( \to\) thay ure bằng phân này sẽ giảm hàm lượng nguyên tố dinh dưỡng \( \to\) ít lợi hơn Vậy có 2 phát biểu đúng
Câu 32 :
Biết khối lượng riêng của nhôm là 2,7g/cm3. Vậy thể tích 1 mol của nhôm là:
Đáp án : B Phương pháp giải :
Công thức: mAl = nAl . MAl = ? (g) Thể tích của Al: VAl = mAl : DAl = ? cm3 Lời giải chi tiết :
m Al = nAl . MAl = 1 . 27 = 27g D = m : V => V = m : D = 27 : 2,7 = 10 cm3
Câu 33 :
Hòa tan 5,1g oxit của một kim loại hóa trị III bằng dung dịch HCl, số mol axit cần dùng là 0,3 mol. Công thức phân tử của oxit đó là :
Đáp án : B Phương pháp giải :
Gọi công thức của oxit là A2O3 Ta có A2O3 + 6HCl → 2ACl3 + 3H2O Từ pthh ta có nA2O3 = 1/6 nHCl = 1/6 . 0,3 = 0,05 mol => MA2O3 = mA2O3 : nA2O3 = ? => Phân tử khối của A Lời giải chi tiết :
Gọi công thức của oxit là A2O3 Ta có A2O3 + 6HCl → 2ACl3 + 3H2O Từ pthh ta có nA2O3 = 1/6 nHCl = 1/6 . 0,3 = 0,05 mol => MA2O3 = mA2O3 : nA2O3 = 5,1 : 0,05 = 102 MA2O3 = 2 . MA + 3 . 16 = 2MA + 48 = 102 => MA = 27 => A là nhôm
Câu 34 :
Cho 5,4 gam bột nhôm vào 200 ml dung dịch NaOH, sau phản ứng thấy khối lượng dung dịch tăng 3,6 gam. Nồng độ mol/lít của dung dịch NaOH là
Đáp án : C Phương pháp giải :
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑ x → x → 1,5x +) Khối lượng dung dịch tăng 3,6 gam => ∆mtăng = mAl – mH2 = 3,6 gam +) nNaOH = nAl phản ứng Lời giải chi tiết :
nAl = 0,2 mol Gọi số mol Al phản ứng là x mol 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑ x → x → 1,5x Khối lượng dung dịch tăng 3,6 gam => ∆mtăng = mAl – mH2 = 3,6 gam => 27x – 1,5x.2 = 3,6 => x = 0,15 mol Theo PT: nNaOH = nAl phản ứng = 0,15 mol $ = > {C_{M\,\,NaOH}} = \frac{{0,15}}{{0,2}} = 0,75M$
Câu 35 :
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Fe2O3 và Al trong điều kiện không có không khí thu được hỗn hợp chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2. Mặt khác nếu cho Y tác dụng với dung dịch HCl dư sẽ thu được 0,4 mol H2. Số mol Al trong X là
Đáp án : A Phương pháp giải :
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 0,2 mol ← 0,3 mol 2Al + 6HCl → AlCl3 + 3H2 0,2 mol → 0,3 mol Fe + 2HCl → FeCl2 + H2 0,1 mol ← 0,1 mol 2Al + Fe2O3 → Al2O3 + 2Fe 0,1 mol ← 0,1 mol Lời giải chi tiết :
Cho Y tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2 => trong Y chứa Al dư 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 0,2 mol ← 0,3 mol => nAl dư = 0,2 mol Y tác dụng với dung dịch HCl dư sẽ thu được 0,4 mol H2 2Al + 6HCl → AlCl3 + 3H2 0,2 mol → 0,3 mol Fe + 2HCl → FeCl2 + H2 0,1 mol ← 0,1 mol Phản ứng nhiệt nhôm: 2Al + Fe2O3 → Al2O3 + 2Fe 0,1 mol ← 0,1 mol => ∑nAl ban đầu = nAl dư + nAl phản ứng = 0,2 + 0,1 = 0,3 mol
Câu 36 :
Cho 11,2 gam kim loại sắt tác dụng hết với dd H2SO4 loãng, thể tích khí H2 thu được ở đktc là
Đáp án : D Phương pháp giải :
+ nFe = mFe/MFe. + Fe + H2SO4 à FeSO4 + H2 + Theo PTHH thì: nH2 = nFe => VH2 = 22,4. nH2 Lời giải chi tiết :
+ nFe = mFe/MFe = 11,2/56 = 0,2 mol. + Fe + H2SO4 → FeSO4 + H2 + Theo PTHH thì nH2 = nFe ⟹ VH2 = 22,4. nH2 = 22,4.0,2 = 4,48 lít
Câu 37 :
Cho dung dịch AgNO3 dư tác dụng với hỗn hợp có hòa tan 12,5 gam hai muối KCl và KBr thu được 20,78 gam hỗn hợp AgCl và AgBr. Thành phần % của muối AgCl trong hỗn hợp thu được sau phản ứng là.
Đáp án : D Lời giải chi tiết :
Câu 38 :
Hòa tan 7,74 gam hỗn hợp 2 kim loại Mg, Al trong 500ml dung dịch hỗn hợp chứa HCl 1M và H2SO4 0,38M loãng. Thu được dung dịch A và 8,736 lít khí H2 (đktc). Khối lượng muối có trong dung dịch A là
Đáp án : B Phương pháp giải :
So sánh số mol H có trong tổng HCl và H2SO4 với số mol H có trong H2 từ đó rút được axit pư dư, kim loại phản ứng hết TH1: giả sử HCl phản ứng hết, H2SO4 dư Tính được: mmuối 1 = mKL + mHCl + mH2SO4 pư - mH2 = ? TH2: giả sử H2SO4 phản ứng hết, HCl dư Tính được mmuối 2 = mKL + mHCl pư + mH2SO4 - mH2 = ? Vì thực tế phản ứng xảy ra đồng thời nên cả 2 axit đều dư Vì thực tế phản ứng xảy ra đồng thời nên 2 axit cùng dư sau phản ứng ⟹ mmuối 1 < mmuối A < mmuối 2 Lời giải chi tiết :
PTHH: Mg + 2HCl → MgCl2 + H2↑ (1) 2Al + 6HCl → 2AlCl3 + 3H2↑ (2) Mg + H2SO4 → MgSO4 + H2↑ (3) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ (4) 500 ml = 0,5 (lít) \(\left. \begin{array}{l} \Rightarrow {n_{HCl}} = 0,5.1 = 0,5\,(mol)\\ \Rightarrow {n_{{H_2}S{O_4}}} = 0,5.0,38 = 0,19\,(mol)\end{array} \right\} \Rightarrow {n_H} = {n_{HCl}} + 2{n_{H2SO4}} = 0,5 + 2.0,19 = 0,88\,(mol)\) nH2(đktc) = 8,736/22,4 = 0,39 (mol) ⟹ nH = 2nH2 = 2.0,39 = 0,78 (mol) Ta thấy: 0,88 > 0,78 nên axit dư, kim loại phản ứng hết. TH1: giả sử HCl phản ứng hết, H2SO4 dư nHCl = 0,5 (mol) ⟹ nH2 (1)+(2) = 1/2nHCl = 1/2.0,5 = 0,25 (mol) ⟹ nH2 (3)+(4) = 0,39 - 0,25 = 0,14 (mol) ⟹ nH2SO4 pư = 0,14 (mol) Theo ĐL BTKL ta có: mmuối = mKL + mHCl + mH2SO4 pư - mH2 = 7,74 + 0,5.36,5 + 0,14.98 - 0,39.2 = 38,93 (g) TH2: giả sử H2SO4 phản ứng hết, HCl dư nH2SO4 = 0,19 (mol) ⟹ nH2(3)+(4) = 0,19 (mol) ⟹ nH2(1)+(2) = 0,39 - 0,19 = 0,2 (mol) ⟹ nHCl pư = 2.0,2 = 0,4 (mol) Theo ĐLBTKL ta có: mmuối = mKL + mHCl pư + mH2SO4 - mH2 = 7,74 + 0,4.36,5 + 0,19.98 - 0,39.2 = 40,18 (g) Vì thực tế phản ứng xảy ra đồng thời nên cả 2 axit đều dư Suy ra tổng khối lượng muối A thu được là: 38,93 (g) < mmuối A < 40,18 (g)
Câu 39 :
Hòa tan 2,8 gam một kim loại R có hóa trị II bằng một hỗn hợp gồm 80 ml dung dịch H2SO4 0,5M và 200 ml dung dịch HCl 0,2M thu được dung dịch A và V lít khí H2(ở đktc). Để trung hòa dung dịch A thì cần 100 ml dung dịch KOH 0,2M. Phát biểu nào dưới đây về bài toán trên là chưa đúng?
Đáp án : D Phương pháp giải :
PTHH: R + H2SO4 → RSO4 + H2↑ (1) R + 2HCl → RCl2 + H2↑ (2) Trong hỗn hợp ban đầu \({n_{{H_2}S{O_4}}}:{n_{HCl}} = 1:1 \to \) phản ứng với R theo tỉ lệ 1: 1 \( \to\) Tỉ lệ của H2SO4 dư và HCl dư cũng là 1: 1 Đặt số mol H2SO4 dư = số mol HCl dư = x (mol) H2SO4 + 2KOH → K2SO4 + 2H2O (3) x →2x (mol) HCl + KOH → KCl + H2O (4) x → x (mol) \( \to\) tổng số mol KOH là: 2x + x = 0,02 \( \to\) x = ? (mol) Từ đó tính được số mol H2SO4; HCl pư ở (1), (2). Đặt vào phương trình (1), (2) tính toán được các dữ liệu mà đề bài yêu cầu. Lời giải chi tiết :
\({n_{{H_2}S{O_4}}} = 0,5.0,08 = 0,04\,\,mol\) ; nHCl = 0,2.0,2 = 0,04 (mol); nKOH = 0,1.0,2 = 0,02 (mol) PTHH: R + H2SO4 → RSO4 + H2↑ (1) R + 2HCl → RCl2+ H2↑ (2) Trong hỗn hợp ban đầu \({n_{{H_2}S{O_4}}}:{n_{HCl}} = 0,04:0,04 = 1:1 \to \) phản ứng với R theo tỉ lệ 1: 1 \( \to\) Tỉ lệ của H2SO4 dư và HCl dư cũng là 1: 1 Đặt số mol H2SO4 dư = số mol HCl dư = x (mol) H2SO4 + 2KOH → K2SO4 + 2H2O (3) x →2x (mol) HCl + KOH → KCl + H2O (4) x → x (mol) \( \to\) tổng số mol KOH là: 2x + x = 0,02 \( \to\) x = \(\dfrac{1}{{150}}\) (mol) \( \to\) \({n_{{H_2}S{O_4}(1)}} = 0,04 - \dfrac{1}{{150}} = \dfrac{1}{{30}}\) (mol) nHCl(1) = 0,04 – \(\dfrac{1}{{150}}\) = \(\dfrac{1}{{30}}\) (mol) PTHH: R + H2SO4 → RSO4 + H2↑ (1) \({1 \over {30}} \leftarrow {1 \over {30}}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, \to {1 \over {30}}\) R + 2HCl → RCl2 + H2↑ (2) \({1 \over {60}} \leftarrow {1 \over {30}}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, \to {1 \over {60}}\) \( \Rightarrow \sum {{n_{{H_2}}} = {1 \over {30}}} + {1 \over {60}} = 0,05\,(mol) \Rightarrow {V_{{H_2}}}(dktc) = 0,05 \times 22,4 = 1,12(l)\) => C đúng \( \Rightarrow \sum {{n_R} = {1 \over {30}}} + {1 \over {60}} = 0,05\,(mol) \Rightarrow {M_R} = {{{m_R}} \over {{n_R}}} = {{2,8} \over {0,05}} = 56\,(Fe)\) => A,B đúng \(\% Fe = {{{m_{Fe}}} \over {{m_{FeS{O_4}}}}}.100\% = {{{1 \over {30}} \times 56} \over {{1 \over {30}} \times 152}}.100\% = 36,84\% \) => D sai
Câu 40 :
Tiến hành hai thí nghiệm: -Thí nghiệm 1: Cho 650 ml dung dịch NaOH 2M vào 400 ml dung dịch AlCl3 aM thu được 3b gam kết tủa. -Thí nghiệm 2: Cho 700 ml dung dịch NaOH 2M vào 400 ml dung dịch AlCl3 aM thu được 2b gam kết tủa. Giá trị của a, b là:
Đáp án : D Phương pháp giải :
3NaOH + AlCl3 → Al(OH)3+ 3NaCl (1) Có thể có: NaOH + Al(OH)3 → NaAlO2 + 2H2O (2) nNaOH (TN1) = 0,65.2=1,3(mol) nNaOH (TN2) = 0,7.2=1,4(mol) nNaOH (TN1) = 1,3<nNaOH (TN2) = 1,4; lượng AlCl3 là như nhau; mà \({m_{Al{{(OH)}_3}(TN1)}} = 3b > {m_{Al{{(OH)}_3}(TN2)}} = 2b\) Nên xảy ra 2 trường hợp sau: Trường hợp 1: Ở thí nghiệm 1 chỉ xảy ra pư (1): NaOH hết, AlCl3 dư. Ở thí nghiệm 2 xảy ra 2 pư (1), (2): kết tủa Al(OH)3 tan một phần. Trường hợp 2: Cả 2 thí nghiệm kết tủa Al(OH)3 đều tan một phần. Lời giải chi tiết :
3NaOH + AlCl3 → Al(OH)3+ 3NaCl (1) Có thể có: NaOH + Al(OH)3 → NaAlO2 + 2H2O (2) nNaOH (TN1) = 0,65.2=1,3(mol) nNaOH (TN2) = 0,7.2=1,4(mol) nNaOH (TN1) = 1,3<nNaOH (TN2) = 1,4; lượng AlCl3 là như nhau; mà \({m_{Al{{(OH)}_3}(TN1)}} = 3b > {m_{Al{{(OH)}_3}(TN2)}} = 2b\) Nên xảy ra 2 trường hợp sau: Trường hợp 1: Ở thí nghiệm 1 chỉ xảy ra pư (1): NaOH hết, AlCl3 dư. Ở thí nghiệm 2 xảy ra 2 pư (1), (2): kết tủa Al(OH)3 tan một phần. + Xét TN1: \({n_{NaOH}} = 3{n_{Al{{(OH)}_3}}} \to 3.\frac{{3b}}{{78}} = 1,3 \to b = \frac{{169}}{{15}}\) + Xét TN2: Theo (1): \({n_{NaOH}} = 3{n_{AlC{l_3}}} = 3.0,4a = 1,2a\) Theo (2): \({n_{NaOH}} = {n_{Al{{(OH)}_3}}} = 0,4a - \frac{{2b}}{{78}} \to 1,2a + 0,4a - \frac{{2b}}{{78}} = 1,4\) → a= 19/18 Ta thấy: \({n_{AlC{l_3}}} = 0,4a = 0,422(mol);{n_{Al{{(OH)}_3}}} = \frac{{3b}}{{78}} = 0,433(mol) > {n_{AlC{l_3}}} = 0,422(mol)\) → Loại Trường hợp 2: Cả 2 thí nghiệm kết tủa Al(OH)3 đều tan một phần. + Xét TN1: \(\begin{gathered} + Xét TN2: Theo (1): \({n_{NaOH}} = 3{n_{AlC{l_3}}} = 3.0,4a = 1,2a\) Theo (2): \({n_{NaOH}} = {n_{Al{{(OH)}_3}}} = 0,4a - \frac{{2b}}{{78}} \to 1,2a + 0,4a - \frac{{2b}}{{78}} = 1,4\) \( \to 1,6a - \frac{{2b}}{{78}} = 1,4(II)\) Giải (I), (II) ta được a=1(M); b = 7,8(g) |