Bài 15. Phản ứng oxi hóa – khử trang 39, 40, 41 SBT Hóa 10 Kết nối tri thức với cuộc sốngSố oxi hoá là một số đại số đặc trưng cho đại lượng nào sau đây của nguyên tử trong phân tử? Trong hợp chất SO3, số oxi hoá của sulfur (lưu huỳnh) là Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Nhận biết 15.1 Số oxi hoá là một số đại số đặc trưng cho đại lượng nào sau đây của nguyên tử trong phân tử? A Hoá trị. B. Điện tích. C. Khối lượng. D. Số hiệu. Lời giải chi tiết: - Đáp án: B Nhận biết 15.2 Trong hợp chất SO3, số oxi hoá của sulfur (lưu huỳnh) là A. +2. B. +3. C. +5. D. +6. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của S - Trong SO3, ta có: x.1 + (-2).3 = 0 " x = +6 ð Đáp án: D Nhận biết 15.3 Fe2O3 là thành phần chính của quặng hematite đỏ, dùng để luyện gang. Số oxi hoá của iron (sắt) trong Fe2O3 là A. +3. B. 3+. C. 3. D. -3. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của Fe - Trong Fe2O3, ta có: x.2 + (-2).3 = 0 " x = +3 => Đáp án: A Nhận biết 15.4 Ammonia (NH3) là nguyên liệu để sản xuất nitric acid và nhiều loại phân bón. Số oxi hóa của nitrogen trong ammonia là A. 3. B. 0. C. +3. D. -3. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của N - Trong NH3, ta có: x.1 + (+1).3 = 0 " x = -3 => Đáp án: D Nhận biết 15.5 Chromium có số oxi hóa +2 trong hợp chất nào sau đây? A. Cr(OH)3. B. Na2CrO4. C. CrCl2. D. Cr2O3 Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của Cr - Trong Cr(OH)3, ta có: x.1 + (-1).3 = 0 " x = +3 - Trong Na2CrO4, ta có: (+1).2 + x.1 + (-2).4 = 0 " x = +6 - Trong CrCl2, ta có: x.1 + (-1).2 = 0 " x = +2 - Trong Cr2O3, ta có: x.2 + (-2).3 = 0 " x = +3 => Đáp án: C Nhận biết 15.6 Phản ứng oxi hoá - khử là phản ứng có sự nhường và nhận A. electron. B. neutron. C. proton. D. cation. Phương pháp giải: Dựa vào định nghĩa phản ứng oxi hóa - khử: là phản ứng hóa học, trong đó có sự chuyển dịch electron giữa các chất, phản ứng hay có sự thay đổi số oxi hóa của một số nguyên tử trong phân tử. Lời giải chi tiết: - Đáp án: A Nhận biết 15.7 Dấu hiệu để nhận ra một phản ứng oxi hoá - khử là dựa trên sự thay đổi đại lượng nào sau đây của nguyên tử? A. Số khối. B. Số oxi hoá. C. Số hiệu. D. Số mol. Phương pháp giải: Dựa vào định nghĩa phản ứng oxi hóa - khử: là phản ứng hóa học, trong đó có sự chuyển dịch electron giữa các chất, phản ứng hay có sự thay đổi số oxi hóa của một số nguyên tử trong phân tử. Lời giải chi tiết: - Đáp án: B Nhận biết 15.8 Trong phản ứng oxi hoá - khử, chất oxi hoá là chất A. nhường electron. B. nhận electron. C. nhận proton. D. nhường proton. Phương pháp giải: Dựa vào - Chất oxi hóa là chất nhận electron - Chất khử là chất nhường electron Lời giải chi tiết: - Đáp án: B Nhận biết 15.9 Dẫn khí H2 đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hoá học sau: CuO + H2 -> Cu + H2O. Trong phản ứng trên, chất đóng vai trò chất khử là A. CuO. B. Cu. C. H2. D. H2O. Phương pháp giải: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng -> Xác định chất oxi hóa, chất khử Lời giải chi tiết: - Dựa vào phương trình ta có: -> H2 là chất khử, CuO là chất oxi hóa -> Đáp án: C Nhận biết 15.10 Phản ứng nào sau đây là phản ứng oxi hoá - khử? Phương pháp giải: Phản ứng từ các đơn chất tạo thành hợp chất hoặc ngược lại chắc chắn xảy ra quá trình oxi hóa - khử Lời giải chi tiết: - Đáp án: A Thông hiểu 15.11 Cho các chất sau Cl2, HCl, NaCl, KClO3, HClO4. Số oxi hoá của nguyên tử Cl trong phân tử các chất trên lần lượt là A. 0; +1, +1; +5; +7. B. 0; -1; -1; +5; +7. C. 1; -1; -1; -5; -7. D. 0; 1; 1; 5; 7. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của Cl - Trong Cl2, ta có: x = 0 - Trong HCl, ta có: x.1 + (+1).1 = 0 " x = -1 - Trong NaCl, ta có: x.1 + (+1).1 = 0 " x = -1 - Trong KClO3, ta có: (+1).1 + x.1 + (-2).3 = 0 " x = +5 - Trong HClO4, ta có: (+1).1 + x.1 + (-2).4 = 0 " x = +7 => Đáp án: B Thông hiểu 15.12 Thuốc tím chứa ion permanganate (MnO4-) có tính oxi hoá mạnh, được dùng để sát trùng, diệt khuẩn trong y học, đời sống và nuôi trồng thuỷ sản. Số oxi hoá của manganese trong ion permanganate là A +2. B. +3. C. +7. D. +6. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của Mn - Trong MnO4-, ta có: x.1 + (-2).4 = -1 " x = +7 => Đáp án: C Thông hiểu 15.13 Cho các phân tử có công thức cấu tạo sau: Số oxi hoá của nguyên tử N trong các phân tử trên lần lượt là A. 0; -3; -4. B. 0; +3; +5. C. -3; -3; +4. D. 0; -3; +5. Phương pháp giải: Dựa vào các quy tắc xác định số oxi hóa - Quy tắc 1: Số oxi hóa của nguyên tử trong các đơn chất bằng 0 - Quy tắc 2: Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0 - Quy tắc 3: Trong các ion, số oxi hóa của nguyên tử (đối với ion đơn nguyên tử) hay tổng số oxi hóa các nguyên tử (đối với ion đa nguyên tử) bằng điện tích của ion đó - Quy tắc 4: + Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, trừ các hydride kim loại như (NaH, CaH2,…) + Số oxi hóa của oxygen bằng -2, trừ OF2 và các peroxide, superoxide như (H2O2, Na2O2, KO2,…) + Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1 + Kim loại kiềm thổ (nhóm IIA) luôn có số oxi hóa +2 + Nhôm (aluminium) có số oxi hóa +3 + Số oxi hóa của nguyên tử fluorine trong các hợp chất bằng -1 Lời giải chi tiết: - Đặt x là số oxi hóa của N - Trong N2, ta có: x = 0 - Trong NH3, ta có: x.1 + (+1).3 = 0 " x = -3 - Trong HNO3, ta có: (+1).1 + x.1 + (-2).3 = 0 " x = +5 => Đáp án: D Thông hiểu 15.14 Carbon đóng vai trò chất oxi hoá ở phản ứng nào sau đây? Phương pháp giải: Xác định số oxi hóa của các nguyên tử carbon trong các phản ứng " Phản ứng nào số oxi hóa của carbon giảm chứng tỏ trong phản ứng đó carbon đóng vai trò chất oxi hóa Lời giải chi tiết: Thông hiểu 15.15 Thực hiện các phản ứng hoá học sau Số phản ứng sulfur đóng vai trò chất oxi hoá là A. 4. B. 2. C. 3. D. 1. Phương pháp giải: Xác định số oxi hóa của các nguyên tử sulfur trong các phản ứng => Phản ứng nào số oxi hóa của sulfur giảm chứng tỏ trong phản ứng đó sulfur đóng vai trò chất oxi hóa Lời giải chi tiết: Thông hiểu 15.16 Khi tham gia các phản ứng đốt cháy nhiên liệu, oxygen đóng vai trò là A. chất khử. B. acid. C. chất oxi hóa. D. base. Lời giải chi tiết: Thông hiểu 15.17 Chlorine vừa đóng vai trò chất oxi hoá, vừa đóng vai trò chất khử trong phản ứng nào sau đây? Phương pháp giải: Xác định số oxi hóa của các nguyên tử chlorine trong các phản ứng " Phản ứng nào số oxi hóa của chlorine vừa tăng vừa giảm chứng tỏ trong phản ứng đó chlorine đóng vai trò vừa là chất khử, vừa là chất oxi hóa Lời giải chi tiết: Thông hiểu 15.18 Cho các phản ứng hoá học sau: Số phản ứng có kèm theo sự thay đổi số oxi hóa của các nguyên tử là A. 2. B. 3. C. 1. D. 4. Phương pháp giải: - Đáp án: C (phản ứng (b)) - Các phản ứng còn lại số oxi hóa của các nguyên tố không thay đổi Thông hiểu 15.19 Khi thiên nhiên nén (CNG - Compressed Natural Gas) có thành phần chính là methane (CH4), là nhiên liệu sạch, thân thiện với môi trường. Xét phản ứng đốt cháy methane trong buồng đốt động cơ xe buýt sử dụng nhiên liệu CNG: a) Xác định các nguyên tử có sự thay đổi số oxi hoá. Viết quá trình oxi hoá, quá trình khử. b) Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron.
Phương pháp giải: Dựa vào - Các bước cân bằng phản ứng oxi hóa - khử + Bước 1: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng => Xác định chất oxi hóa, chất khử + Bước 2: Viết quá trình oxi hóa và quá trình khử + Bước 3: Xác định (và nhân) hệ số thích hợp vào các quá trình sao cho tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận + Bước 4: Đặt các hệ số vào sơ đồ phản ứng. Cân bằng số lượng nguyên tử của các nguyên tố còn lại Lời giải chi tiết: Thông hiểu 15.20 Xét phản ứng sản xuất Cl2, trong công nghiệp: a) Xác định các nguyên tử có sự thay đổi số oxi hoá. Chỉ rõ chất oxi hoá, chất khử b) Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron. Phương pháp giải: Dựa vào - Các bước cân bằng phản ứng oxi hóa - khử + Bước 1: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng => Xác định chất oxi hóa, chất khử + Bước 2: Viết quá trình oxi hóa và quá trình khử + Bước 3: Xác định (và nhân) hệ số thích hợp vào các quá trình sao cho tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận + Bước 4: Đặt các hệ số vào sơ đồ phản ứng. Cân bằng số lượng nguyên tử của các nguyên tố còn lại Lời giải chi tiết: Vận dụng 15.21 Trên thế giới, zinc (kẽm) được sản xuất chủ yếu từ quặng zinc blende có thành phần chính là ZnS. Ở giai đoạn đầu của quá trình sản xuất, quặng zinc blende được nung trong không khi để thực hiện phản ứng: a) Xác định các nguyên tử có sự thay đổi số oxi hoá. Viết các quá trình oxi hoá, quá trình khử. b) Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron. Phương pháp giải: Dựa vào - Các bước cân bằng phản ứng oxi hóa - khử + Bước 1: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng => Xác định chất oxi hóa, chất khử + Bước 2: Viết quá trình oxi hóa và quá trình khử + Bước 3: Xác định (và nhân) hệ số thích hợp vào các quá trình sao cho tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận + Bước 4: Đặt các hệ số vào sơ đồ phản ứng. Cân bằng số lượng nguyên tử của các nguyên tố còn lại Lời giải chi tiết: Vận dụng 15.22 Khi đốt hoá lỏng thường gọi là gas, có thành phần gồm propane (C3H8) và butane (C4H10). Xét phản ứng đốt cháy butane khi đun bếp gas: C4H10 + O2 ->CO2 + H2O. a) Xác định các nguyên tử có sự thay đổi số oxi hoá. Chỉ rõ chất oxi hoá, chất khử. b) Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron Phương pháp giải: Dựa vào - Các bước cân bằng phản ứng oxi hóa - khử + Bước 1: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng => Xác định chất oxi hóa, chất khử + Bước 2: Viết quá trình oxi hóa và quá trình khử + Bước 3: Xác định (và nhân) hệ số thích hợp vào các quá trình sao cho tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận + Bước 4: Đặt các hệ số vào sơ đồ phản ứng. Cân bằng số lượng nguyên tử của các nguyên tố còn lại Lời giải chi tiết: Vận dụng 15.23 Hàm lượng iron(II) sulfate được xác định qua phản ứng oxi hoá - khử với potassium permanganate: FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O a) Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron Chi rõ chất oxi hóa, chất khử. b) Tính thể tích dung dịch KMnO4 0,02 M để phản ứng vừa đủ với 20 mL dung dịch FeSO4 0,10 M. Phương pháp giải: Dựa vào - Các bước cân bằng phản ứng oxi hóa - khử + Bước 1: Xác định số oxi hóa của các nguyên tử có sự thay đổi số oxi hóa trong phản ứng => Xác định chất oxi hóa, chất khử + Bước 2: Viết quá trình oxi hóa và quá trình khử + Bước 3: Xác định (và nhân) hệ số thích hợp vào các quá trình sao cho tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận + Bước 4: Đặt các hệ số vào sơ đồ phản ứng. Cân bằng số lượng nguyên tử của các nguyên tố còn lại Lời giải chi tiết: a) - Bước 1: \(\mathop {Fe}\limits^{ + 2} S{O_4} + K\mathop {Mn}\limits^{ + 7} {O_4} + {H_2}S{O_4} \to \mathop {F{e_2}}\limits^{ + 3} {\left( {S{O_4}} \right)_3} + {K_2}S{O_4} + \mathop {Mn}\limits^{ + 2} S{O_4} + {H_2}O\) => FeSO4 là chất khử, KMnO4 là chất oxi hóa - Bước 2: + Quá trình oxi hóa: \(2\mathop {Fe}\limits^{ + 2} \to 2\mathop {Fe}\limits^{ + 3} + 2.1e\) + Quá trình khử: \(\mathop {Mn}\limits^{ + 7} + 5e \to \mathop {Mn}\limits^{ + 2} \) - Bước 3:
- Bước 4: 10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O b) \({n_{FeS{O_4}}} = 0,1.0,02 = 0,002\)mol -> Theo phản ứng ta có: \({n_{KMn{O_4}}} = 0,002.2:10 = 0,0004\)mol -> \({V_{KMn{O_4}}} = \frac{{0,0004}}{{0,02}} = 0,02\)(L) = 20 (mL) Vận dụng 15.24 Cho 2,34 g kim loại M (hoá trị n) tác dụng với dung dịch H2SO4 (đặc, nóng, dư) thu được 3,2227 L khí SO2 (điều kiện chuẩn). Xác định kim loại M. Phương pháp giải: - Viết quá trình cho nhận electron - Áp dụng định luật bảo toàn electron: - Kẻ bảng xét hóa trị của M từ 1 đến 3 Lời giải chi tiết: - Ta có các quá trình cho nhận e như sau: \(\begin{array}{l}\mathop S\limits^{ + 6} + 2e \to \mathop S\limits^{ + 4} \\\quad 0,26 \leftarrow 0,13{\kern 1pt} \,(mol)\end{array}\) \(\begin{array}{l}\mathop M\limits^0 \to \mathop M\limits^{ + n} + ne\\\frac{{0,26}}{n} \leftarrow \,\;\,0,26\;(mol)\end{array}\) - Có \({n_{S{O_2}}} = \frac{{3,2227}}{{24,79}} = 0,13\)mol => n e nhận = 0,13.2 = 0,26 mol = n e cho => nM = \(\frac{{0,26}}{n}\) => MM = \(2,34:\frac{{0,26}}{n} = 9n\) - Ta có bảng giá trị:
=> Vậy kim loại M là aluminium (Al)
|














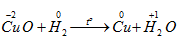
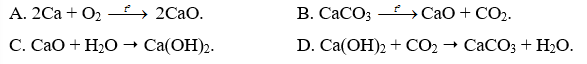
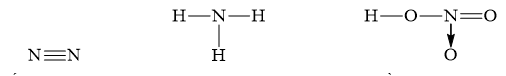
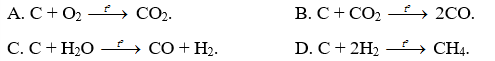
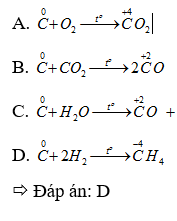

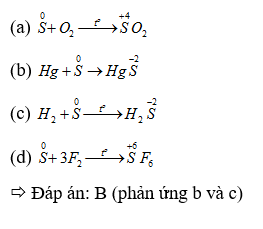

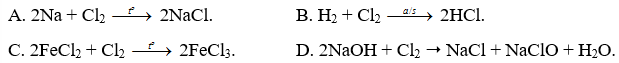
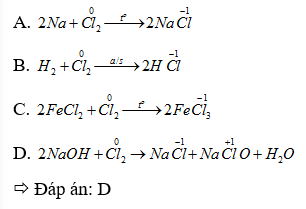
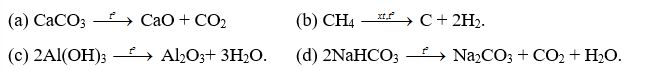
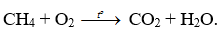
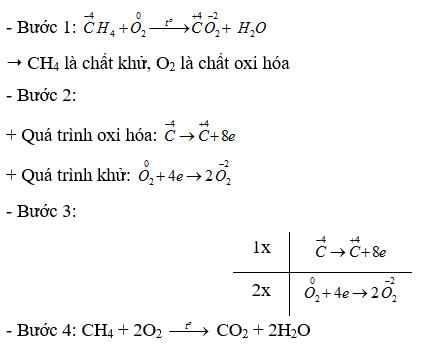
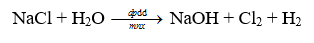
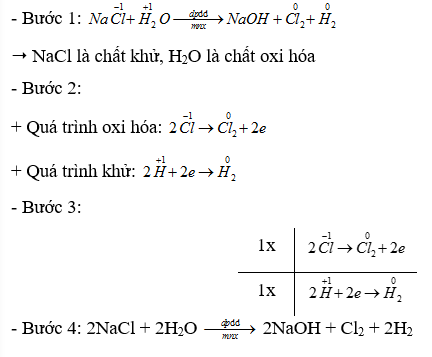
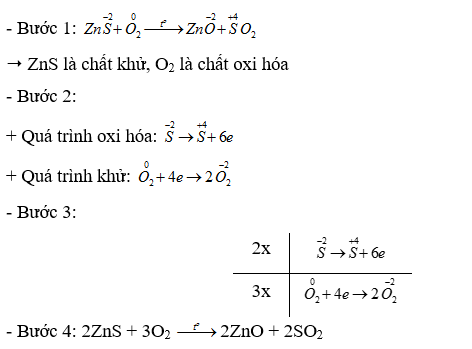
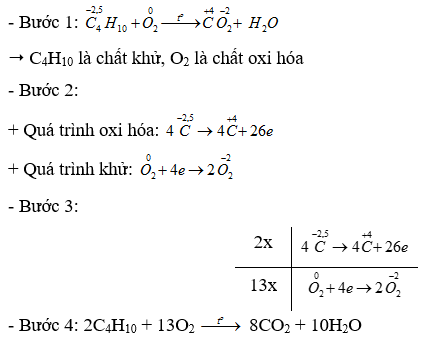






Danh sách bình luận