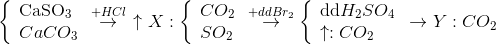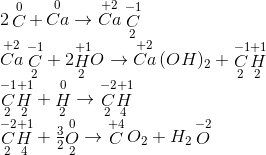40 câu hỏi lý thuyết về hợp chất của cacbon có lời giải (phần 2)Làm bàiQuảng cáo
Câu hỏi 1 : Dẫn CO (dư) qua hỗn hợp rắn X gồm: CuO, MgO, Fe3O4. Chất rắn thu được sau phản ứng (biết các phản ứng xảy ra hoàn toàn) là:
Đáp án: B Phương pháp giải: CO khử được các oxit của KL đứng sau Al trong dãy hoạt động hóa học của KL. Lời giải chi tiết: CO khử được các oxit của KL đứng sau Al trong dãy hoạt động hóa học của KL. Do đó các oxit CuO, Fe3O4 bị khử thành Cu và Fe; MgO không bị khử. Vậy các chất rắn thu được là Cu, Fe, MgO. Đáp án B Câu hỏi 2 : Khi nhiệt phân hỗn hợp chất rắn sau: (NH4)2CO3 , KHCO3, Mg(HCO3)2, FeCO3 đến khối lượng không đổi trong môi trường không có không khí thì sản phẩm rắn gồm các chất:
Đáp án: A Phương pháp giải: Nắm được phản ứng nhiệt phân muối cacbonat: - Muối cacbonat trung hòa của kim loại kiềm đều không bị nhiệt phân - Các muối cacbonat trung hòa của KL khác bị nhiệt phân thành oxit tương ứng và CO2 (trong muôi trường không có không khí) - Muối hidrocacbonat bị nhiệt phân (đến khối lượng không đổi): + Nếu là muối của KL kiềm: tạo muối cacbonat trung hòa, CO2, H2O + Nếu là muối của các KL khác: tạo oxit tương ứng, CO2, H2O - Muối amoni cacbonat nhiệt phân tạo NH3, CO2 , H2O Lời giải chi tiết: Nhiệt phân đến khối lượng không đổi: (NH4)2CO3 → 2NH3 + CO2 + H2O 2KHCO3 → K2CO3 + H2O + CO2 Mg(HCO3)2 → MgO + CO2 + H2O FeCO3 → FeO + CO2 Như vậy chất rắn sau phản ứng gồm: FeO, MgO, K2CO3 Đáp án A Câu hỏi 3 : Cho khí CO dư đi qua hỗn hợp rắn: MgO, CuO, Al2O3, Fe3O4 khi đun nóng thì chất rắn còn lại trong bình là
Đáp án: C Phương pháp giải: Các oxit của kim loại đứng sau nhôm mới bị khử bởi CO, H2, C, Al Lời giải chi tiết: Những oxit bị khử tạo KL là: CuO và Fe3O4 Chất rắn sau phản ứng gồm: MgO, Cu, Al2O3, Fe Đáp án C Câu hỏi 4 : Trong các cặp chất sau đây: a) C + H2O b) (NH4)2CO3 + KOH c) NaOH + CO2 d) CO2 + Ca(OH)2 e) K2CO3 + BaCl2 g) Na2CO3 + Ca(OH)2 h) CaCO3 + HCl i) HNO3 + NaHCO3 k) CO + CuO. Nhóm gồm các cặp chất mà phản ứng giữa các chất sinh ra sản phẩm khí là:
Đáp án: D Phương pháp giải: Dựa vào phản ứng hóa học giữa các chất để trả lời Lời giải chi tiết: a) C + H2O \(\xrightarrow{{{t^o}}}\) CO↑ + H2↑ C + 2H2O \(\xrightarrow{{{t^o}}}\) CO2↑ + 2H2↑ b) (NH4)2CO3 + 2KOH → 2NH3↑+ K2CO3 + 2H2O c) NaOH + CO2 → NaHCO3 2NaOH + CO2 → Na2CO3 + H2O d) 2CO2 + Ca(OH)2 → Ca(HCO3)2 CO2 + Ca(OH)2 → CaCO3↓ + H2O e) K2CO3 + BaCl2 → BaCO3↓ + 2KCl g) Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH h) CaCO3 + HCl → CaCl2 + H2O + CO2↑ i) HNO3 + NaHCO3 → NaNO3 + H2O + CO2↑ k) CO + CuO Cu + CO2↑ Vậy các phản ứng tạo khí là: a, b, h, i, k Đáp án D Câu hỏi 5 : Phương trình ion rút gọn của phản ứng giữa dung dịch HCl và dung dịch Na2CO3 là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: 2HCl + Na2CO3 → H2O + 2NaCl + CO2 Đáp án B Câu hỏi 6 : Dẫn luồng khí CO qua hổn hợp Al2O3, CuO, MgO, Fe2O3 (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Câu hỏi 7 : Cho phản ứng : $$CO{\rm{ }} + {\rm{ }}{I_2}{O_5}{\rm{ }}\buildrel {{t^0}} \over \longrightarrow {\rm{ }}{{\rm{I}}_2}{\rm{ }} + {\rm{ }}?$$ Sản phẩm còn thiếu trong phản ưng là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án: B Dễ thấy chất tham gia phản ứng có cacbon vì vậy loại ngay phương án C. D. Chất tham gia còn có oxi => chỉ có thể là CO2 Câu hỏi 8 : Dẫn luồng khí CO qua hổn hợp Al2O3, MgO, Fe2O3,CuO (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án: A Chú ý: CO chỉ khử được các oxit kim loại đứng sau Al Câu hỏi 9 : Thổi khí CO2 dư vào dung dịch Ca(OH)2, muối thu được là
Đáp án: A Phương pháp giải: Viết PTHH, xác định muối thu được. Lời giải chi tiết: Vì CO2 dư nên lượng CO2 nhiều do vậy xảy ra phản ứng: 2CO2 + Ca(OH)2 → Ca(HCO3)2 Đáp án A Câu hỏi 10 : CO2 không phản ứng với chất nào trong các chất sau đây?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án B Câu hỏi 11 : Tiến hành hai thí nghiệm sau: Thí nghiệm 1: Cho từ từ từng giọt HCl cho đến dư vào dung dịch Na2CO3 và khuấy đều. Thí nghiệm 2: Cho từ từ từng giọt Na2CO3 cho đến dư vào dung dịch HCl và khuấy đều. Kết luận rút ra là:
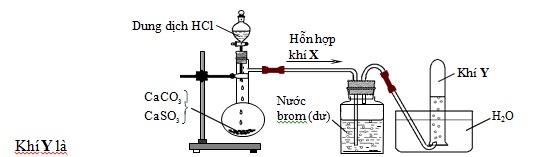
Đáp án: B Phương pháp giải: Dạng bài: Muối Cacbonat, Hidrocacbonat + H+ - TH1 : Nếu Cho từ từ muối (CO32- và HCO3-) vào dung dịch axit => Do ban đầu H+ rất dư so với muối nên 2 muối đều phản ứng đồng thời CO32- + 2H+ -> CO2 + H2O HCO3- + H+ -> CO2 + H2O - TH2 : Nếu cho từ từ H+ vào dung dịch muối (CO32- và HCO3-) => Do ban đầu H+ thiếu nên phản ứng với CO32- trước : CO32- + H+ -> HCO3- HCO3- + H+ -> CO2 + H2O - TH3 : Trộn nhanh 2 dung dịch axit và muối => Không biết chất nào phản ứng với chất nào trước => Xét cả 2 trường hợp TH1 và TH2 => Lấy giá trị trong khoảng. Lời giải chi tiết: Thí nghiệm 1: Cho từ từ H+ vào CO32- CO32- + H+ → HCO3- HCO3- + H+ → CO2 + H2O => Ban đầu chưa có khí, một lúc sau thấy khí thoát ra. Thí nghiệm 2: Cho từ từ CO32- vào H+ CO32- + 2H+ → CO2 + H2O => Xuất hiện bọt khí ngay lập tức. Đáp án B Câu hỏi 12 : Hình vẽ sau đây mô tả thí nghiệm điều chế và thu khí Y từ hỗn hợp rắn gồm CaCO3 và CaSO3:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Ta có sơ đồ sau
Đáp án C Câu hỏi 13 : Dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Thực hiện các thí ngiệm sau TN1: cho (a+b)mol CaCl2 vào dd X. TN2: cho (a+b) mol Ca(OH)2 vào dd X Khối lượng kết tủa thu được trong 2 TN là
Đáp án: B Phương pháp giải: Lời giải chi tiết:
TN1: Ca2+ + CO32- → CaCO3 a+b b b TN2: OH- + HCO3- → CO32- + H2O 2(a+b) a a Ca2+ + CO32- → CaCO3 a+b b+a b +a Đáp án B Câu hỏi 14 : Một dung dịch có chứa các ion sau . Để tách được nhiều cation ra khỏi dung dịch mà không đưa thêm ion mới vào thì ta có thể cho dung dịch tác dụng với dung dịch nào sau đây?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Dùng Na2CO3 do CO32- kết tủa được các ion Ba2+, Ca2+, Mg2+ và phản ứng với H+ sinh ra khí Đáp án B Câu hỏi 15 : Có 5 lọ mất nhãn đựng 5 chất bột màu trắng: NaCl, Na2CO3, Na2SO4, BaCO3, BaSO4. Chỉ dùng nước và khí CO2 thì có thể nhận được mấy chất
Đáp án: D Phương pháp giải: Lời giải chi tiết: - Hòa tan vào nước + 2 mẫu không tan là BaCO3 và BaSO4 + 3 mẫu còn lại đều tan. - Sục CO2 vào 2 mẫu không tan + Mẫu tan là BaCO3 BaCO3 + CO2 + H2O → Ba(HCO3)2 + Mẫu không tan là BaSO4 + Xuất hiện 2 kết tủa là Na2CO3, Na2SO4 + 1 không có hiện tượng gì là NaCl + Có kết tủa => chất ban đầu là BaCO3 => chất ban đầu là Na2CO3 Đáp án D Câu hỏi 16 : Liên kết hóa học trong phân tử CO2 là loại liên kết gì?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: Liên kết C=O trong phân tử CO2 là liên kết cộng hóa trị có cực nhưng do có cấu tạo thẳng nên CO2 là phân tử không có cực => Loại liên kết hóa học của nó vẫn là liên kết cộng hóa trị có cực Đáp án B Câu hỏi 17 : Khẳng định nào sau đây không đúng?
Đáp án: B Phương pháp giải: Lời giải chi tiết: C là phi kim có tính khử nên không tác dụng được với kim loại Đáp án B Câu hỏi 18 : Hiện tượng hóa học xảy ra khi sục từ từ đến dư khí CO2 vào dung dịch nước vôi trong là:
Đáp án: B Phương pháp giải: Lời giải chi tiết:
Câu hỏi 19 : Cho các thí nghiệm sau: (1) Sục từ từ đến dư khí CO2 vào dung dịch nước vôi trong. (2) Sục CO2 vào dung dịch Ba(OH)2 dư. (3) Sục 2a mol CO2 vào 2a mol dung dịch Ba(OH)2. (4) Sục 2a mol SO2 vào a mol Ca(OH)2. Số thí nghiệm thu được kết tủa là
Đáp án: B Phương pháp giải: Lời giải chi tiết:
Câu hỏi 20 : Dẫn luồng khí CO qua hỗn hợp Al2O3, CuO, MgO, Fe2O3 đun nóng, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là:
Đáp án: A Phương pháp giải: Chỉ những oxit của KL đứng sau Al trong dãy hoạt động hóa học bị khử bởi CO hoặc H2 Lời giải chi tiết: CuO và Fe2O3 bị CO khử ở nhiệt độ cao theo PTHH: CuO + CO → Cu + CO2 Fe2O3 + 3CO → 2Fe + 3CO2 Như vậy chất rắn thu được sau phản ứng gồm: Al2O3, Cu, MgO, Fe Đáp án A Câu hỏi 21 : Chất được dùng để chữa bệnh đau dạ dày là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Khi nồng độ axit HCl trong dạ dày vượt mức cho phép sẽ gây đau dạ dày. Người ta thường sử dụng thuốc muối có thành phần chính là NaHCO3 để chữa do phản ứng sau: NaHCO3 + HCl → NaCl + CO2 + H2O Đáp án D Câu hỏi 22 : Dẫn luồng khí CO dư qua hỗn hợp CuO, Al2O3, CaO, MgO có số mol bằng nhau (nung nóng ở nhiệt độ cao) thu được chất rắn A. Hòa tan A vào nước dư còn lại chất rắn X. X gồm:
Đáp án: D Phương pháp giải: CO chỉ khử được các oxi kim loại từ Al trở về sau trong dãy điện hóa Các oxit bazo của kim loại kiềm, kiềm thổ (trừ Be, Mg) tan được trong nước Lời giải chi tiết: \(CO\,du + \left\{ \matrix{ CO + Cu \(\buildrel {{t^0}} \over\longrightarrow \)Cu + H2O CaO + H2O → Ca(OH)2 Ca(OH)2 + Al2O3 → Ca(AlO2)2 + H2O Vì các chất ban đầu có cùng số mol nên Al2O3 phản ứng hết với dd Ca(OH)2. Do vậy chất rắn sau phản ứng chỉ có Cu và MgO Đáp án D Câu hỏi 23 : Dẫn khí CO (dư) đi qua hỗn hợp gồm Al2O3, FeO, CuO ở nhiệt độ cao đến phản ứng hoàn toàn, thu được chất rắn X. Để hòa tan hết X có thể dùng dung dịch (loãng, dư) nào sau đây?
Đáp án: A Phương pháp giải: CO chỉ khử được các oxit của kim loại đứng sau Al trong dãy điện hóa, từ đó xác định được rắn X và chọn dd (loãng, dư) để hòa tan hết X cho phù hợp Lời giải chi tiết: CO dư qua Al2O3, FeO, CuO ở nhiệt độ cao đến phản ứng hoàn toàn, thu được rắn X là: Al2O3, Fe và Cu Để hòa tan hết rắn X ta dùng dung dịch HNO3 Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O Đáp án A Câu hỏi 24 : Trên bề mặt của vỏ trứng gia cầm có những lỗ nhỏ nên vi khuẩn có thể xâm nhập được và hơi nước, cacbon đioxit có thể thoát ra làm trứng nhanh hỏng. Để bảo quản trứng lâu hỏng, người ta thường nhúng trứng vào dung dịch Ca(OH)2, phản ứng hóa học xảy ra trong quá trình này là
Đáp án: C Phương pháp giải: Lời giải chi tiết: Ca(OH)2 có thể phản ứng với CO2 trong không khí tạo CaCO3 lấp đầy những lỗ nhỏ li ti đó. PTHH: Ca(OH)2 + CO2 → CaCO3 ↓ + H2O. Đáp án C Câu hỏi 25 : Vào mùa lạnh người ta thường sử dụng than để sưởi ấm, tuy nhiên có nhiều trường hợp bị ngộ độc dẫn đến tử vong do hít phải một hàm lượng đủ lớn khí X (không màu, không mùi, hơi nhẹ hơn không khí). Chất khí X và biện pháp tránh bị ngộ độc khi sử dụng than để sưởi ấm lần lượt là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Chất khí độc dẫn đến tử vong nhẹ hơn không khí là CO do CO có ái tính với hemoglobin trong máu mạnh hơn, ngăn cản hemoglobin vận chuyển oxi trong máu. → Biện pháp: Không dùng trong phòng kín mà phải để cửa thoáng. Đáp án D Câu hỏi 26 : Hiệu ứng nhà kính là hiện tượng Trái đất đang ấm dần lên, do các bức xạ có bước sóng dài trong vùng hồng ngoại bị giữ lại, mà không bức xạ ra ngoài vũ trụ. Chất khí là nguyên nhân chủ yếu gây nên hiệu ứng nhà kính là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Khí CO2 là nguyên nhân chính gây ra hiện tượng hiệu ứng nhà kính. Đáp án D Câu hỏi 27 : Phản ứng nào sau đây không xảy ra?
Đáp án: D Phương pháp giải: - Muối cacbonat tan không bị nhiệt phân (trừ muối amoni), muối cacbonat không tan bị nhiệt phân \(MgC{O_3}\xrightarrow{{{t^0}}}MgO + C{O_2}\) - Tất cả các muối hiđrocacbonat đều bị nhiệt phân \(2HCO_3^ - \xrightarrow{{{t^0}}}CO_3^{2 - } + C{O_2} + {H_2}O\) Lời giải chi tiết: Na2CO3 là muối cacbonat tan nên không bị nhiệt phân Đáp án D Câu hỏi 28 : Hợp chất nào sau đây của cacbon dùng làm thuốc giảm đau dạ dày do thừa axit?
Đáp án: C Phương pháp giải: Lý thuyết về các hợp chất của cacbon. Lời giải chi tiết: NaHCO3 được dùng làm thuốc đau dạ dày do thừa axit. Đáp án C Câu hỏi 29 : Sản phẩm lần lượt tạo thành khi sục từ từ CO2 đến dư vào nước vôi trong là
Đáp án: C Phương pháp giải: Viết phương trình hóa học của phản ứng và kết luận Lời giải chi tiết: Sục từ từ khí CO2 đến dư vào nước vôi trong, phản ứng lần lượt xảy ra là: \(C{O_2} + Ca{(OH)_2} \to CaC{{\rm{O}}_3} + {H_2}O\) \(C{O_2} + {H_2}O + CaC{{\rm{O}}_3} \to Ca{(HC{O_3})_2}\) Đáp án C Câu hỏi 30 : Cho sơ đồ chuyển hóa sau: C -> CaC2 -> C2H2 -> C2H4 -> CO2 Điều nhận định nào sau đây đúng:
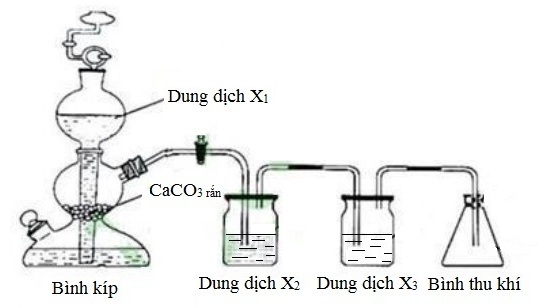
Đáp án: B Phương pháp giải: Viết các PTHH, xác định số oxi hóa. Lời giải chi tiết: => Có 3 phản ứng oxi hóa khử Đáp án B Câu hỏi 31 : Khí CO2 được điều chế trong phòng thí nghiệm có lẫn X1 và hơi nước, để làm sạch khí CO2 người ta bố trí như hình bên. Cho các nhận định sau:
(a) X1 là HCl. (b) X2, X3 lần lượt là NaHCO3 và H2SO4 đặc. (c) X2, X3 lần lượt là H2SO4 đặc và NaHCO3. (d) X2 có vai trò giữ lại hidroclorua. (e) X3 có vai trò làm khô khí CO2. Số nhận định đúng là
Đáp án: A Phương pháp giải: Lời giải chi tiết: (a) đúng (b) đúng, NaHCO3 giữ lại HCl, H2SO4 giữ lại hơi nước từ đó ta thu được CO2 khô (c) sai, vì nếu X3 là NaHCO3 thì CO2 sẽ bị lẫn hơi nước (d) đúng, X2 là NaHCO3 giữ lại HCl (e) đúng, H2SO4 đặc giữ lại H2O để làm khô khí CO2 Vậy có 4 phát biểu đúng Đáp án A Câu hỏi 32 : Cho các thí nghiệm sau: (1) Sục khí CO2 tới dư vào dung dịch Ca(OH)2. (2) Sục khí CO2 tới dư vào dung dịch NaAlO2. (3) Cho dung dịch Na2CO3 vào dung dịch AlCl3. (4) Cho NaHSO4 vào dung dịch Ba(HCO3)2. (5) Cho dung dịch NaHCO3 vào dung dịch BaCl2. (6) Cho dung dịch NaHCO3 vào dung dịch Ba(OH)2. Số thí nghiệm thu được kết tủa sau khi kết thúc phản ứng là:
Đáp án: D Phương pháp giải: Dựa vào tính chất hóa học của các hợp chất của cacbon để viết các phương trình hóa học xảy ra. Lời giải chi tiết: (1) CO2 + Ca(OH)2 → CaCO3↓ + H2O CO2 + CaCO3 + H2O → Ca(HCO3)2 (2) CO2 + NaAlO2 + H2O → Al(OH)3 ↓ + NaHCO3 (3) 3Na2CO3 + 2AlCl3 + 6H2O → 2Al(OH)3↓ (keo trắng) + 3CO2↑ + 6NaCl (4) 2NaHSO4 + Ba(HCO3)2 → BaSO4 ↓ + Na2SO4 + 2CO2 + 2H2O (5) Không xảy ra phản ứng (6) 2NaHCO3 + Ba(OH)2 → BaCO3 ↓ + Na2CO3 + 2H2O Vậy có 4 thí nghiệm thu được kết tủa sau phản ứng là thí nghiệm (2), (3), (4) và (6). Đáp án D Câu hỏi 33 : Oxit Y của một nguyên tố X ứng với hóa trị II có thành phần phần trăm theo khối lượng của X là 42,86%. Có các phát biểu sau: (1) Y là khí không màu, không mùi, không vị, tan nhiều trong nước, là khí rất độc. (2) Y là oxit axit. (3) Ở nhiệt độ cao, Y có thể khử được nhiều oxit kim loại. (4) Y có thể được điều chế trực tiếp từ phản ứng giữa X nung đỏ và hơi nước. (5) Từ axit fomic có thể điều chế được Y. Số phát biểu đúng là:
Đáp án: A Phương pháp giải: Từ % khối lượng của X trong oxit Y ta tìm được nguyên tố X và xác định được công thức oxit Y. Dựa vào tính chất vật lí, tính chất hóa học và phương pháp điều chế để xác định số phát biểu đúng. Lời giải chi tiết: Oxit Y của một nguyên tố X ứng với hóa trị II có công thức là XO. Ta có: %X = \(\frac{X}{{X + 16}}.100\% = 42,86\% \) Giải phương trình trên ta có X = 12, suy ra X là C, công thức oxit Y là CO. (1) sai vì khí CO rất ít tan trong nước. (2) sai vì CO là oxit trung tính, không phải là oxit axit. (3) đúng vì ở nhiệt độ cao, CO có thể khử được nhiều oxit của kim loại đứng sau Al. (4) đúng vì CO có thể được điều chế trực tiếp từ phản ứng giữa than (C) nung đỏ và hơi nước. C + H2O \(\xrightarrow{{{t^0}}} \) CO + H2 (5) đúng vì HCOOH \(\xrightarrow{{{H_2}S{O_4}dac,{t^0}}}\) CO + H2O Vậy có 3 phát biểu đúng. Đáp án A Câu hỏi 34 : : Cho 4 lọ dung dịch riêng biệt X, Y, Z, T chứa các chất khác nhau trong số 4 chất: (NH4)2CO3, NaHCO3, NaNO3, NH4NO3. Thực hiện nhận biết 4 dung dịch trên bằng dung dịch Ba(OH)2 thu được kết quả sau
Nhận xét nào sau đây là đúng?
Đáp án: C Phương pháp giải: Lời giải chi tiết: PTHH khi cho 4 chất tác dụng với dung dịch Ba(OH)2 là: \(\begin{gathered} NaNO3 không phản ứng với dung dịch Ba(OH)2. Z là NaNO3. Đáp án C Câu hỏi 35 : Có 4 lọ dung dịch riêng biệt X, Y, Z, T chứa các chất khác nhau trong 4 chất sau: (NH4)2CO3, KHCO3, NaNO3, NH4NO3. Bằng cách dùng dung dịch Ca(OH)2 cho lần lượt vào từng dung dịch, thu được kết quả: 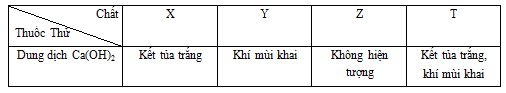
Nhận xét nào sau đây đúng:
Đáp án: B Phương pháp giải: Tính chất hóa học của các chất vô cơ Lời giải chi tiết: X + Ca(OH)2 tạo kết tủa và không tạo khí => X là KHCO3 Ca(OH)2 + 2KHCO3 → CaCO3 + K2CO3 + 2H2O Y + Ca(OH)2 chỉ tạo khí => Y là NH4NO3 Ca(OH)2 + 2NH4NO3 → Ca(NO3)2 + 2NH3 + 2H2O Z + Ca(OH)2 không có hiện tượng => Z là NaNO3 T + Ca(OH)2 tạo khí và kết tủa => (NH4)2CO3 Ca(OH)2 + (NH4)2CO3 → CaCO3 + 2NH3 + 2H2O Đáp án B Câu hỏi 36 : Cho hỗn hợp khí X gồm CO2, CO, N2 và hơi nước lần lượt đi qua các bình mắc nối tiếp chứa lượng dư mỗi chất: CuO đun nóng; dung dịch nước vôi trong; dung dịch H2SO4 đặc.Giả thiết các phản ứng xảy ra hoàn toàn. Khí ra khỏi bình chứa H2SO4 đặc là
Đáp án: D Phương pháp giải: Dựa vào kiến thức tính chất hóa học của các khí CO2, CO, N2 để xác định xem qua bình nào thì khí nào bị giữ lại, khí nào bị thoát ra. Lời giải chi tiết: Cho hỗn hợp khí X qua CuO, t0 có CO bị giữ lại CO + CuO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + CO2↑ Khí đi ra gồm: CO2 và N2. Hỗn hợp khí này cho qua dd Ca(OH)2 thì CO2 sẽ bị giữ lại CO2 + Ca(OH)2 → CaCO3↓ + H2O Khí thoát ra là hơi H2O và N2. Cho hỗn hợp khí này qua dd H2SO4 đặc thì H2O bị giữ lại (do H2SO4 đặc có tính háo nước mạnh) => khí thoát ra khỏi bình chứa H2SO4 đặc là N2. Đáp án D Câu hỏi 37 : Cho các phát biểu sau: (1) Nguyên nhân ngộ độc khi sưởi ấm bằng than trong phòng kín chủ yếu do khí CO2. (2) Trong các mặt nạ chống độc người ta thường cho bột than hoạt tính. (3) Ure là loại phân đạm tốt nhất có công thức là (NH2)2CO. (4) Thuốc nổ đen (người Trung Quốc tìm ra) là hỗn hợp: KNO3 + S + C. (5) Tinh thể Al2O3 có lẫn tạp chất Fe2+, Fe3+ và Ti4+ ta có đá saphia dùng làm đồ trang sức. Số phát biểu đúng là
Đáp án: D Phương pháp giải: Dựa vào kiến thức tổng hợp các chất vô cơ Lời giải chi tiết: (1) sai do khí CO chứ không phải CO2 (2) đúng, vì than hoạt tính có tính hấp phụ (3) đúng, vì ure có hàm lượng nito cao nhất nhé (4) đúng (5) đúng → có 4 phát biểu đúng Đáp án D Câu hỏi 38 : Cho các chất: AgNO3; Cu(NO3)2, MgCO3, Ba(HCO3)2, NH4HNO3, NH4NO3, và Fe(NO3)2. Nếu nung các chất trên đến khối lượng không đổi trong các bình kín không có không khí, rồi cho nước vào bình, số bình có thể tạo lại chất ban đầu sau các thí nghiệm là
Đáp án: C Phương pháp giải: Lời giải chi tiết: \(\begin{gathered} Vậy có 5 chất là: AgNO3, Cu(NO3)2, CaCO3, Ba(HCO3)2, NH4HCO3 Đáp án C Câu hỏi 39 : Hòa tan hoàn toàn hỗn hợp gồm MgO, Zn(OH)2, Al, FeCO3, Cu(OH)2, Fe trong dung dịch H2SO4 loãng dư, sau phản ứng thu được dung dịch X. Cho vào dung dịch X một lượng Ba(OH)2 dư thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi thu được hỗn hợp chất rắn Z, sau đó dẫn luồng khí CO dư (ở nhiệt độ cao) từ từ đi qua Z đến khi phản ứng xảy ra hoàn toàn thu được chất rắn G. Trong G chứa:
Đáp án: A Phương pháp giải: Dựa vào tính chất hóa học của các chất để viết các phương trình hóa học xảy ra. Từ đó xác định được thành phần dung dịch X, kết tủa Y, chất rắn Z. Dựa vào tính chất khử oxit kim loại ở nhiệt độ cao để xác định thành phần chất rắn G. Lời giải chi tiết: Sơ đồ phản ứng: \(\left\{ \begin{array}{l}MgO\\Zn{\left( {OH} \right)_2}\\Al\\FeC{O_3}\\Cu{\left( {OH} \right)_2}\\Fe\end{array} \right.\)\(\overset{+{{H}_{2}}S{{O}_{4}}loangdu}{\mathop{\to }}\,\)\({\rm{dd}}X\left\{ \begin{array}{l}MgS{O_4}\\ZnS{O_4}\\A{l_2}{(S{O_4})_3}\\FeS{O_4}\\CuS{O_4}\\{H_2}S{O_4}\end{array} \right.\)\(\overset{+Ba{{(OH)}_{2}}du}{\mathop{\to }}\,\)\(\left\{ \begin{array}{l}Mg{(OH)_2}\\Fe{(OH)_2}\\Cu{(OH)_2}\\BaS{O_4}\end{array} \right.\)\(\overset{+{{O}_{2}},{{t}^{o}}}{\mathop{\to }}\,\)\(\left\{ \begin{array}{l}MgO\\F{e_2}{O_3}\\CuO\\BaS{O_4}\end{array} \right.\)\(\overset{+CO,{{t}^{o}}}{\mathop{\to }}\,\)\(\left\{ \begin{array}{l}MgO\\Fe\\Cu\\BaS{O_4}\end{array} \right.\) Vậy chất rắn G gồm MgO, Fe, Cu và BaSO4. Lưu ý Zn(OH)2 và Al(OH)3 tan trong dung dịch kiềm dư. Đáp án A Câu hỏi 40 : Từ hai muối X và Y thực hiện các phản ứng sau: X \(\xrightarrow{{{t^0}}} \) X1 + CO2 X1 + H2O → X2 X2 + Y → X + Y1 + H2O X2 + 2Y → X + Y2 + 2H2O Hai muối X, Y tương ứng là:
Đáp án: D Phương pháp giải: Do X nhiệt phân thu được sản phẩm X1 có khả năng phản ứng với nước nên X là BaCO3 hoặc CaCO3 → X2 là kiềm Do X2 + Y tạo ra X nên Y là muối CO32-- hoặc HCO3- Do X2 tác dụng với Y theo 2 tỉ lệ khác nhau nên Y phải là muối HCO3- Kết hợp các dữ kiện trên ta xác định được 2 muối X và Y. Lời giải chi tiết: Do X nhiệt phân thu được sản phẩm X1 có khả năng phản ứng với nước nên X là BaCO3 hoặc CaCO3 → X2 là kiềm. Do X2 + Y tạo ra X nên Y là muối CO32- hoặc HCO3- Do X2 tác dụng với Y theo 2 tỉ lệ khác nhau nên Y phải là muối HCO3- Vậy X là CaCO3, Y là NaHCO3 PTHH: CaCO3 \(\xrightarrow{{{t^0}}} \) CaO + CO2 CaO + H2O → Ca(OH)2 Ca(OH)2 + NaHCO3 → CaCO3 + NaOH + H2O Ca(OH)2 + 2 NaHCO3 → CaCO3 + Na2CO3 + 2H2O Đáp án D Quảng cáo
|