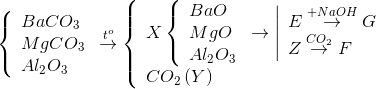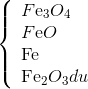40 bài tập lý thuyết về hợp chất của cacbon có lời giải (phần 1)Làm bàiQuảng cáo
Câu hỏi 1 : Khí nào sau đây là khí độc:
Đáp án: B Phương pháp giải: Lời giải chi tiết: CO là khí rất độc, chỉ cần một lượng nhỏ khí CO có thể gây tử vong. Đáp án B Câu hỏi 2 : Trong công nghiệp CO được điều chế bằng phương pháp nào
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 3 : Sự hình thành thạch nhũ trong các hang động đá vôi là nhờ phản ứng hoá học nào sau đây?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Câu hỏi 4 : Thành phần chính của khí than ướt là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Thành phần chính của khí than ướt là: CO, CO2, H2, N2. Đáp án A Câu hỏi 5 : Phản ứng nào sau đây không xảy ra
Đáp án: D Phương pháp giải: Lời giải chi tiết: Muối cacbonat của kim loại kiềm không bị nhiệt phân Đáp án D Câu hỏi 6 : ’’Nước đá khô’’ không nóng chảy mà thăng hoa nên được dùng để tạo môi trường lạnh và khô rất tiện cho việc bảo quản thực phẩm. Nước đá khô là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Câu hỏi 7 : Khí B có tính chất: rất độc, không màu, ít tan trong nước, cháy trong không khí sinh ra chất khí làm đục nước vôi trong. Khí B là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án: B Câu hỏi 8 : CO khử được oxit kim loại nào trong các oxit sau :
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án: A CO khử được các oxit từ Mg trở về sau trong dãy điện hóa Câu hỏi 9 : Dẫn khí CO qua đồng(II) oxit nung nóng đỏ. Phản ứng xảy ra hoàn toàn, sản phẩm thu được là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: \(CO{\rm{ }} + {\rm{ }}CuO{\rm{ }}\buildrel {{t^0}} \over \longrightarrow {\rm{ }}Cu{\rm{ }} + {\rm{ }}C{O_2}\) Vậy sản phẩm thu được là Cu, CO2. Đáp án B Câu hỏi 10 : Phát biểu nào đúng trong các phát biểu sau ?
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án: C Các số oxi hóa của cacbon là -4 ; 0; +2 ;+4. Chất chỉ có tính khử nếu nó có số oxi hóa thấp nhất, chất chỉ có tính oxi hóa nếu nó có số oxi hóa cao nhất. Chất có cả tính khử và tính oxi hóa nếu có số oxi hóa trung gian. $$\mathop C\limits^0 ;{\rm{ }}\mathop C\limits^{ + 2} O$$ có số oxi hóa trung gian => có cả tính khử và tính oxi hóa. Câu hỏi 11 : Không thể dùng CO2 để dập tắt đám cháy của chất nào sau đây ?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án: B Vì CO2 cháy được trong Mg theo phương trình:
$$C{O_2}{\rm{ }} + {\rm{ }}2Mg{\rm{ }}\buildrel {{t^0}} \over \longrightarrow {\rm{ }}2MgO{\rm{ }} + {\rm{ }}C$$ Do vậy với các đám cháy Mg ta nên dùng cát để dập cháy chứ không dùng bình cứu hỏa CO2 Câu hỏi 12 : Muối cacbonat nào sau đây không bị nhiệt phân?
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 13 : Cho các muối sau NaHCO3, Na2CO3, Ca(HCO3)2, CaCO3, FeCO3 và MgCO3. Số muối bị phân hủy ở nhiệt độ cao:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Trừ Na2CO3 Đáp án A Câu hỏi 14 : Cho các chất: O2 (1),Cl2 (2), Al2O3 (3), Fe2O3 (4), HNO3 (5), HCl (6), CaO (7), H2SO4 đặc (8), ZnO (9), PbCl2 (10). Cacbon monooxit phản ứng trực tiếp được với bao nhiêu chất?
Đáp án: A Phương pháp giải: Lời giải chi tiết: (1) CO + 1/2O2 Đáp án A Câu hỏi 15 : Để phòng nhiễm độc CO, là khí không màu, không mùi, rất độc người ta dùng chất hấp thụ là
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Câu hỏi 16 : C và CO thể hiện tính khử trong phản ứng oxi – hóa khử khi:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án: A Mẹo: khử- cho; O -lấy ;bị gì sự ấy. Tức chất khử là chất nhường e, chất oxi hóa là chất nhận e. nhường e, số oxi hóa tăng sau phản ứng. Câu hỏi 17 : Khí nào sau đây là nguyên nhân chính gây nên hiệu ứng nhà kính:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án: B Hiệu ứng nhà kính là hiện tượng trái đất nóng lên do bức xạ mặt trời chiếu xuống trái đất nhưng bị các khí hấp thụ (CO2 + hơi nước…) giữ lại trong bầu không khí => làm cho nhiệt độ bầu không khí bao quanh khí quyển tăng lên. Lớp khí CO2 có tác dụng như một lớp kính giữ nhiệt lượng tỏa ngược vào vũ trụ của Trái Đất trên quy mô toàn cầu. Câu hỏi 18 : Cho các chất: O2 (1),NaOH (2), Mg (3), Na2CO3 (4), SiO2 (5), HCl (6), CaO (7), Al (8), ZnO (9), H2O (10), NaHCO3 (11), KMnO4 (12), HNO3 (13), Na2O (14). Cacbon đioxit phản ứng trực tiếp được với bao nhiêu chất?
Đáp án: B Phương pháp giải: Lời giải chi tiết: (2) CO2 + NaOH →NaHCO3 Đáp án B Câu hỏi 19 : Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Trong dung dịch G chứa
Đáp án: B Phương pháp giải: Lời giải chi tiết:
E tác dụng với NaOH => Al2O3 còn dư => Ba(OH)2 hết => G chứa NaOH và NaAlO2 Đáp án B Câu hỏi 20 : Nhận định nào sau đây đúng
Đáp án: D Phương pháp giải: Phương pháp: * Tính chất vật lý của muối cacbonat - Trạng thái: rắn , tinh thể - Tính tan: + HCO3-: tan + CO32-: muối cacbonat của kim loại kiềm, amoni tan, còn lại không tan Lời giải chi tiết:
Hướng dẫn giải: A. Muối hidrocacbonat đều tan => đúng B. Muối cacbonat đều là chất rắn ở trạng thái tinh thể=> đúng C. Muối cacbonat của kim loại kiềm, amoni tan, còn lại không tan => đúng Đáp án D Câu hỏi 21 : Nhiệt phân muối hidrocacbonat tạo ra sản phẩm là
Đáp án: B Phương pháp giải: Hướng dẫn giải: 2 HCO3- -> CO32- + H2O+ CO2 => Nhiệt phân muối hidrocacbonat tạo ra muối cacbonat, CO2, H2O Lời giải chi tiết:
Đáp án B Câu hỏi 22 : Hiện tượng khi cho từ từ dung dịch Ca(OH)2 vào dung dịch Ca(HCO3)2
Đáp án: B Phương pháp giải: Phương pháp: Ca(OH)2 + Ca(HCO3)2 → 2CaCO3 + 2H2O Lời giải chi tiết:
Hướng dẫn giải: Ca(OH)2 + Ca(HCO3)2 → 2CaCO3 + 2H2O => xuất hiện kết tủa trắng Đáp án B Câu hỏi 23 : Hiện tượng khi cho từ từ dung dịch HCl vào dung dịch Ca(HCO3)2
Đáp án: A Phương pháp giải: Phương pháp: 2HCl + Ca(HCO3)2 → CaCl2 + 2CO2 +2 H2O Lời giải chi tiết:
Hướng dẫn giải: 2HCl + Ca(HCO3)2 → CaCl2 + 2CO2 +2 H2O => Xuất hiện chất khí Đáp án A Câu hỏi 24 : Dung dịch muối X làm quỳ tím hóa xanh, dung dịch muối Y không làm quỳ tím đổi màu. Trộn X và Y thấy có kết tủa. X, Y là cặp nào sau đây
Đáp án: C Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: A. NaOH, K2SO4. Không tạo kết tủa => loại B. NaOH, FeCl3. FeCl3 làm quỳ đổi đỏ => loại C. Na2CO3, BaCl2. Na2CO3 làm quỳ đổi xanh, BaCl2 không đổi màu quỳ, tạo kết tủa BaCO3 => thỏa mãn D. K2CO3, NaCl. Không tạo kết tủa => loại Đáp án C Câu hỏi 25 : Trong các nhận định sau đây, nhận định nào đúng 1. CO2 là chất khí, không màu, không mùi, không vị 2. CO2 là nhẹ hơn không khí 3. CO2 ít tan trong nước 4. CO2 tan nhiều trong nước 5. CO2 là chất khí không duy trì sự cháy sự sống
Đáp án: A Phương pháp giải: Phương pháp: *Tính chất vật lí của CO2 - Chất khí không màu , không mùi, không vị - Tan ít trong nước - Nặng hơn không khí - Không duy trì sự cháy, sự sống Lời giải chi tiết:
Hướng dẫn giải 1. CO2 là chất khí, không màu, không mùi, không vị => đúng 2. CO2 là nhẹ hơn không khí => sai ( CO2 nặng hơn không khí MCO2 =44, Mkk=29) 3. CO2 ít tan trong nước => Đúng 4. CO2 tan nhiều trong nước => Sai 5. CO2 là chất khí không duy trì sự cháy sự sống => Đúng =>1,3,5 đúng Đáp án A Câu hỏi 26 : Khí CO2 điều chế trong phòng thí nghiệm thường lẫn khí HCl.Để loại bỏ HCl ra khỏi hỗn hợp,ta dùng
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: Để loại bỏ khí HCl ta phải dùng dung dịch NaHCO3 bão hòa vì HCl + NaHCO3 NaCl + Na2CO3 => Có thể dùng dung dịch NaHCO3 bão hòa để tinh chế khí CO2 Đáp án B Câu hỏi 27 : Có thể phân biệt khí CO2 và khí SO2 bằng chất nào sau đây
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: A. Cả 2 khí đều phản ứng với H2O =>dung dịch trong suốt => không phân biệt được B. Chỉ có SO2 làm mất màu dung dịch brom, còn CO2 thì không phản ứng SO2 + Br2 + 2H2O H2SO4 + 2HBr => dùng để phân biệt CO2 và SO2 C. Cả CO2 và SO2 đều phản ứng với dung dịch NaOH => dung dịch trong suốt => không phân biệt được D. CO2 và SO2 đều phản ứng với dung dịch Ba(OH)2 tạo kết tủa trắng giống nhau => không phân biệt được Đáp án B Câu hỏi 28 : Trong các nhận định sau đây, nhận định nào đúng 1. CO là chất khí, không màu, không mùi, không vị 2. CO là chất khí độc 3. CO ít tan trong nước 4. CO tan nhiều trong nước 5. CO là chất khí có mùi sốc
Đáp án: A Phương pháp giải: Phương pháp: * Tính chất vật lý của CO - Là chất khí không màu, không mùi, không vị - Độc - Ít tan trong nước Lời giải chi tiết:
Hướng dẫn giải: CO là chất khí không màu, không mùi, không vị, độc,ít tan trong nước => 1,2,3 đúng, 4,5 sai Đáp án A Câu hỏi 29 : Khử Fe2O3 bằng CO thu được hỗn hợp rắn. Hỗn hợp rắn có thể chứa tối đa bao nhiều chất?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: Fe2O3 + CO -> CO2 +hỗn hợp rắn có thể có Đáp án B Câu hỏi 30 : Cho khí CO dư đi qua ống sứ đựng CuO, FeO, Al2O3,Fe2O3 nung nóng thu được chất rắn có chứa (biết các phản ứng xảy ra hoàn toàn)
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải: CO khử oxit của kim loại đứng sau Al => Al2O3 không bị khử , CuO, FeO, Fe2O3 bị khử hoàn toàn thành kim loại Fe, Cu. => chất rắn gồm: Al2O3, Fe, Cu Đáp án B Câu hỏi 31 : Cho các chất khí O2; N2; CO2; CO. Chất độc là:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Câu hỏi 32 : Một trong những nguyên nhân gây tử vong trong nhiều vụ cháy là do nhiễm độc khí X. Khi vào cơ thể, khí X kết hợp với hemoglobin, làm giảm khả năng vận chuyển oxi của máu. Khí X là:
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Câu hỏi 33 : Một chất Y có tính chất sau: - Không màu, rất độc. - Cháy trong không khí với ngọn lửa màu xanh và sinh ra chất khí làm đục nước vôi trong. Y là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: CO là khí có những tính chất thỏa mãn với đề bài: - Không màu, rất độc - Cháy trong không khí với ngọn lửa màu xanh và sinh ra khí làm đục nước vôi trong: 2CO + O2 → 2CO2 (nhiệt độ) CO2 + Ca(OH)2 → CaCO3 + H2O Đáp án B Câu hỏi 34 : Nhận định nào sau đây là đúng?
Đáp án: A Phương pháp giải: Lời giải chi tiết: A đúng B sai vì các muối cacbonat của KL kiềm bền với nhiệt, không bị nhiệt phân C sai vì các muối cacbonat của KL kiềm tan được trong nước D sai vì hầu hết các muối cacbonat đều không tan trừ các muối cacbonat của KL kiềm Đáp án A Câu hỏi 35 : Cho các chất sau: CuO, O2, dung dịch Ca(OH)2, FeO. Số chất tác dụng được với CO (đun nóng) là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: CuO + CO \(\buildrel {{t^0}} \over\longrightarrow \) Cu + CO2 2CO + O2 \(\buildrel {{t^0}} \over\longrightarrow \) 2CO2 CO + FeO \(\buildrel {{t^0}} \over\longrightarrow \) Fe + CO2 => Có 3 chất phản ứng được với CO (đun nóng) Đáp án C Câu hỏi 36 : Khí X thoát ra khi đốt than trong lò, đốt xăng dầu trong động cơ, gây ngộ độc hô hấp cho người và vật nuôi do làm giảm khả năng vận chuyển oxi của máu. X là
Đáp án: A Phương pháp giải: Lời giải chi tiết: CO là khí thoát ra khi đốt than trong lò, đốt xăng dầu trong động cơ, gây ngộ độc hô hấp cho người và vật nuôi do làm giảm khả năng vận chuyển oxi của máu. Đáp án A Câu hỏi 37 : Ở nhiệt độ cao, khí CO khử được oxit nào sau đây?
Đáp án: A Phương pháp giải: CO, H2 khử được những oxit của KL đứng sau Al trong dãy hoạt động hóa học. Lời giải chi tiết: CO, H2 khử được những oxit của KL đứng sau Al trong dãy hoạt động hóa học. Vậy nên CO khử được CuO. Đáp án A Câu hỏi 38 : Oxit nào sau đây không tạo muối?
Đáp án: B Phương pháp giải: Oxit không tạo muối là các oxit trung tính như NO, CO, N2O. Lời giải chi tiết: Oxit không tạo muối là oxit trung tính → Oxit này là CO Đáp án B Câu hỏi 39 : Cho khí CO dư đi qua hỗn hợp gồm CuO, MgO, PbO và Al2O3 nung nóng đến phản ứng hoàn toàn thu được hỗn hợp rắn A. Chất rắn A gồm:
Đáp án: A Phương pháp giải: CO + oxit kim loại (sau Al) \(\overset{t^{o}}{\rightarrow}\) Kim loại + CO2 Lời giải chi tiết: Ta có: CuO + CO \(\overset{t^{o}}{\rightarrow}\) CO2 + Cu MgO + CO \(\overset{t^{o}}{\rightarrow}\) không phản ứng PbO + CO \(\overset{t^{o}}{\rightarrow}\) Pb + CO2 Al2O3 + CO \(\overset{t^{o}}{\rightarrow}\) không phản ứng → Chất rắn sau phản ứng thu được gồm: Cu, Pb, MgO và Al2O3 Đáp án A Câu hỏi 40 : Công thức CaCO3 tương ứng với thành phần hoá học chính của loại đá nào sau đây?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đá vôi có thành phần hóa học chính là CaCO3. Đáp án B Quảng cáo
|














 CO2
CO2