Câu hỏi:
Hệ số cân bằng của \(C{u_2}S\) và \(HN{O_3}\) trong phản ứng \(C{u_2}S + HN{O_3} \to Cu{(N{O_3})_2} + {H_2}S{O_4} + NO + {H_2}O\) là:
- A 3 và 22
- B 3 và 18
- C 3 và 10
- D 3 và 12
Phương pháp giải:
Phương pháp cân bằng phương trình phản ứng bằng phương pháp thăng bằng e
Nguyên tắc: Dựa vào định luật bảo toàn e, số e mà chất khử nhường bằng số e chất oxi hóa nhận.
cân bằng theo 4 bước
- Bước 1: Xác định số oxi hóa của các nguyên tố có số oxi hóa thay đổi
- Bước 2: Viết các quá trình oxi hóa, quá trình khử.
- Bước 3: Nhân các hệ số thích hợp để cân bằng số e cho – nhận
- Bước 4: Đặt hệ số chất oxi hóa, chất khử vào sơ đồ phản ứng. Cân bằng các nguyên tố theo thứ tự:
Kim loại (cation) – gốc axit (anion) – môi trường (axit, bazơ) – cân bằng số nguyên từ H – cân bằng số nguyên tử hiđro.)
Lời giải chi tiết:
Sơ đồ phản ứng \(\overbrace {C{u_2}S}^0 + H\mathop {{\text{ }}N}\limits^{ + 5} {O_3} \to \mathop {Cu}\limits^{ + 2} {(N{O_3})_2} + {H_2}\mathop {{\text{ }}S}\limits^{ + 6} {O_4} + \mathop {{\text{ }}N}\limits^{ + 2} O + {H_2}O\)
Các quá trình oxi hóa – khử
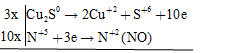
\(3C{u_2}S + 22HN{O_3} \to 6Cu{(N{O_3})_2} + 3{H_2}S{O_4} + 10NO + 8{H_2}O\)
Hệ số cân bằng của \(C{u_2}S\) và \(HN{O_3}\) lần lượt là 3 và 22
Đáp án A


















