Lý thuyết quá trình đẳng nhiệt. Định luật Bôi-lơ - Ma-ri-ốtTrạng thái và quá trình biến đổi trạng thái Quảng cáo
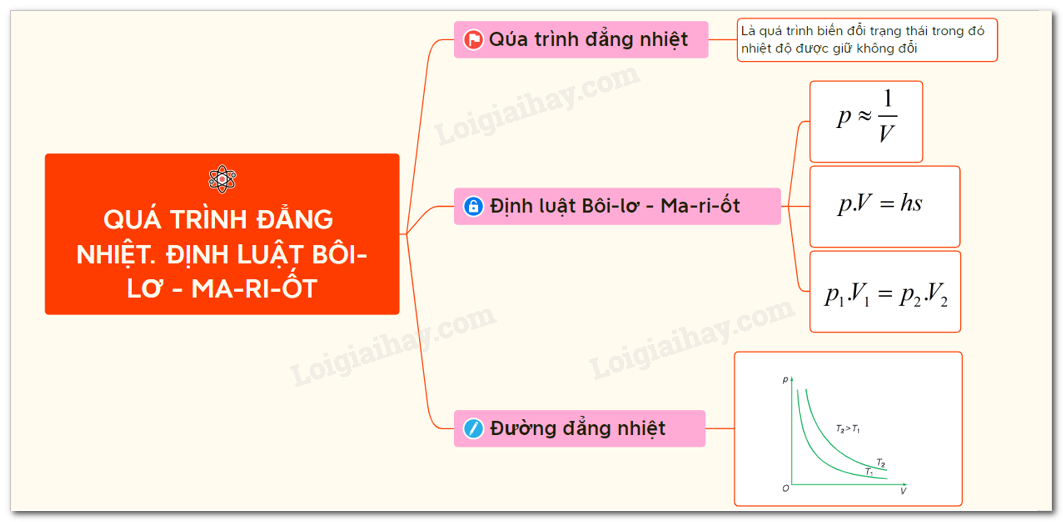
I - TRẠNG THÁI VÀ QUÁ TRÌNH BIẾN ĐỔI TRẠNG THÁI - Trạng thái của một lượng khí được xác định bằng các thông số: V (thể tích), p (áp suất) và T (nhiệt độ tuyệt đối). - Lượng khí có thể chuyển từ trạng thái này sang trạng thái khác bằng các quá trình biến đổi trạng thái - Khi một thông số trạng thái không đổi ta gọi đó là các đẳng quá trình + Áp suất không đổi: Quá trình đẳng áp + Thể tích không đổi: Quá trình đẳng tích + Nhiệt độ không đổi: Quá trình đẳng nhiệt II - ĐỊNH LUẬT BÔI-LƠ - MA-RI-ỐT 1. Quá trình đẳng nhiệt Quá trình đẳng nhiệt là quá trình biến đổi trạng thái trong đó nhiệt độ được giữ không đổi. 2. Định luật Bôilơ - Mariốt Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích. \(p \sim \frac{1}{V} \to pV = h/s\) III - ĐƯỜNG ĐẲNG NHIỆT Đường biểu diễn sự biến thiên của áp suất theo thể tích khi nhiệt độ không đổi gọi là đường đẳng nhiệt. 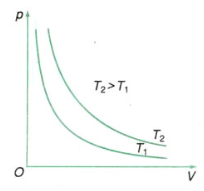 Trong hệ tọa độ (p,V) đường đẳng nhiệt là đường hypebol Sơ đồ tư duy về quá trình đẳng nhiệt. Định luật Bôi-lơ - Ma-ri-ốt
|




















Danh sách bình luận