Lý thuyết Hợp kim - Sự ăn mòn kim loại - Hóa 12 Cánh diềuHợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim. Quảng cáo
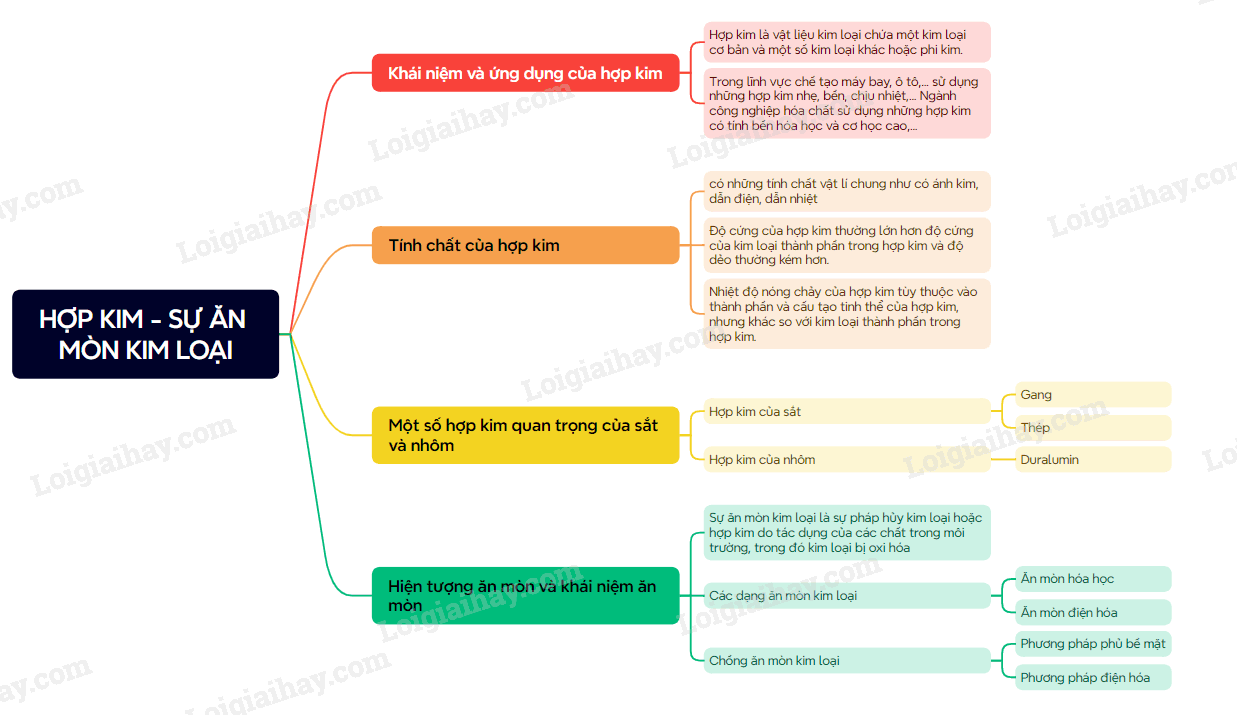
I. Hợp kim 1. Khái niệm hợp kim và việc sử dụng phổ biến của hợp kim - Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim. Ví dụ: thép là hợp kim, trong đó kim loại cơ bản là sắt, phu kim là carbon và một số kim loại như chromium, nickel,… - Hợp kim thường khó bị oxi hóa và có một số tính chất đáp ứng được nhiều mục đích sử dụng khác nhau. Vì vậy trong thực tế, hợp kim được sử dụng phổ biến hơn kim loại. 2. Tính chất của hợp kim - Tính chất hóa học của hợp kim thường tương tự tính chất hóa học của các đơn chất thành phần tham gia tạo hợp kim. - Tính chất vật lí và tính chất cơ học của hợp kim thường khác nhiều so với tính chất của các đơn chất thành phần tham gia tạo hợp kim. 3. Một số hợp kim của sắt và nhôm a) Hợp kim của sắt hầu hết các hợp kim của sắt là thép. Các loại thép có thành phần khác nhau nên tính chất và ứng dụng khác nhau. Ví dụ: - Fe và C tạo thép thường, có độ cứng và độ dẻo phù hợp để làm vật liệu trong ngành xây dựng, giao thông và cơ khí. - Fe, C, Cr và Ni tạo thép không giả, được dùng làm vật liệu chế tạo dao, kéo, dụng cụ phẫu thuật,… - Gang là hợp kim của sắt và carbon, trong đó có hàm lượng C lớn hơn so với thép. Gang có độ cứng cao nhưng giòn nên khó gia công hơn thép. b) Hợp kim của nhôm - Đặc điểm nổi bật nhất của hợp kim nhôm là nhẹ. - Duralumin (hay dural) là loại hợp kim quan trọng nhất của nhôm, có thành phần gồm nhôm, đồng, magnesium, manganese,…được sử dụng nhiều trong lĩnh vực hàng không vũ trụ để chế tạo cánh máy bay; lĩnh vực quốc phòng để chế tạo áo giáp khiên bảo vệ; lĩnh vực chế tạo ô tô,… II. Ăn mòn kim loại 1. Hiện tượng ăn mòn và khái niệm ăn mòn Sự ăn mòn kim loại là sự pháp hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa: M \( \to \) Mn+ + ne 2. Các dạng ăn mòn kim loại a) Ăn mòn hóa học Ăn mòn hóa học là quá trình oxi hóa – khử, trong đó các electron của kim loại chuyển trực tiếp đến các chất trong môi trường. b) Ăn mòn điện hóa Ăn mòn điện hóa là quá trình ăn mòn kim loại do sự tạo thành pin điện hóa. Điều kiện xảy ra sự ăn mòn điện hóa 1. Có hai kim loại khác nhau hoặc kim loại với phi kim,… 2. Tiếp xúc trực tiếp với nhau hoặc gián tiếp qua dây dẫn điện 3. Cùng tiếp xúc với một dung dịch chất điện li Thiếu một trong ba điều kiện trên sẽ không xảy ra sự ăn mòn điện hóa 3. Chống ăn mòn kim loại a) Phương pháp phủ bề mặt Phương pháp bảo vệ bề mặt là phủ lên bề mặt của kim loại một lớp sơn, dầu, mỡ, chất dẻo hoặc tráng, mạ bằng một kim loại khác. b) Phương pháp điện hóa Trong phương pháp điện hóa, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hóa học mạnh hơn. SƠ ĐỒ TƯ DUY
|




















Danh sách bình luận