Bài 11. Phương trình trạng thái của khí lí tưởng trang 32, 33, 34 SBT Vật lí 12 Kết nối tri thứcTrong hiện tượng nào sau đây cả ba thông số trạng thái của một lượng khí để thay đổi? Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
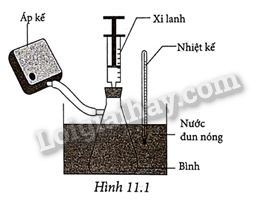
11.1 Trong hiện tượng nào sau đây cả ba thông số trạng thái của một lượng khí để thay đổi? A. Không khí bị đun nóng trong một bình kín. B. Không khí bên trong quả bóng bàn bị bẹp được nhúng vào nước phồng lên như cũ. C. Không khí trong một quả bóng bay bị em bé bóp bẹp. D. Cả ba hiện tượng trên. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Không khí bên trong quả bóng bàn bị bẹp được nhúng vào nước phồng lên như cũ. Đáp án: B 11.2 Biểu thức nào sau đây phù hợp với phương trình trạng thái của khí lí tưởng? A. \(\frac{P}{V}\)= hằng số. B.\(pV \sim \frac{1}{T}\). C. \(pV = nRT.\) D. \(pV\sim\frac{1}{t}\). Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Phương trình trạng thái của khí lí tưởng:\(pV = nRT.\) Đáp án: C 11.3 Phương trình nào sau đây không phải là phương trình Clapeyron? A. \(\frac{{pV}}{T} = nR.\) B. \(pV = \frac{m}{M}RT.\) C. \(\frac{{pV}}{T} = \)hằng số D. \(pV = nRT.\) Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Phương trình Clapeyron gồm: \(\frac{{pV}}{T} = nR\);\(pV = \frac{m}{M}RT\];\[pV = nRT\) Đáp án: C 11.4 Nên dùng phương trình Clapeyron để xác định các thông số trạng thái của chất khí trong trường hợp nào sau đây? Tại sao? a) Khí trong quả bóng thám không đang bay lên cao. b) Không khí trong quả bóng bàn bị bẹp được nhúng vào nước nóng. c) Khí trong bọt khí đang nổi lên trong một ấm đun nước khi nước sắp sôi. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Trường hợp (b) và (c). Vì trong các trường hợp này, khối lượng khí không đổi. 11.5 Hãy chứng tỏ rằng với dụng cụ vẽ ở Hình 11.1, người ta có thể làm thí nghiệm kiểm chứng phương trình trạng thái của một lượng khí không đổi: \(\frac{{pV}}{T} = \)hằng số
Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Với dụng cụ này có thể đồng thời đo độ lớn của V, p và T. Từ đó tính được \(\frac{{pV}}{T}\)luôn không đổi. 11.6 Trong SGK Vật lí của một số nước, phương trình trạng thái của khí lí tưởng được xây dựng từ phương trình của quá trình đẳng nhiệt và phương trình của quá trình đẳng tích. 1. Hãy dùng cách trên để xây dựng phương trình trạng thái của khí lí tưởng. 2. Theo em thì cách này có thể có những ưu điểm nào, nhược điểm nào so với Bài viết cách dùng trong SGK của chúng ta. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: 1. Trong quá trình đẳng nhiệt, \(pV = \)hằng số Trong quá trình đẳng tích, \(\frac{p}{T} = \) hằng số Ta có thể viết phương trình trạng thái khí lý tưởng: \(pV = nRT.\) Trong đó: – R là hằng số khí lý tưởng. – n là số mol của khí. – T là nhiệt độ tuyệt đối (Kelvin). 2. Về mặt phương pháp thì hai cách làm là tương đương nhau. Tuy nhiên, cách dùng quá trình đẳng tích có ưu điểm hơn cách dùng quá trình đẳng áp ở chỗ thí nghiệm về quá trình đẳng tích dễ thực hiện hơn nhiều so với thí nghiệm về quá trình đẳng áp. 11.7 Xác định khối lượng riêng của không khí trên đỉnh Fansipan cao 3140 m trong dãy Hoàng Liên Sơn, biết mỗi khi lên cao 10 m thì áp suất khí quyển giảm 1 mmHg và nhiệt độ trên đỉnh núi này là 2 °C. Biết khối lượng riêng ở điều kiện chuẩn (0 °C và 760 mmHg) của khí quyển là 1,29 kg/m3. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết:
Ta có: \(D = \frac{m}{V}\) Áp dụng phương trình trạng thái của lí tưởng: \(\frac{{{p_1}{V_0}}}{{{T_1}}} = \frac{{{p_2}V}}{{{T_2}}} \Rightarrow \frac{{{p_1}m}}{{{T_1}{D_1}}} = \frac{{{p_2}m}}{{{T_2}{D_2}}} \Rightarrow {D_2} = \frac{{{D_1}{p_2}{T_1}}}{{{p_1}{T_2}}} = \frac{{1,29.446.273}}{{760.275}} = 0,75(kg/{m^3})\)
11.8 Một bạn bơm một quả bóng bay bằng khí He. Sau khi bơm 0,25 mol khí ở nhiệt độ 298 K vào bóng thì áp suất khí trong bong bóng là 1,20.103 Pa. Hỏi bóng có bị vỡ không nếu bơm thêm 0,15 mol He ở cùng nhiệt độ trên vào bóng? Biết vỏ bóng chỉ chịu được áp suất tối đa là 1,50.105 Pa, sau khi bơm 0,25 mol khí, thể tích của bóng không tăng khi tiếp tục bơm thêm khí vào bóng.
Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Bóng sẽ bị vỡ vì p2 = 1,92.105 Pa.
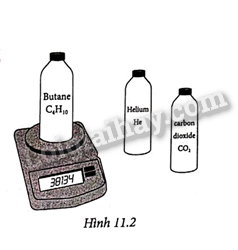
Thể tích của bóng bằng: \({V_1} = \frac{{{n_1}R{T_1}}}{{{p_1}}} = \frac{{0,25.8,31.298}}{{{{1,2.10}^3}}} \approx 0,517({m^3})\) Vì thể tích không thay đổi, ta có thể tính áp suất mới bằng cách sử dụng phương trình khí lý tưởng: \({p_2} = \frac{{{n_2}R{T_2}}}{V} = \frac{{0,4.8,31.298}}{{0,517}} \approx {1,92.10^3}(Pa)\) 11.9 Có ba chai thuỷ tinh giống nhau (khối lượng và dung tích bằng nhau) đựng các chất khí khác nhau ( He, C4H10, CO2 ) ở cùng nhiệt độ 20 °C và áp suất 1,913.105 Pa. Các chai đựng khí được cân bằng cân điện tử. Kết quả cân được ghi trong hàng thứ 2 bảng dưới. 1. Tính các giá trị còn trống trong bảng, biết khối lượng của chai khi chưa chứa khí là 378,68 g. 2. So sánh các số liệu tìm được trong hàng cuối. Có phải chúng ta có thể dự đoán được kết quả so sánh này không? Tại sao? 3. Hãy dùng phương trình trạng thái của khí lí tưởng để tìm lại các giá trị của n trong bảng.
Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết:
2. Số mol trong các chai bằng nhau. Có thể tiên đoán được dựa trên phương trình: \(pV = nRT\) 3. Hướng dẫn cách làm. Ví dụ với chai chứa CO2. – Dựa vào thể tích của 1 mol khí CO2 ở điều kiện chuẩn để xác định thể tích của một mol khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa), từ đó suy ra thể tích của 2,02 g khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa). – Áp dụng phương trình \[pV = nRT\]cho khí CO2 với các dữ liệu V tính ở trên (V=0,58 lít = 0,58.103 m3; T = 293 K; p = 1,913.105 Pa và R = 8,31 để tính n. 11.10 Một tàu ngầm dùng để nghiên cứu biển đang lặn ở độ sâu 100 m. Người ta mở một bình dung tích 60 lít chứa khí ở áp suất 107 Pa và nhiệt độ 27 °C để đẩy nước ra khỏi thùng chứa nước ở giữa hai lớp vỏ của tàu làm cho tàu nổi lên. Sau khi dãn nở, nhiệt độ của khí là 3 °C. Tính thể tích nước bị đẩy ra khỏi tàu. Coi khối lượng riêng của nước biển là 1 000 kg/m3; gia tốc trọng trường là 9,81 m/s2, áp suất khí quyển là 1,013.105 Pa. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: Áp dụng định luật Bôi-lơ-Ma-ri-ốt: \({p_1}{V_1} = {p_2}{V_2} \Rightarrow {p_2} = \frac{{{p_1}{V_1}}}{{{V_2}}} = \frac{{{{10}^7}.60}}{{{V_2}}}\) Áp suất tuyệt đối của khí trong bình sau khi dãn nở:\(p{'_2} = {p_2} + {p_o} = \frac{{{{10}^7}.60}}{{{V_2}}} + {1,013.10^5}\) Áp suất do nước biển tác dụng lên tàu ở độ sâu 100m: \({p_n} = {p_o} + Dgh = {1,013.10^5} + 1000.9,81.100 = {1,09.10^6}(Pa)\) Áp suất do nước biển tác dụng lên tàu bằng áp suất của khí trong bình sau khi dãn nở: \({p_n} = p{'_2} \Leftrightarrow {1,09.10^6} = \frac{{{{10}^7}.60}}{{{V_2}}} + {1,013.10^5} \Rightarrow {V_2} = 54,6(l)\) Thể tích nước bị đẩy ra khỏi tàu: \(V = {V_1} - {V_2} = 60 - 54,6 = 5,4(l)\) 11.11 Người ta bơm 10 m3 không khí nóng ở nhiệt độ T = 300 K vào một khinh khí cầu. Nhiệt độ và áp suất của khí quyển lúc này là T = 279 K và po = 1,00 bar. Khối lượng khí cầu là 240 kg. Khi đó, khinh khí cầu chưa thể bay lên được. a) Tính lượng không khí chứa trong khinh khí cầu. Biết muốn khí cầu bay lên chỉ cần tăng nhiệt độ của không khí trong khí cầu mà không cần bơm thêm không khí vào hoặc lấy bớt không khí ra. Coi đây là quá trình đẳng áp; nhiệt dung riêng đẳng áp của không khí là ra không khí là \({c_{mp}} = 7\frac{R}{2}\);hằng số khí lí tưởng R = 8,31 J/mol.K và khối lượng mol của không khí MA = 29 g/mol. b) Tính thể tích của khí cầu để nó có thể bắt đầu bay lên. c) Tính nhiệt cấp cho khí cầu để đun nóng không khí. (Trích đề thi Olympic Vật lí Thụy Sĩ 1996) Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: a) Lượng không khí trong khí cầu khi chưa bay lên: \(n = \frac{{{p_o}{V_o}}}{{R{T_1}}} = {4,01.10^4}(mol)\) Khối lượng không khí trong khí cầu khi chưa bay lên: \({m_{kk}} = {1,16.10^3}{\rm{ }}kg\) Khối lượng của cả khí cầu: \({m_{kc}} = 240{\rm{ }}kg + {1,16.10^3}kg = {1,40.10^3}kg.\) b) Trạng thái của không khí trong khí cầu khi chưa bay lên: \(({p_1} = {p_o};{V_1} = {V_o} = 1000{m^3};{T_1} = 300K)\) Trạng thái của không khí trong khí cầu khi bay lên: \(({p_2} = {p_o};{V_2} = ?;{T_2} = ?)\) Coi khi bay lên lực đẩy Archimede bằng trọng lượng của khí cầu: \({F_A} = P \Rightarrow {D_o}g{V_2} = {m_{kc}}g\) (1) Từ phương trình trạng thái của khí lí tưởng: \({p_o}{V_o} = {n_o}R{T_o}\) và công thức tính khối lượng riêng của không khí: \({D_o} = \frac{m}{{{V_o}}} = \frac{{nM}}{{{D_o}}} \to {D_o} = \frac{{{p_o}M}}{{R{T_o}}} = 1,25(kg/{m^3})\) Từ (1) rút ra \({V_2} = \frac{{{T_2}}}{{{T_1}}} = \frac{{{{1,4.10}^3}}}{{1,25}} = {1,12.10^3}({m^3})\) 3. Vì số mol n và áp suất p của không khí trong khí cầu không đổi nên đây là quá trình đẳng áp của một lượng khí không đổi: \(\begin{array}{l}\frac{{{T_2}}}{{{T_1}}} = \frac{{{V_2}}}{{{V_1}}} = 1,12 \Rightarrow {T_2} = 336(K)\\Q = n{c_p}\Delta T = n\frac{7}{2}R\Delta T = {4,2.10^7}(J)\end{array}\) 11.12 Về bóng thám không vô tuyến (Radiosonde) Ngày nay, trong ngành khí tượng, người ta dùng bóng thám không vô tuyến có mang các thiết bị cảm biến khí tượng, thiết bị vô tuyến điện và ở định vị toàn cầu để thu thập và gửi về các trung tâm khí tượng ở mặt đất số liệu về nhiệt độ, áp suất, độ ẩm của khí quyển; tốc độ gió; tốc độ di chuyển của các đám mây,... Vỏ bóng được làm bằng cao su tự nhiên hoặc cao su tổng hợp từ hợp chất polychloroprene. Bóng được bơm khí H2 hoặc He. Vỏ bóng trước khi thả có độ dày khoảng 0,051 mm và chỉ giảm xuống còn khoảng 0,0025 mm ở độ cao mà bóng bị vỡ. Tuỳ loại bóng mà khi bắt đầu thả, bóng có thể có đường kính từ 1m đến 2 m, đến khi đạt độ cao trên 30 km thì đường kính của bóng có thể tăng lên gấp 3 lần. Bóng có thể bay lên độ cao tới 40 km, chịu được nhiệt độ tới – 95 °C và thường tồn tại trên cao trong khoảng từ 1 giờ đến 3 giờ trước khi vỡ, tự động mở dù rơi xuống. Mặc dù bóng có gắn thiết bị định vị toàn cầu nhưng xác suất để tìm lại các thiết bị của bóng còn nguyên vẹn là rất nhỏ. 1. Bóng thám không chỉ có thể bay lên được trong điều kiện nào sau đây? Hãy tìm phương án trả lời chính xác nhất. A. Khi khối lượng riêng của bóng nhỏ hơn khối lượng riêng của không khí bên ngoài. B. Khi khối lượng riêng của khí dùng để bơm bóng nhỏ hơn khối lượng riêng của không khí bên ngoài. C. Khi áp suất do chuyển động nhiệt của các phân tử khí trong vỏ bóng nhỏ hơn áp suất khí quyển bên ngoài. D. Khi áp suất do chuyển động nhiệt của các phân tử khí trong vỏ bóng lớn hơn điện áp suất khí quyển bên ngoài. 2. Nội dung câu nào dưới đây là đúng, sai?
3. Khi bóng đang bay lên, khí trong bóng có tuân theo định luật Boyle không? Tại sao? 4. Giải thích tại sao càng bay lên cao thì thể tích của bóng càng tăng và đến một độ cao nhất định nào đó thì bóng sẽ bị vỡ. Phương pháp giải: Vận dụng kiến thức về trạng thái khí lý tưởng Lời giải chi tiết: 1. Khi khối lượng riêng của bóng nhỏ hơn khối lượng riêng của không khí bên ngoài. Điều này là chính xác vì một quả bóng khí bay lên nếu khí trong bóng có khối lượng riêng nhỏ hơn khối lượng riêng của không khí bên ngoài. Khi khối lượng riêng của khí trong bóng nhỏ hơn không khí bên ngoài, lực nâng (do chênh lệch khối lượng riêng) sẽ khiến bóng nổi lên. 2. a) và b) – đúng; c) – sai. Để xác định các thông số trạng thái của khí trong bóng khi bóng đang bay lên có thể dùng phương trình trạng thái của khí lí tưởng \(\frac{{pV}}{T} = \)hằng số. Vì nhiệt độ trong bóng không thay đổi. 3. Không. Vì nhiệt độ của không khí bên ngoài giảm làm cho nhiệt độ của khí bên trong cũng giảm. Do đó, quá trình này không phải là quá trình đẳng nhiệt. 4. Bóng càng bay lên cao thì nhiệt độ và mật độ của không khí bên ngoài giảm càng nhanh nên áp suất của không khí bên ngoài bóng giảm càng mạnh (Ví dụ ở độ cao 30 km nhiệt độ không khí bên ngoài bóng có thể xuống tới – 90 °C, còn áp suất thì chỉ còn cỡ 1 mmHg). Do nhiệt độ giảm nên áp suất khí bên trong bóng cũng giảm, tuy nhiên áp suất này vẫn còn lớn hơn rất nhiều so với áp suất không khí bên ngoài, lực do khí bên trong bóng tác dụng lên vỏ bóng càng tăng thì thể tích bóng càng lớn, vỏ bóng mỏng dần tới một mức độ nào đó thì vỡ (một vỏ bóng trước khi thả có độ dày khoảng 0,051 mm thì khi bóng lên tới độ cao mà bóng bị vỡ, chỉ còn 0,0025 mm).
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




















Danh sách bình luận