Bài 26.11 trang 61 SBT Hóa học 10Giải bài 26.11 trang 61 sách bài tập Hóa học 10. Dựa vào cấu tạo, hãy giải thích vì sao tính oxi hoá của ion hipoclorit (ClO^-) mạnh hơn ion clorat (ClO_3^-). Quảng cáo
Đề bài Dựa vào cấu tạo, hãy giải thích vì sao tính oxi hoá của ion hipoclorit \(ClO^-\) mạnh hơn ion clorat \(ClO_3^-\). Lấy thí dụ phản ứng để minh hoạ. Phương pháp giải - Xem chi tiết Xem lại lý thuyết về nhóm halogen. Tại đây Lời giải chi tiết \(ClO^-\) và \(ClO_3^-\) có cấu tạo tương ứng như sau :
Liên kết Cl-O trong \(ClO_3^-\) ngắn hơn trong \(ClO^-\) nên độ bền \(ClO_3^-\) > \(ClO^-\). Do đó tính oxi hoá \(ClO_3^-\) < \(ClO^-\). Trong dung dịch nước, ion \(ClO_3^-\) chỉ oxi hoá trong môi trường axit mạnh, còn ion \(ClO^-\) oxi hoá trong bất kì môi trường nào. Thí dụ : \(NaClO + 2KI + H_2O → NaCl + I_2 + 2KOH\) \(NaClO_3 + 6KI + 3H_2SO_4 → NaCl + 3I_2 + 3K_2SO_4 + 3H_2O\) Loigiaihay.com
|














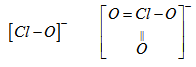






Danh sách bình luận