Bài 19.4, 19.5, 19.6 trang 47 SBT Hóa học 10Giải bài 19.4, 19.5, 19.6 trang 47 sách bài tập Hóa học 10. 19.4. Phản ứng trong đó có sự thay đổi số oxi hóa của các nguyên tử trong cùng một phân tử gọi là phản ứng oxi hóa - khử nội phân tử. Quảng cáo
Lựa chọn câu để xem lời giải nhanh hơn
Câu 19.4. Phản ứng trong đó có sự thay đổi số oxi hóa của các nguyên tử trong cùng một phân tử gọi là phản ứng oxi hóa - khử nội phân tử. Phản ứng nào sau đây thuộc loại trên? A. \(2KCl{O_3}\xrightarrow{{{t^o}}}2KCl + 3{O_2}\) B. \(S + 2{H_2}S{O_4}\xrightarrow{{}}3S{O_2} + {H_2}O\) C. \(4N{O_2} + {O_2} + 2{H_2}O\xrightarrow{{}}4HN{O_3}\) D. \(2NO + {O_2}\xrightarrow{{}}2N{O_2}\) Phương pháp giải: Xác định số oxi hóa của các chất trong các PTHH Lời giải chi tiết: A. \(2K\mathop {Cl}\limits^{ + 5} \mathop {{O_3}}\limits^{ - 2} \xrightarrow{{{t^o}}}2K\mathop {Cl}\limits^{ - 1} + 3\mathop {{O_2}}\limits^0 \) B. \(\mathop S\limits^0 + 2{H_2}\mathop S\limits^{ + 6} {O_4}\xrightarrow{{}}3\mathop S\limits^{ + 4} {O_2} + {H_2}O\) C. \(4\mathop N\limits^{ + 4} {O_2} + \mathop {{O_2}}\limits^0 + 2{H_2}O\xrightarrow{{}}4H\mathop N\limits^{ + 4} \mathop {{O_3}}\limits^{ - 2} \) D. \(2\mathop N\limits^{ + 2} O + \mathop {{O_2}}\limits^0 \xrightarrow{{}}2\mathop N\limits^{ + 4} \mathop {{O_2}}\limits^{ - 2} \) => Chọn A Câu 19.5. Phản ứng nào cho dưới đây chỉ xảy ra sự thay đổi số oxi hoá của một nguyên tố ?
Phương pháp giải: Xác định số oxi hóa của các chất trong các PTHH Lời giải chi tiết: A. \(2K\mathop {Cl}\limits^{ + 5} \mathop {{O_3}}\limits^{ - 2} \xrightarrow{{{t^o}}}2K\mathop {Cl}\limits^{ - 1} + 3\mathop {{O_2}}\limits^0 \) B.\(2K\mathop {Mn}\limits^{ + 7} \mathop {{O_4}}\limits^{ - 2} \xrightarrow{{{t^o}}}{K_2}\mathop {Mn}\limits^{ + 6} {O_4} + Mn{O_2} + \mathop {{O_2}}\limits^0 \) C. \(K\mathop N\limits^{ + 5} \mathop {{O_3}}\limits^{ - 2} \xrightarrow{{{t^o}}}K\mathop N\limits^{ + 3} {O_2} + \mathop {{O_2}}\limits^0 \) D. \(\mathop N\limits^{ - 3} {H_4}\mathop N\limits^{ + 5} \mathop {{O_3}}\limits^{} \xrightarrow{{{t^o}}}\mathop {{N_2}}\limits^{ + 3} O + {H_2}O\) => Chọn D Câu 19.6. Cho sơ đồ phản ứng : \(F{e_3}{O_4} + HN{O_3} \to Fe{\left( {N{O_3}} \right)_3} + NO + {H_2}O\) Cân bằng PTHH của phản ứng trên. Các hệ số tương ứng với phân tử các chất là dãy số nào sau đây ? A. 3, 14, 9, 1, 7 B. 3, 28, 9, 1, 14 C. 3, 26, 9, 2, 13 D. 2, 28, 6, 1, 14 Phương pháp giải: Cân bằng PTHH theo phương pháp thăng bảng electron tại đây. Lời giải chi tiết: \(3F{e_3}{O_4} + 28HN{O_3} \to 9Fe{\left( {N{O_3}} \right)_3} + NO + 14{H_2}O\) => Chọn B Loigiaihay.com
|














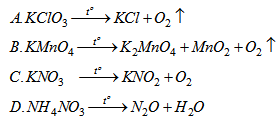
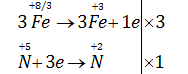






Danh sách bình luận