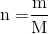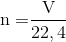Đề kiểm tra 1 tiết Hóa 8 chương 3: Mol và tính toán hóa học - Đề số 1Đề bài
Câu 1 :
0,05 mol Na có khối lượng bằng bao nhiêu?
Câu 2 :
Cho biết công thức tính số mol, khi đề bài cho biết thể tích (V) ở đktc:
Câu 3 :
Thể tích mol của chất khí phụ thuộc vào?
Câu 4 :
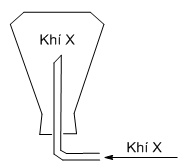
Khí nào có thể thu được bằng cách đặt ngược bình (hình vẽ):
Câu 5 :
Trong 1 mol CO2 có bao nhiêu phân tử?
Câu 6 :
Thể tích 1 mol của hai chất khí bằng nhau nếu được đo ở
Câu 7 :
Khí N2 nặng hơn khí H2 bằng bao nhiêu lần? (N = 14, H = 1)
Câu 8 :
Một mol nguyên tử Nhôm có chứa bao nhiêu nguyên tử nhôm?
Câu 9 :
0,5 mol khí O2 có bao nhiêu phân tử O2 ?
Câu 10 :
Phát biểu nào sau đây đúng và đầy đủ nhất? “Hai chất chỉ có thể tích bằng nhau khi”:
Câu 11 :
Cho 5,6 gam Fe phản ứng với 0,15 mol HCl theo phương trình: Fe + 2HCl \( \to\) FeCl2 + H2. Kết luận nào sau đây là chính xác:
Câu 12 :
Chọn đáp án đúng trong các khẳng định sau:
Câu 13 :
Tính số mol phân tử có trong 6,72 lít khí H₂(đo ở đktc)?
Câu 14 :
Ở điều kiện tiêu chuẩn, thể tích mol của các chất khí có giá trị là:
Câu 15 :
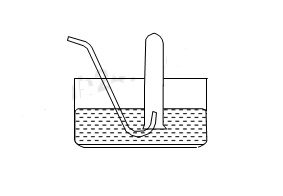
Cho hình vẽ về cách thu khí dời nước như sau: Hình vẽ bên có thể áp dụng để thu được khí nào trong các khí sau đây?
Câu 16 :
Trong các hợp chất sau, hợp chất nào có hàm lượng nitơ cao nhất?
Câu 17 :
0,35 mol khí SO2 ở điều kiện tiêu chuẩn có thể tích bằng bao nhiêu?
Câu 18 :
Phải lấy bao nhiêu mol phân tử CO2 để có 1,5.1023 phân tử CO2?
Câu 19 :
Phải lấy bao nhiêu lít khí CO2 ở đktc để có 3,01.1023 phân tử CO2?
Câu 20 :
Thể tích của 280 gam khí nitơ ở đktc là: +) Khí nitơ có công thức hóa học là N2 +) Tính khối lượng mol N2 +) \({n_{{N_2}}} = \frac{m}{M}\) +) \({V_{{N_2}}} = n*22,4\)
Câu 21 :
Khí A có công thức dạng RO2. Biết dA/KK = 1,5862. Hãy xác định công thức của khí A.
Câu 22 :
Tỉ khối của A đối với H2 là 22. A là khí nào sau đây?
Câu 23 :
Khí A có công thức phân tử dạng RO2, có tỉ khối hơi so với H2 là 32. Vậy A có công thức phân tử là:
Câu 24 :
Một cửa hàng có bán một số loại phân đạm có công thức hóa học sau: ure: CO(NH2)2; amoni sunfat: (NH4)2SO4; amoni nitrat: NH4NO3; canxi nitrat: Ca(NO3)2. Bác nông dân không biết phải mua loại phân đạm nào có hàm lượng nguyên tố N cao nhất để bón cho ruộng. Em hãy giúp bác nông dân lựa chọn.
Câu 25 :
Hợp chất A có khối lượng mol là 94, có thành phần các nguyên tố là: 82,98% K; còn lại là oxi. Công thức hoá học của hợp chất A là
Câu 26 :
Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
Câu 27 :
Tính thể tích của oxygen (đkc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
Câu 28 :
Theo sơ đồ: Cu + O2 → CuO. Nếu cho 3,2 gam Cu tác dụng với 0,8 gam O2. Khối lượng CuO thu được là
Câu 29 :
Cho sắt tác dụng với dung dịch axit H2SO4 theo sơ đồ sau: Fe + H2SO4 → FeSO4 + H2. Có 22,4 gam sắt tác dụng với 24,5 gam H2SO4. Thể tích khí H2 thu được ở đktc là
Câu 30 :
Một hỗn hợp X gồm H2 và O2 (không có phản ứng xảy ra) có tỉ khối so với không khí là 0,3276. Phần trăm theo số mol của khí H2 trong hỗn hợp là
Lời giải và đáp án
Câu 1 :
0,05 mol Na có khối lượng bằng bao nhiêu?
Đáp án : B Phương pháp giải :
Công thức tính khối lượng : m = n × M Lời giải chi tiết :
0,05 mol Na có khối lượng là: mNa = 0,05×23 = 1,15 (g)
Câu 2 :
Cho biết công thức tính số mol, khi đề bài cho biết thể tích (V) ở đktc:
Đáp án : C Lời giải chi tiết :
Cho biết công thức tính số mol, khi đề bài cho biết thể tích (V) ở đktc: n = V:22,4
Câu 3 :
Thể tích mol của chất khí phụ thuộc vào?
Đáp án : D Lời giải chi tiết :
Thể tích mol của chất khí phụ thuộc vào Nhiệt độ của chất khí, Áp suất của chất khí
Câu 4 :
Khí nào có thể thu được bằng cách đặt ngược bình (hình vẽ):
Đáp án : D Phương pháp giải :
Khí thu được bằng cách đặt úp bình \( \to\) khí này có phân tử khối nhẹ hơn không khí (Mkk≈ 29 g/mol) Lời giải chi tiết :
Khí thu được bằng cách đặt úp bình \( \to\) khí này có phân tử khối nhẹ hơn không khí \( \to\) khí X là khí H2 (\({M_{{H_2}}} = 2\,\,g/mol\))
Câu 5 :
Trong 1 mol CO2 có bao nhiêu phân tử?
Đáp án : A Lời giải chi tiết :
1 mol chứa số nguyên tử là: 6,02.1023 => trong 1 mol CO2 có 6,02.1023 phân tử
Câu 6 :
Thể tích 1 mol của hai chất khí bằng nhau nếu được đo ở
Đáp án : D Lời giải chi tiết :
Thể tích 1 mol của hai chất khí bằng nhau nếu được đo ở cùng điều kiện nhiệt độ và áp suất.
Câu 7 :
Khí N2 nặng hơn khí H2 bằng bao nhiêu lần? (N = 14, H = 1)
Đáp án : D Phương pháp giải :
Lấy phân tử khối của N2 chia cho phân tử khối của H2 Lời giải chi tiết :
Phân tử khối của N2 = 14×2 = 28 (gam/mol) Phân tử khối của H2 = 2×1 = 2 (gam/mol) Suy ra \({d_{{N_2}/{H_2}}} =\dfrac{{28}}{2}= 14\) Vậy N2 nặng hơn H2 14 lần
Câu 8 :
Một mol nguyên tử Nhôm có chứa bao nhiêu nguyên tử nhôm?
Đáp án : D Lời giải chi tiết :
Một mol nguyên tử Nhôm có chứa 6.1023 nguyên tử nhôm
Câu 9 :
0,5 mol khí O2 có bao nhiêu phân tử O2 ?
Đáp án : A Phương pháp giải :
Công thức tính số phân tử O2 là: n× 6.1023 = ? Lời giải chi tiết :
Số phân tử O2 là: 0,5 × 6.1023 = 3. 1023 phân tử
Câu 10 :
Phát biểu nào sau đây đúng và đầy đủ nhất? “Hai chất chỉ có thể tích bằng nhau khi”:
Đáp án : C Lời giải chi tiết :
Hai chất chỉ có thể tích bằng nhau khi Số mol bằng nhau trong cùng điều kiện về nhiệt độ và áp suất
Câu 11 :
Cho 5,6 gam Fe phản ứng với 0,15 mol HCl theo phương trình: Fe + 2HCl \( \to\) FeCl2 + H2. Kết luận nào sau đây là chính xác:
Đáp án : B Phương pháp giải :
Tính số mol Fe : nFe = mFe : MFe = ? (mol) Dựa vào phương trình so sánh xem Fe và HCl chất nào phản ứng hết. Lời giải chi tiết :
nFe = 5,6 : 56 = 0,1 (mol) Fe + 2HCl \( \to\) FeCl2 + H2 Theo phương trình 1 2 (mol) Theo đề bài: 0,1 0,15 (mol) Ta thấy : \(\dfrac{{0,1}}{1} > \dfrac{{0,15}}{2}\). Do vậy HCl là chất phản ứng hết, Fe là chất còn dư.
Câu 12 :
Chọn đáp án đúng trong các khẳng định sau:
Đáp án : A Lời giải chi tiết :
Mol là lượng chất có chứa 6.1023 nguyên tử hoặc phân tử của chất đó.
Câu 13 :
Tính số mol phân tử có trong 6,72 lít khí H₂(đo ở đktc)?
Đáp án : A Lời giải chi tiết :
1 mol phân tử H2 (đo ở đktc) chiếm thể tích 22,4 lít X mol phân tử H2 (đo ở đktc) chiếm thể tích 6,72 lít \( \to x = \dfrac{{1.6,72}}{{22,4}} = 0,3\,\,mol\)
Câu 14 :
Ở điều kiện tiêu chuẩn, thể tích mol của các chất khí có giá trị là:
Đáp án : B Lời giải chi tiết :
Ở điều kiện tiêu chuẩn, thể tích mol của các chất khí có giá trị là: 22,4 lít
Câu 15 :
Cho hình vẽ về cách thu khí dời nước như sau: Hình vẽ bên có thể áp dụng để thu được khí nào trong các khí sau đây?
Đáp án : B Lời giải chi tiết :
Khí thu bằng phương pháp đẩy nước phải chọn những khí ít hoặc không tan trong nước → chọn B có CO2 ít tan trong nước và H2 không tan trong nước
Câu 16 :
Trong các hợp chất sau, hợp chất nào có hàm lượng nitơ cao nhất?
Đáp án : C Lời giải chi tiết :
Tư duy nhanh: hợp chất của N với O có càng nhiều nguyên tử N thì hàm lượng nito càng cao \(\mathop N\limits^1 \mathop O\limits^1 \) \(\mathop N\limits^1 {\mathop O\limits^2 _2}\) \(\mathop {{N_2}}\limits^2 \mathop O\limits^1 \) \(\mathop {{N_2}}\limits^2 \mathop {{H_4}}\limits^{} \mathop {{O_3}}\limits^3 \) Ta thấy tỉ lệ 2:1 trong hợp chất N2O là lớn nhất. Do vậy hàm lượng nitơ trong N2O là cao nhất.
Câu 17 :
0,35 mol khí SO2 ở điều kiện tiêu chuẩn có thể tích bằng bao nhiêu?
Đáp án : B Phương pháp giải :
Công thức tính thể tích khí ở đktc: V = n × 22,4 = ? (lít) Lời giải chi tiết :
Thể tích 0,35 mol SO2 ở đktc là : VSO2(đktc) = 0,35 × 22,4 = 7,84 (lít)
Câu 18 :
Phải lấy bao nhiêu mol phân tử CO2 để có 1,5.1023 phân tử CO2?
Đáp án : B Lời giải chi tiết :
6,02.1023 phân tử CO2 = 1 mol => 1,5.1023 phân tử CO2 = $\dfrac{{1,{{5.10}^{23}}.1}}{{{{6.10}^{23}}}} \approx 0,25$ mol
Câu 19 :
Phải lấy bao nhiêu lít khí CO2 ở đktc để có 3,01.1023 phân tử CO2?
Đáp án : A Lời giải chi tiết :
1 mol CO2 chứa 6,02.1023 phân tử => $\dfrac{{3,{{01.10}^{23}}}}{{6,{{02.10}^{23}}}} = 0,5$ mol CO2 chứa 3,01.1023 phân tử => thể tích khí CO2 là: V = n.22,4 = 0,5.22,4 = 11,2 lít
Câu 20 :
Thể tích của 280 gam khí nitơ ở đktc là: +) Khí nitơ có công thức hóa học là N2 +) Tính khối lượng mol N2 +) \({n_{{N_2}}} = \frac{m}{M}\) +) \({V_{{N_2}}} = n*22,4\)
Đáp án : D Lời giải chi tiết :
Khối lượng mol của khí N2 là: M = 2.14 = 28 g/mol => số mol khí N2 là: $n = \frac{m}{M}\, = \frac{{280}}{{28}} = 10\,(mol)$ => thể tích cảu 280 gam khí nitơ là: V = n.22,4 = 10.22,4 = 224 lít
Câu 21 :
Khí A có công thức dạng RO2. Biết dA/KK = 1,5862. Hãy xác định công thức của khí A.
Đáp án : B Phương pháp giải :
+) Tỉ khối của A so với không khí là 1,5862 => MA = 29 . dA/KK +) Khối lượng mol của khí A là: ${M_{R{O_2}}} = {M_R} + 2.{M_O}$ => MR Lời giải chi tiết :
Tỉ khối của A so với không khí là 1,5862 => MA = 29 . dA/KK = 29.1,5862 = 46 g/mol Khối lượng mol của khí A là: ${M_{R{O_2}}} = {M_R} + 2.{M_O}$ => MR = 46 – 2.16 = 14 gam => R là N => Công thức của A là NO2
Câu 22 :
Tỉ khối của A đối với H2 là 22. A là khí nào sau đây?
Đáp án : C Phương pháp giải :
Tỉ khối của A đối với H2 : ${d_{A/{H_2}}} = \dfrac{{{M_A}}}{{{M_{{H_2}}}}} = 22 = > {M_A} = 22.{M_{{H_2}}}$ Lời giải chi tiết :
Tỉ khối của A đối với H2 : ${d_{A/{H_2}}} = \dfrac{{{M_A}}}{{{M_{{H_2}}}}} = 22 = > {M_A} = 22.{M_{{H_2}}} = 22.2 = 44$ g/mol Loại A vì NO2 có M = 14 + 16.2 = 46 Loại B vì N2 có M = 2.14 = 28 Chọn C vì CO2 có M = 12 + 16.2 = 44 Loại D vì Cl2 có M = 2.35,5 = 71
Câu 23 :
Khí A có công thức phân tử dạng RO2, có tỉ khối hơi so với H2 là 32. Vậy A có công thức phân tử là:
Đáp án : A Phương pháp giải :
+) ${d_{A/{H_2}}} = \frac{{{M_A}}}{{{M_{{H_2}}}}} = > {M_A} = {d_{A/{H_2}}}.{M_{{H_2}}}$ +) A có công thức phân tử là RO2 => M = MR + 2.MO = 64 => MR => nguyên tố R Lời giải chi tiết :
Khí A có tỉ khối so với H2 là 32 => ${d_{A/{H_2}}} = \frac{{{M_A}}}{{{M_{{H_2}}}}} = > {M_A} = {d_{A/{H_2}}}.{M_{{H_2}}} = 32.2 = 64$ A có công thức phân tử là RO2 => M = MR + 2.MO = 64 => MR = 64 – 2.16 = 32 => R là nguyên tố S Vậy công thức phân tử của A là SO2
Câu 24 :
Một cửa hàng có bán một số loại phân đạm có công thức hóa học sau: ure: CO(NH2)2; amoni sunfat: (NH4)2SO4; amoni nitrat: NH4NO3; canxi nitrat: Ca(NO3)2. Bác nông dân không biết phải mua loại phân đạm nào có hàm lượng nguyên tố N cao nhất để bón cho ruộng. Em hãy giúp bác nông dân lựa chọn.
Đáp án : A Phương pháp giải :
+) Tính khối lượng phân tử mỗi chất +) Tính %N tương ứng Lời giải chi tiết :
+) ${M_{CO{{(N{H_2})}_2}}} = 12 + 16 + (14 + 2).2 = 60$ => Phần trăm khối lượng của N trong CO(NH2)2 là: $\% N = \frac{{2.{M_N}}}{{{M_{CO{{(N{H_2})}_2}}}}}.100\% = \frac{{2.14}}{{60}}.100\% = 46,67\% $ +) ${M_{{{(N{H_4})}_2}S{O_4}}} = (14 + 4).2 + 32 + 16.4 = 132$ => Phần trăm khối lượng của N trong (NH4)2SO4 là: $\% N = \frac{{2.{M_N}}}{{{M_{{{(N{H_4})}_2}S{O_4}}}}}.100\% = \frac{{2.14}}{{132}}.100\% = 21,21\% $ +) ${M_{N{H_4}N{O_3}}} = 14 + 4 + 14 + 16.3 = 80$ => $\% N = \frac{{2.{M_N}}}{{{M_{N{H_4}N{O_3}}}}}.100\% = \frac{{2.14}}{{80}}.100\% = 35\% $ +) ${M_{Ca{{(N{O_3})}_2}}} = 40 + (14 + 16.3).2 = 164$ => $\% N = \frac{{2.{M_N}}}{{{M_{Ca{{(N{O_3})}_2}}}}}.100\% = \frac{{2.14}}{{164}}.100\% = 17,07\% $ Vậy phân có hàm lượng nguyên tố N cao nhất là ure: CO(NH2)2
Câu 25 :
Hợp chất A có khối lượng mol là 94, có thành phần các nguyên tố là: 82,98% K; còn lại là oxi. Công thức hoá học của hợp chất A là
Đáp án : C Phương pháp giải :
Hợp chất A gồm K và O mà %K = 82,98% => %O +) mK = $\dfrac{{94.82,98}}{{100}}$ => nK +) mO = $\dfrac{{94.17,02}}{{100}}$ => nO +) Từ tỉ lệ mol K và O => CTPT Lời giải chi tiết :
Hợp chất A gồm K và O mà %K = 82,98% => %O = 100% - 82,98% = 17,02% Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là: mK = $\dfrac{{94.82,98}}{{100}}$ = 78 gam và mO = $\dfrac{{94.17,02}}{{100}}$ = 16 gam => Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là: nK = $\dfrac{{78}}{{39}}$ = 2 mol nO = $\dfrac{{16}}{{16}}$ = 1 mol Vậy công thức hoá học của hợp chất là K2O
Câu 26 :
Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
Đáp án : A Phương pháp giải :
+) Tính số mol khí CH4 phản ứng: ${n_{C{H_4}}} = \dfrac{{1,12}}{{22,4}}$ PTHH: CH4 + 2O2 $\xrightarrow{{{t^o}}}$ CO2 + 2H2O Tỉ lệ theo PT: 1mol 2mol 1mol 2mol 0,05mol ?mol Từ PTHH, ta có: ${n_{{O_2}}} = \dfrac{{0,05.2}}{1}$ => thể tích khí O2 : V = 22,4.n Lời giải chi tiết :
Số mol khí CH4 phản ứng là: ${n_{C{H_4}}} = \dfrac{{1,12}}{{22,4}} = 0,05\,mol$ PTHH: CH4 + 2O2 $\xrightarrow{{{t^o}}}$ CO2 + 2H2O Tỉ lệ theo PT: 1mol 2mol 1mol 2mol 0,05mol ?mol Từ PTHH, ta có: ${n_{{O_2}}} = \dfrac{{0,05.2}}{1} = 0,1\,mol$ => thể tích khí O2 cần dùng là: ${V_{{O_2}}} = 22,4.n = 22,4.0,1 = 2,24$ lít
Câu 27 :
Tính thể tích của oxygen (đkc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
Đáp án : C Phương pháp giải :
+) Tính số mol P phản ứng PTHH: 4P + 5O2 $\xrightarrow{{{t^o}}}$ 2P2O5 Tỉ lệ theo PT: 4mol 5mol 2mol 1mol ?mol Từ PTHH, ta có: ${n_{{O_2}}} = \dfrac{{0,1.5}}{4}$ => Thể tích oxi cần dùng là: V = 24,79.n Lời giải chi tiết :
Số mol P phản ứng là: ${n_P} = \dfrac{{3,1}}{{31}} = 0,1\,mol$ PTHH: 4P + 5O2 $\xrightarrow{{{t^o}}}$ 2P2O5 Tỉ lệ theo PT: 4mol 5mol 1mol ? mol Nhân chéo chia ngang ta được: ${n_{{O_2}}} = \dfrac{{0,1.5}}{4}$ $ = 0,125\,mol$ => Thể tích oxi cần dùng là: V = 22,4.n = 24,79.0,125 = 3,1 lít
Câu 28 :
Theo sơ đồ: Cu + O2 → CuO. Nếu cho 3,2 gam Cu tác dụng với 0,8 gam O2. Khối lượng CuO thu được là
Đáp án : D Phương pháp giải :
+) Tính số mol Cu và số mol O2 +) Xét tỉ lệ: $\dfrac{{{n_{Cu}}}}{2}$ và $\dfrac{{{n_{{O_2}}}}}{1}$ => chất dư thừa hoặc vừa đủ, phản ứng tính theo chất phản ứng hết Lời giải chi tiết :
Số mol Cu là: ${n_{Cu}} = \dfrac{{3,2}}{{64}} = 0,05\,mol$ Số mol O2 là: ${n_{{O_2}}} = \dfrac{{0,8}}{{32}} = 0,025\,mol$ PTHH: 2Cu + O2 → 2CuO Xét tỉ lệ: $\dfrac{{{n_{Cu}}}}{2} = \dfrac{{0,05}}{2} = 0,025$ và $\dfrac{{{n_{{O_2}}}}}{1} = \dfrac{{0,025}}{1} = 0,025$ Vì tỉ lệ $\dfrac{{{n_{Cu}}}}{2} = \dfrac{{{n_{{O_2}}}}}{1}$ => phản ứng vừa đủ => tính theo Cu hoặc O2 đều được PTHH: 2Cu + O2 → 2CuO 2mol 2mol 0,05mol → 0,05mol => khối lượng CuO thu được là: mCuO = 0,05.80 = 4 gam Cách 2: Vì các chất đều phản ứng vừa đủ => áp dụng định luật bảo toàn khối lượng ta có: ${m_{CuO}} = {m_{Cu}} + {m_{{O_2}}} = 3,2 + 0,8 = 4\,gam$
Câu 29 :
Cho sắt tác dụng với dung dịch axit H2SO4 theo sơ đồ sau: Fe + H2SO4 → FeSO4 + H2. Có 22,4 gam sắt tác dụng với 24,5 gam H2SO4. Thể tích khí H2 thu được ở đktc là
Đáp án : A Phương pháp giải :
+) Tính số mol Fe và số mol H2SO4 +) Viết PTHH +) Xét tỉ lệ: $\dfrac{{{n_{F{\text{e}}}}}}{1}$ và $\dfrac{{{n_{{H_2}S{O_4}}}}}{1}$ => chất dư và chất hết => tính số mol H2 theo chất hết Lời giải chi tiết :
Số mol Fe là: ${n_{F{\text{e}}}} = \dfrac{{22,4}}{{56}} = 0,4\,mol$ Số mol H2SO4 là: ${n_{{H_2}S{O_4}}} = \dfrac{m}{M} = \dfrac{{24,5}}{{2 + 32 + 16.4}} = 0,25\,mol$ PTHH: Fe + H2SO4 → FeSO4 + H2 Xét tỉ lệ: $\dfrac{{{n_{F{\text{e}}}}}}{1} = \dfrac{{0,4}}{1} = 0,4$ và $\dfrac{{{n_{{H_2}S{O_4}}}}}{1} = \dfrac{{0,25}}{1} = 0,25$ Vì 0,25 < 0,4 => Fe dư, H2SO4 phản ứng hết => tính số mol H2 theo H2SO4 PTHH: Fe + H2SO4 → FeSO4 + H2 1mol 1mol 0,25 mol → 0,25 mol => Thể tích khí H2 thu được ở đktc là: V = 22,4.n = 22,4.0,25 = 5,6 lít
Câu 30 :
Một hỗn hợp X gồm H2 và O2 (không có phản ứng xảy ra) có tỉ khối so với không khí là 0,3276. Phần trăm theo số mol của khí H2 trong hỗn hợp là
Đáp án : B Phương pháp giải :
+) Tỉ khối của X so với không khí : ${d_{X/kk}} = \dfrac{{{{\bar M}_X}}}{{29}} = > {\bar M_X}$ Công thức tính khối lượng trung bình của hỗn hợp X là ${M_X} = \dfrac{{{n_{{H_2}}}.{M_{{H_2}}} + {n_{{O_2}}}.{M_{{O_2}}}}}{{{n_{{H_2}}} + {n_{{O_2}}}}}$ +) phần trăm số mol khí H2 là: $\% {n_{{H_2}}} = \dfrac{{{n_{{H_2}}}}}{{{n_{{H_2}}} + {n_{{O_2}}}}}.100\% $ Lời giải chi tiết :
Gọi số mol của H2 và O2 trong hỗn hợp lần lượt là x và y mol Tỉ khối của X so với không khí : ${d_{X/kk}} = \dfrac{{{{\bar M}_X}}}{{29}} = > {\bar M_X} = 29.0,3276 = 9,5$ Công thức tính khối lượng trung bình của hỗn hợp X là ${M_X} = \dfrac{{{n_{{H_2}}}.{M_{{H_2}}} + {n_{{O_2}}}.{M_{{O_2}}}}}{{{n_{{H_2}}} + {n_{{O_2}}}}} = \dfrac{{2{\text{x}} + 32y}}{{x + y}} = 9,5$ => 2x + 32y = 9,5x + 9,5y => 7,5x = 22,5 => x = 3y => phần trăm số mol khí H2 là: $\% {n_{{H_2}}} = \dfrac{{{n_{{H_2}}}}}{{{n_{{H_2}}} + {n_{{O_2}}}}}.100\% = \dfrac{{3y}}{{3y + y}}.100\% = 75\% $ |