Câu hỏi:
Cho phương trình hóa học sau: CH2=CH2 + KMnO4 + H2O → CH2(OH)-CH2(OH) + MnO2 + KOH
Hệ số nguyên tối giản của các chất tham gia phản ứng trong phương trình trên là
- A 3:2:4
- B 3: 1: 2
- C 3:2:2
- D 3: 4 : 1
Phương pháp giải:
Dựa vào phương pháp cân bằng pư oxi hóa khử để cân bằng phương trình. Từ đó tìm được hệ số nguyên tối giản của các chất tham gia phản ứng trong phương trình trên
Lời giải chi tiết:
Bước 1: Xác định số oxi hóa của các chất
\(\mathop C\limits^{ - 2} {H_2} = \mathop C\limits^{ - 2} {H_2} + K\mathop {Mn}\limits^{ + 7} {O_4} + {H_2}O \to \mathop C\limits^{ - 1} {H_2}(OH) - \mathop C\limits^{ - 1} {H_2}(OH) + \mathop {Mn}\limits^{ + 4} {O_2} + KOH\)
Bước 2: Viết các quá trình nhường, nhận e, sau đó đặt hệ số trước mỗi quá trình sao cho tổng số electron nhường = tổng số electron nhận
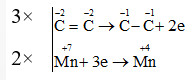
Bước 3: Đặt hệ số tương ứng vào các chất trong phương trình ta được
\(3\mathop C\limits^{ - 2} {H_2} = \mathop C\limits^{ - 2} {H_2} + 2K\mathop {Mn}\limits^{ + 7} {O_4} + 4{H_2}O \to 3\mathop C\limits^{ - 1} {H_2}(OH) - \mathop C\limits^{ - 1} {H_2}(OH) + \mathop {2Mn}\limits^{ + 4} {O_2} + 2KOH\)
→ Hệ số nguyên tối giản của các chất tham gia phản ứng trong phương trình trên là 3:2:4
Đáp án A


















