Lý thuyết Định luật Boyle - Vật lí 12 Kết nối tri thứcCác thông số trạng thái của một lượng khí Định luật Boyle Tổng hợp đề thi học kì 2 lớp 12 tất cả các môn - Kết nối tri thức Toán - Văn - Anh - Hoá - Sinh - Sử - Địa Quảng cáo
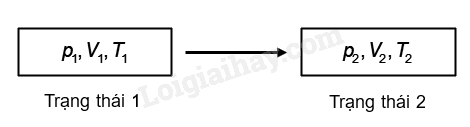
Bài 9. Định luật Boyle I. Các thông số trạng thái của một lượng khí - Một lượng khí đựng trong một bình kín được xác định bởi bốn đại lượng là khối lượng (m), thể tích (V), nhiệt độ (T) và áp suất (p). - Khi thể tích, nhiệt độ và áp suất của một khối lượng khí xác định không thay đổi, ta nói lượng khí ở trạng thái cân bằng. Thể tích, áp suất và nhiệt độ của lượng khí được gọi là các thông số trạng thái của nó. - Khí chuyển từ trạng thái này sang trạng thái khác bằng các quá trình biến đổi trạng thái, gọi tắt là quá trình. - Người ta thường biểu diễn trạng thái và quá trình biến đổi trạng thái của một khối lượng khí xác định bằng hình dưới đây:
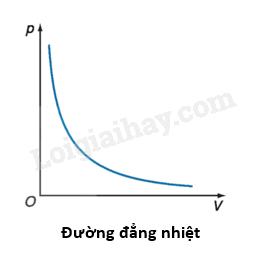
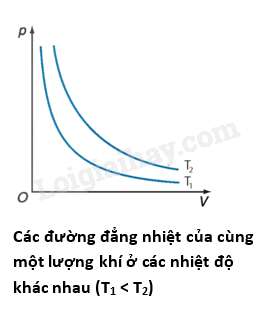
- Trong hầu hết các quá trình biến đổi trạng thái của một khối lượng khí xác định thì cả ba thông số trạng thái (áp suất, thể tích, nhiệt độ) đều có thể biến đổi. II. Định luật Boyle 1. Quá trình đẳng nhiệt Quá trình biến đổi trạng thái của một khối lượng khí xác định khi nhiệt độ giữ không đổi được gọi là quá trình đẳng nhiệt. 2. Định luật Boyle - Khi nhiệt độ của một khối lượng khí xác định giữ không đổi thì áp suất gây ra bởi khí tỉ lệ nghịch với thể tích của nó: pV = hằng số - Đồ thị biểu diễn định luật Boyle là một nhánh của đường hypebol. - Đường đẳng nhiệt của cùng một lượng khí ứng với các nhiệt độ khác nhau thì khác nhau. Đường đẳng nhiệt của cùng một lượng khí ứng với nhiệt độ \({T_1}\) ở thấp hơn đường đẳng nhiệt ứng với nhiệt độ \({T_2}\), với \({T_1} < {T_2}\). - Nếu gọi \({p_1},\,\,{V_1}\) là áp suất và thể tích của khí ở trạng thái 1; \({p_2},\,\,{V_2}\) là áp suất và thể tích của khí ở trạng thái 2 thì: \({p_1}{V_1} = {p_2}{V_2}\) Sơ đồ tư duy về “Định luật Boyle”
|





















Danh sách bình luận