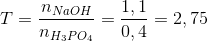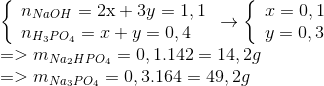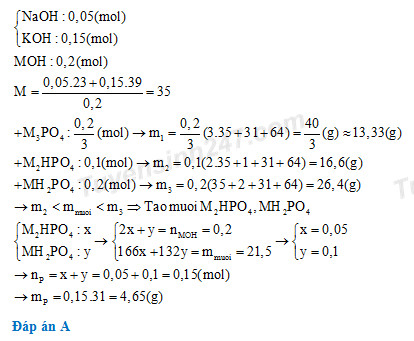20 bài tập vận dụng cao về axit photpphoric và muối photphat có lời giảiLàm bàiQuảng cáo
Câu hỏi 1 : Trộn 100 ml dung dịch KH2PO4 1M với 150 ml dung dịch NaOH 1M thu được dung dịch X chứa m gam chất tan. Giá trị của m là ? Giả sử rằng các muối không bị thủy phân.
Đáp án: C Phương pháp giải: Lời giải chi tiết: nOH- = 0,15 mol; nH2PO4- = 0,1 mol Dung dịch sau chứa các ion: K+ (0,1 mol), Na+ (0,15 mol), PO43- (x mol) và HPO42- (y mol) BTNT “P” có: x + y = 0,1 (1) Trung hòa điện tích: 3x + 2y = 0,1 + 0,15 (2) Giải (1) và (2) => x = 0,05 và y = 0,05 => m = 0,1.39 + 0,15.23 + 0,05.95 + 0,05.96 = 16,9 gam Đáp án C Câu hỏi 2 : Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
Đáp án: C Phương pháp giải: Gọi công thức trung bình của bazo và làm tương tự như cho 1 bazo tác dụng với P2O5 Lời giải chi tiết: 2P -> P2O5 -> 2H3PO4 => nH3PO4 = nP = 0,2 mol ,nOH = 0,5 mol => 2 < nOH : nH3PO4 = 2,5 < 3 Các phản ứng : 2MOH + H3PO4 -> M2HPO4 + 2H2O 3MOH + H3PO4 -> M3PO4 + 3H2O => Muối gồm : 0,1 mol M2HPO4 và 0,1 mol M3PO4 => mmuối = mK + mNa + mHPO4 + mPO4 = 35,4g Đáp án C Câu hỏi 3 : Thể tích khí NH3 (đktc) và khối lượng H3PO4 để điều chế được 1,235 tấn amophot (tỉ lệ mol NH4H2PO4 : (NH4)2HPO4 = 1 : 1) là
Đáp án: A Phương pháp giải: Bảo toàn nguyên tố. Lời giải chi tiết: Giả sử số mol NH4H2PO4 và (NH4)2HPO4 là x (kmol) mamophot = mNH4H2PO4 + m(NH4)2HPO4 => 115x + 132x = 1235 kg => x = 5 (kmol) BTNT "N": nNH3 = nNH4H2PO4 + 2n(NH4)2HPO4 = x + 2x = 15 kmol => V = 336 m3 BTNT "P": nH3PO4 = nNH4H2PO4 + n(NH4)2HPO4 = x + x = 10 kmol => mH3PO4 = 980 kg Đáp án A Câu hỏi 4 : Đốt cháy một lượng photpho (có khối lượng lớn hơn 2,48 gam) bằng oxi dư, lấy sản phẩm cho vào 75 gam dung dịch NaOH 8% rồi làm khô thu được m gam chất rắn khan X trong đó có 8,52 gam Na2HPO4. Giá trị của m là
Đáp án: B Phương pháp giải: Lời giải chi tiết: - Theo đề ta có: mNaOH = 75.8% = 6 gam => nNaOH = 0,15 mol nNa2HPO4 = 8,52 : 142 = 0,06 mol mP > 2,48 gam => nP > 0,08 mol - Đặt muối còn lại là NanH3-nPO4 (muối còn lại có thể là NaH2PO4 hoặc Na3PO4) => \(\frac{{{n_{Na}}}}{{{n_P}}} = \frac{n}{{3 - n}} = \frac{{0,15}}{{{n_P}}} < \frac{{0,15}}{{0,08}} = 1,875\) => n = 1 Bảo toàn nguyên tố Na: nNaH2PO4 = nNaOH - 2nNa2HPO4 = 0,15 - 2.0,06 = 0,03 mol => m = mNa2HPO4 + mNaH2PO4 = 8,52 + 120.0,03 = 12,12 gam Đáp án B Câu hỏi 5 : Cho m gam P2O5 tác dụng với 253,5 ml dung dịch NaOH 2M .Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn dung dịch X, thu được 3m gam chất rắn khan. Giá trị của m là:
Đáp án: C Phương pháp giải: Lời giải chi tiết:
Câu hỏi 6 : Lấy 240 ml dung dịch gồm NaOH 1,6M và KOH 1M tác dụng hết với dung dịch H3PO4 thu được dung dich X. Chia X thành 2 phần bằng nhau: - Phần 1: Cô cạn thu được 20,544 gam hỗn hợp muối khan. - Phần 2: Cho tác dụng với dung dịch CaCl2 (dư) thu được m gam kết tủa. Giá trị của m là
Đáp án: B Phương pháp giải: Quy đổi hỗn hợp kiềm về MOH với M=(23.0,384+39.0,24)/0,624=379/13. Lời giải chi tiết: nNaOH=0,384 mol; nKOH=0,24 mol. Gọi CT chung của kiềm là MOH (với M=(23.0,384+39.0,24)/0,624=379/13) Giả sử chỉ tạo một trong các muối sau: MH2PO4: m muối=0,624.(1640/13)=78,72 g. M2HPO4: m muối=(0,624/2).(2006/13)=48,144 g. M3PO4: m muối=(0,624/3).(2372/13)=37,952 g. 37,952 gmuối=20,544.2=41,088<48,144 g => Tạo 2 muối M2HPO4 (x mol); M3PO4 (y mol). Ta có: (2006/13)x+(2372/13)y=20,544(1) 2x+3y=0,024/2(2) =>x=0,048; y=0,072 =>m↓=mCa3(PO4)2+mCaHPO4=0,036.310+0,048.136=17,688 gam. Đáp án B Câu hỏi 7 : Lấy V(ml) dung dịch H3PO4 35% ( d = 1,25gam/ml ) đem trộn với 100 ml dung dịch KOH 2M thu được dung dịch X có chứa 14,95 gam hỗn hợp 2 muối K3PO4 và K2HPO4. Tính V1
Đáp án: B Phương pháp giải: Phương pháp: 2KOH+ H3PO4 -> K2HPO4 + 2H2O 2x x x 3KOH + H3PO4 -> K3PO4 + 3H2O 3y y y Lời giải chi tiết:
Hướng dẫn giải 2KOH+ H3PO4 -> K2HPO4 + 2H2O 2x x x 3KOH + H3PO4 -> K3PO4 + 3H2O 3y y y => chọn B Đáp án B Câu hỏi 8 : Cho 1,32 gam (NH4)2SO4 tác dụng với dung dịch NaOH dư, đun nóng thu được một sản phẩm khí. Hấp thụ hoàn toàn lượng khí trên vào dung dịch chứa 3,92 gam H3PO4. Khối lượng muối thu được là
Đáp án: A Phương pháp giải: Phương pháp: (NH4)2SO4 + 2NaOH Na2SO4 + 2NH3 + 2H2O 0,01 0,02 0,02 H3PO4 + NH3 NH4H2PO4 So sánh số mol, tính theo chất hết Lời giải chi tiết:
Hướng dẫn giải (NH4)2SO4 + 2NaOH Na2SO4 + 2NH3 + 2H2O 0,01 0,02 0,02 H3PO4 + NH3 NH4H2PO4 Bđ 0,04 0,02 p/u 0,02 0,02 0,02 Sau 0,02 0 0,02 => mmuối = 115.0,02=2,3 gam => chọn A Đáp án A
Câu hỏi 9 : Cho a mol P2O5 vào 200 ml dung dịch NaOH thì thu được dung dịch chứa 0,15 mol Na2HPO4 và 0,25 mol NaH2PO4. Hãy xác định giá trị của a và nồng độ của NaOH.
Đáp án: B Phương pháp giải: Lời giải chi tiết: Hướng dẫn giải:
NaOH+ H3PO4 -> NaH2PO4 + H2O 0,25 0,25 0,25 2Na OH + H3PO4 -> Na2HPO4 + 2H2O 0,3 0,15 0,15 => nNaOH = 0,25+0,3=0,55mol => CM(NaOH) = 0,55:0,2=2,75 M Đáp án B Câu hỏi 10 : Cho 44g NaOH vào dung dịch chứa 39,2g H3PO4. Sau khi phản ứng xảy ra hoàn toàn , đem cô dung dịch thu được đến cạn khô. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu ?
Đáp án: D Phương pháp giải: Phương pháp: nNaOH = 44:40=1,1 mol
2<T<3 tạo 2 muối Na2HPO4 ,Na3PO4 2NaOH+ H3PO4 Na2HPO4 + 2H2O 2x.................x 3Na OH + H3PO4 Na3PO4 + 3H2O 3y...............y Lời giải chi tiết:
Hướng dẫn giải nNaOH = 44/40=1,1 mol nH3PO4=39,2/98=0,4 mol.
2<T<3 tạo 2 muối Na2HPO4 ,Na3PO4 2NaOH+ H3PO4 Na2HPO4 + 2H2O 2x.................x 3Na OH + H3PO4 Na3PO4 + 3H2O 3y...............y => chọn D Đáp án D
Câu hỏi 11 : Đốt cháy hoàn toàn m gam P trong oxi dư. Cho toàn bộ sản phẩm tạo thành vào 100ml dung dịch chứa hỗn hợp NaOH 0,5M và KOH 1,5M đến khi các phản ứng xảy ra hoàn toàn, cô cạn dung dịch sau phản ứng, làm khô thu được 21,5 gam chất rắn khan. Giá trị của m là:
Đáp án: A Phương pháp giải: Lời giải chi tiết:
Câu hỏi 12 : Từ 5,299 kg quặng photphorit chứa 78% Ca3(PO4)2 còn lại là tạp chất trơ người ta tiến hành điều chế axit photphoric với hiệu suất cả quá trình là 75%. Lấy 0,5% axit thu được hòa tan vào nước rồi trộn với 100 ml dung dịch NaOH xM thu được dung dịch X. Cô can cẩn thận dung dịch X thu được 17,2 gam chất rắn. Giá trị gần đúng của x là
Đáp án: D Phương pháp giải: PTHH : Ca3(PO4)2 nCa3(PO4)2 =5299.0,78:310=13,33 mol → nH3PO4 = 13,33.0,75.2.0,005=0,1 mol Các phương trình có thể xảy ra là : H3PO4 + 3NaOH → Na3PO4 + 3H2O H3PO4 + 2NaOH → Na2 HPO4 + 2H2O H3PO4 + NaOH → NaH2PO4 + H2O Nếu chất rắn chỉ có muối thì Lượng muối tạo ra tối đa khi tạo thành Na3PO4 => mNa3PO4 = 0,1.164 =16,4 < 17,2 → còn dư NaOH → chỉ tạo muối Na3PO4: 0,1 mol và còn dư NaOH : 0,8g Bảo toàn Na tìm được số mol NaOH Lời giải chi tiết:
Hướng dẫn giải PTHH : Ca3(PO4)2 → 2H3PO4 nCa3(PO4)2 =5299.0,78:310=13,33 mol → nH3PO4 = 13,33.0,75.2.0,005=0,1 mol Các phương trình có thể xảy ra là : H3PO4 + 3NaOH → Na3PO4 + 3H2O H3PO4 + 2NaOH → Na2 HPO4 + 2H2O H3PO4 + NaOH → NaH2PO4 + H2O Nếu chất rắn chỉ có muối Lượng muối tạo ra tối đa khi tạo thành Na3PO4 => mNa3PO4 = 0,1.164 =16,4 < 17,2 → còn dư NaOH → chỉ tạo muối Na3PO4: 0,1 mol và còn dư NaOH : 0,8g hay 0,02 mol Bảo toàn nguyên tố Na có 0,1.3 + 0,02 = nNaOH = 0,32 =0,1x → x =3,2M Đáp án D Câu hỏi 13 : Cho m gam P2O5 vào dung dịch chứa 0,1 mol NaOH và 0,05 mol KOH, thu được dung dịch X. Cô cạn X, thu được 13,9 gam hỗn hợp chất rắn khan. Giá trị của m là
Đáp án: B Phương pháp giải: Quy về công thức chung của dd kiềm là MOH với M là nguyên tử khối trung bình của Na và K Từ số mol MOH xét các trường hợp: + Chỉ tạo 1 muối MH2PO4 thì thu được mi gam chất rắn + Chỉ tạo 1 muối M2HPO4 thì thu được m2 gam muối + Chỉ tạo muối M3PO4 thì thu được m3 gam muối So sánh giá trị m đề bài đã cho với mi, m2, m3 Nếu mi < m < m2 => tạo 2 muối MH2PO4 và M2HPO4 Nếu m2 < m < m3 => tạo 2 muối M2HPO4 và M3PO4 Khi đó bảo toàn mol MOH và khối lượng rắn m 2 ẩn 2 phương trình giải ra đáp án. Lời giải chi tiết: Giả sử dung dịch kiềm có công thức chung là: MOH: 0,15 (mol) với \(M = \frac{{0,1.23 + 0,05.39}}{{0,1 + 0,05}} = \frac{{85}}{3}(g/mol)\) + Nếu phản ứng chỉ tạo 1 muối: \(\begin{gathered} Ta thấy 11,45= m2 < mrắn = 13, 9 < m1 = 18,8 => tạo cả 2 muối MH2PO4 và M2HPO4 \(\left\{ \begin{gathered} BTNT: P => nP = nMH2PO4 + nM2PO4 = 0,05 + 0,05 = 0,1 (mol) => nP2O5 = ½ nP = 0,05 (mol) => mP2O5 = 0,05. 142 = 7,1 (g) Đáp án B Câu hỏi 14 : Cho m gam P2O5 vào dung dịch chứa 0,1 mol NaOH và 0,05 mol KOH thu được dung dịch X. Cô cạn X, thu được 8,56 gam hỗn hợp chất rắn khan. Giá trị của m là:
Đáp án: D Phương pháp giải: Tính khối lượng chất rắn tại 3 điểm: - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và PO43- => m1 - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và HPO42- => m2 - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và H2PO4- => m3 So sánh khối lượng chất rắn đề bài cho với m1, m2, m3 từ đó suy ra được sản phẩm của phản ứng. + Nếu m chất rắn < m1 => Tạo Na+; K+; PO43-; OH- dư + m1 < m chất rắn < m2 => Tạo Na+; K+; PO43-; HPO42- + m2 < m chất rắn < m3 => Tạo Na+; K+; HPO42-; H2PO4- + m chất rắn > m3 => Tạo Na+; K+; H2PO4-; H+ dư Lời giải chi tiết: - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và PO43- (0,05 mol (BTĐT)) => m1 = 0,1.23 + 0,05.39 + 0,05.95 = 9 gam - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và HPO42- (0,075 mol (BTĐT)) => m2 = 0,1.23 + 0,05.39 + 0,075.96 = 11,45 gam - Nếu tạo muối gồm: Na+ (0,1 mol); K+ (0,05 mol) và H2PO4- (0,15 mol (BTĐT)) => m3 = 0,1.23 + 0,05.39 + 0,15.97 = 18,8 gam Theo đề bài: m chất rắn = 8,56 gam < m1 => Dung dịch thu được chứa: Na+ (0,1 mol); K+ (0,05 mol); PO43- (a mol) và OH- dư (b mol) + BTĐT: nNa+ + nK+ = 3nPO43- + nOH- => 3a + b = 0,1 + 0,05 (1) + m chất rắn = mNa+ + mK+ + mPO43- + mOH- => 0,1.23 + 0,05.39 + 95a + 17b = 8,56 (2) Giải hệ (1) và (2) được: a = 0,04 và b = 0,03 BTNT "P": 2.nP2O5 = nPO43- => nP2O5 = 0,5.nPO43- = 0,02 mol => m = 0,02.142 = 2,84 gam Đáp án D Câu hỏi 15 : Cho m gam P2O5 tác dụng với 253,5 ml dung dịch NaOH 2M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được 3m gam chất rắn. Giá trị của m là:
Đáp án: B Phương pháp giải: Tính khối lượng chất rắn tại 3 điểm: - Nếu tạo muối Na3PO4 (theo ẩn m) - Nếu tạo muối Na2HPO4 (theo ẩn m) - Nếu tạo muối NaH2PO4 (theo ẩn m) So sánh khối lượng chất rắn đề bài cho với m1, m2, m3 từ đó suy ra được sản phẩm của phản ứng. + Nếu m chất rắn < m1 => Tạo Na3PO4 và NaOH dư + m1 < m chất rắn < m2 => Tạo Na3PO4, Na2HPO4 + m2 < m chất rắn < m3 => Tạo Na2HPO4; NaH2PO4 + m chất rắn > m3 => Tạo NaH2PO4; H3PO4 dư Lời giải chi tiết: nP2O5 = m/142 (mol) - Nếu tạo muối Na3PO4: BTNT "P": nNa3PO4 = 2nP2O5 = m/71 (mol) => m1 = 164.(m/71) ≈ 2,3m (gam) - Nếu tạo muối Na2HPO4: BTNT "P": nNa2HPO4 = 2nP2O5 = m/71 (mol) => m1 = 142.(m/71) = 2m (gam) - Nếu tạo muối NaH2PO4: BTNT "P": nNaH2PO4 = 2nP2O5 = m/71 (mol) => m1 = 120.(m/71) ≈ 1,69m (gam) Theo đề bài: m chất rắn = 3m > m1 => Dung dịch thu được chứa: Na3PO4 (a mol) và NaOH (b mol) + BTNT "Na": nNaOH bđ = 3a + b = 0,507 (1) + m chất rắn = 164a + 40b = 3m (2) + BTNT "P": 2nP2O5 = nNa3PO4 => 2.m/142 = a (3) Giải hệ (1) (2) (3) được: a = 0,12; b = 0,147; m = 8,52 Vậy m = 8,52 gam. Đáp án B Câu hỏi 16 : Đốt cháy hoàn toàn m gam P bằng oxi rồi hòa tan hoàn toàn sản phẩm cháy vào dung dịch chứa 0,1 mol H2SO4 thu được dung dịch X. Cho 0,5 mol KOH vào X, sau khi các phản ứng xảy ra hoàn toàn cô cạn dung dịch thu được 943m/62 gam chất rắn. Giá trị của m là:
Đáp án: B Phương pháp giải: Ta có: 4P + 5O2 → 2P2O5 (1) Cho sản phẩm cháy vào dung dịch chứa 0,1 mol H2SO4 thì: P2O5 + 3H2O → 2H3PO4 (2) nH3PO4 = nP = m/31 (mol) Dung dịch X chứa H3PO4 và H2SO4 Cho 0,5 mol KOH phản ứng với dung dịch X: 2KOH + H2SO4 → K2SO4 + 2H2O (3) Khi cho KOH phản ứng với H3PO4 có thể xảy ra các PTHH sau: KOH + H3PO4 → KH2PO4 + H2O (4) 2KOH + H3PO4 → K2HPO4 + 2H2O (5) 3KOH + H3PO4 → K3PO4 + 3H2O (6) Xét các trường hợp sau: - TH1: Chất rắn sau phản ứng chỉ chứa các muối Dùng định luật bảo toàn khối lượng tính giá trị m. - TH2: Chất rắn sau phản ứng có KOH dư 3KOH + H3PO4 → K3PO4 + 3H2O (6) 3m/31 m/31 m/31 Từ khối lượng chất rắn sau phản ứng tính được giá trị m. Lời giải chi tiết: Ta có: 4P + 5O2 → 2P2O5 (1) Cho sản phẩm cháy vào dung dịch chứa 0,1 mol H2SO4 thì: P2O5 + 3H2O → 2H3PO4 (2) Ta có: nH3PO4 = nP = m/31 (mol) Dung dịch X chứa H3PO4 và H2SO4 Cho 0,5 mol KOH phản ứng với dung dịch X: 2KOH + H2SO4 → K2SO4+ 2H2O (3) 0,2 ← 0,1 → 0,1 mol → Số mol KOH phản ứng với H3PO4 là 0,5 - 0,2 = 0,3 mol KOH + H3PO4 → KH2PO4 + H2O (4) 2KOH + H3PO4 → K2HPO4 + 2H2O (5) 3KOH + H3PO4 → K3PO4 + 3H2O (6) Xét các trường hợp sau: -TH1: Chất rắn sau phản ứng chỉ chứa các muối → nH2O = nKOH = 0,5 mol Theo định luật bảo toàn khối lượng ta có: mKOH + maxit = mmuối + mH2O →\(0,5.56 + {\rm{ }}0,1.98 + {\rm{ }}98.\frac{m}{{31}} = \frac{{943m}}{{62}} + {\rm{ }}0,5.18\) → m = 2,39 gam → nH3PO4 = nP = 0,077 mol → \(T = \frac{{{n_{KOH}}}}{{{n_{H3PO4}}}} = \frac{{0,3}}{{0,077}} = 3,89 > 3\) → Loại vì khi đó chất rắn sau phản ứng ngoài muối còn có KOH dư. - TH2: Chất rắn sau phản ứng có KOH dư 3KOH + H3PO4 → K3PO4 + 3H2O (6) 3m/31 m/31 m/31 Chất rắn sau phản ứng có chứa \(\left\{ \begin{array}{l}\;0,1{\rm{ }}mol\,{\rm{ }}{K_2}S{O_4}\\\frac{m}{{31}}mol\,{K_3}P{O_4}\\(0,3 - \frac{{3m}}{{31}})mol\,KOH{\rm{ }}du\end{array} \right.\) → \(0,1.174 + \frac{m}{{31}}.{\rm{ }}212 + {\rm{ }}(0,3 - \frac{{3m}}{{31}}).56 = \frac{{943m}}{{62}}\) → m = 2,48 gam Đáp án B Câu hỏi 17 : Hòa tan 3,82 gam hỗn hợp X gồm NaH2PO4, Na2HPO4 và Na3PO4 vào nước dư thu được dung dịch Y. Trung hòa hoàn toàn Y cần 50 ml dung dịch KOH 1M, thu được dung dịch Z. Khối lượng kết tủa thu được khi cho Z tác dụng hết với dung dịch AgNO3 dư là
Đáp án: C Phương pháp giải: HPO42- + OH- → PO43- + H2O H2PO4-+ 2OH- → PO43- + 2H2O PO43- + 3Ag+ → Ag3PO4 Gọi số mol của NaH2PO4, Na2HPO4 và Na3PO4 lần lượt là a, b, c mol → Phương trình khối lượng Và phương trình số mol OH- → a + b + c → mAg3PO4 Lời giải chi tiết: HPO42- + OH- → PO43- + H2O H2PO4-+ 2OH- → PO43- + 2H2O PO43- + 3Ag+ → Ag3PO4 Gọi số mol của NaH2PO4, Na2HPO4 và Na3PO4 lần lượt là a,b, c mol + mX = 120a + 142b + 164c = 3,82 (1) + nKOH = 2a + b = 0,05 mol (2) → 120a + 142b + 164b + 22.(2a + b) = 3,82 + 0,05.22 = 4,92 → 164.(a + b + c) = 4,92 → a + b + c = 0,03 → mAg3PO4 = nPO4 3- = a + b + c = 0,03.419 = 12,57 gam Đáp án C Câu hỏi 18 : Cho m gam P2O5 vào 700 ml dung dịch KOH 1M, sau khi kết thúc phản ứng, cô cạn dung dịch thu được (3m + 5,4) gam chất rắn. Giá trị của m là:
Đáp án: A Phương pháp giải: Xét 2 trường hợp sau: - TH1: Chất rắn khan chỉ chứa các muối P2O5+ 3H2O → 2 H3PO4 KOH + H3PO4 → KH2PO4 + H2O 2KOH + H3PO4 → K2HPO4 + 2H2O 3KOH + H3PO4 → K3PO4 + 3H2O Vì dung dịch sau phản ứng chỉ chứa muối nên ta có: nH2O = nKOH Áp dụng định luật bảo toàn khối lượng ta tính được giá trị m. -TH2: Chất rắn khan chứa muối và KOH dư P2O5 + 3H2O → 2 H3PO4 3KOH + H3PO4 → K3PO4 + 3H2O Tính toán theo phương trình tìm được m. Lời giải chi tiết: Ta có: \({n_{{P_2}{O_5}}} = \frac{m}{{142}}(mol)\) -TH1: Chất rắn khan chỉ chứa các muối P2O5 + 3H2O → 2 H3PO4 m/142 2m/142 mol KOH + H3PO4 → KH2PO4 + H2O 2KOH + H3PO4 → K2HPO4 + 2H2O 3KOH + H3PO4 → K3PO4 + 3H2O Vì dung dịch sau phản ứng chỉ chứa muối nên ta có: nH2O = nKOH = 0,7 (mol) Áp dụng định luật bảo toàn khối lượng ta có: mKOH + mH3PO4 = mmuối + mH2O → 0,7.56 + 2m.98/142 = 3m + 5,4 + 0,7.18 → m = 13,09 gam → nH3PO4 = 2m/142 = 0,184 mol Ta thấy: \(\frac{{{n_{KOH}}}}{{{n_{H3PO4}}}} = \frac{{0,7}}{{0,184}} > 3\) → Sau phản ứng có KOH dư → Trường hợp này loại -TH2: Chất rắn khan chứa muối và KOH dư P2O5+ 3H2O → 2 H3PO4 \(\frac{m}{{142}}\) \(\frac{{2m}}{{142}}\)mol 3KOH + H3PO4 → K3PO4 + 3H2O \(\frac{{6m}}{{142}}\) \(\frac{{2m}}{{142}}\) \(\frac{{2m}}{{142}}\) mol Chất rắn khan chứa 2m/142 mol K3PO4 và (0,7-6m/142) mol KOH → 212 . 2m/142+ 56 . (0,7-6m/142) = 3m + 5,4 → m = 14,2 gam Đáp án A Câu hỏi 19 : Cho m gam P2O5 tác dụng với 500 ml dung dịch KOH 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (không chứa H3PO4), cô cạn dung dịch X thu được 193m/71 gam chất rắn khan. Nếu cho X tác dụng với dung dịch BaCl2 dư thì thu được bao nhiêu gam kết tủa?
Đáp án: B Phương pháp giải: Xét 2 trường hợp: TH 1: Chất rắn gồm K3PO4 và KOH dư TH2: Chất rắn chỉ gồm muối. Dùng bảo toàn khối lượng để tìm số mol H3PO4, từ đó tìm được số mol mỗi muối trong dung dịch X. Khi đó viết phương trình khi cho dung dịch X tác dụng với dung dịch BaCl2 tìm được khối lượng kết tủa. Lời giải chi tiết: Đặt nP2O5 = x mol → nH3PO4 = 2x mol Nếu KOH vẫn còn dư → Chất rắn gồm K3PO4 (2x mol) và KOH dư (0,5- 6x) mol → 212.2x + 56. (0,5-6x) = 193.142/171 Suy ra x = 0,094 Loại vì 0,5 - 6x < 0. Vậy KOH phản ứng hết. Khi đó nH2O = nKOH = 0,5 mol Theo bảo toàn khối lượng: mH3PO4 + mKOH = mmuối + mH2O → 98.2x + 0,5.56 = 193.142x/71 + 0,5.18 → x = 0,1 → m = 14,2 Ta có: nH3PO4 = 0,2 mol và nKOH = 0,5 mol → X chứa K3PO4 (0,1 mol) và K2HPO4 (0,1 mol) Vậy kết tủa gồm Ba3(PO4)2 (0,05 mol) và BaHPO4 (0,1 mol) → mkết tủa = 53,35 gam Đáp án B Câu hỏi 20 : Cho m gam P2O5 tác dụng với 400 ml dung dịch NaOH 0,3M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được 1,55m gam chất rắn. Giá trị của m gần nhất với:
Đáp án: A Phương pháp giải: Xét các trường hợp sau: TH1: P2O5 và NaOH pứ vừa đủ tạo muối: nH2O = nNaOH Dùng bảo toàn khối lượng để tìm m. TH2:Chất rắn gồm: NaOHdư; Na3PO4 Dùng bảo toàn khối lượng để tìm m. Lời giải chi tiết: TH1: P2O5 và NaOH pứ vừa đủ tạo muối: nH2O = nNaOH = 0,12mol P2O5 + H2O → 2H3PO4 m/142 → 2m/142 mol Có thể xảy ra các PT: H3PO4 + NaOH → NaH2PO4+ H2O (3) H3PO4 + 2NaOH → Na2HPO4+ 2H2O (4) H3PO4 + 3NaOH → Na3PO4 + 3H2O (5) Bảo toàn khối lượng ta có: mH3PO4 + mNaOH = m rắn + mH2O (2m/142) . 98 + 0,12 . 40 = 1,55m + 0,12 . 18 →m = 15,555 gam gần nhất với 15,6 gam TH2: Chất rắn gồm: NaOHdư; Na3PO4 P2O5 + 6NaOH → 2Na3PO4 + 3H2O m/142 0,12 2m/142 3m/142 Bảo toàn khối lượng ta có: mP2O5 + mNaOHbđ = m rắn + mH2O m + 0,12 . 40 = 1,55m + 18 . 3m/142 → m = 5,16g (Loại) Đáp án A Quảng cáo
|














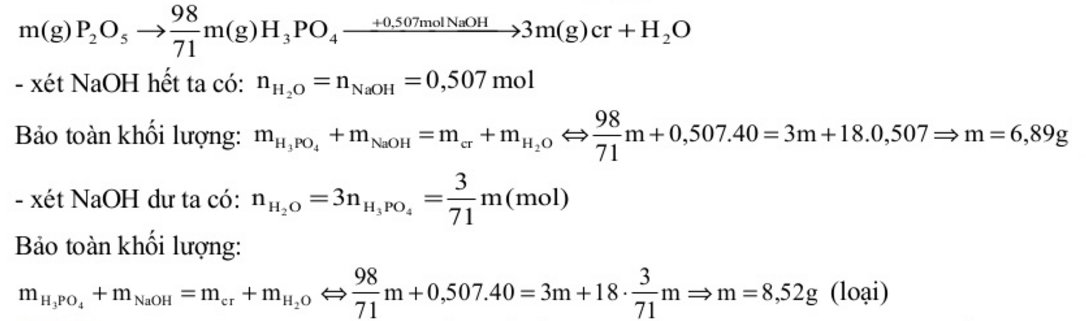
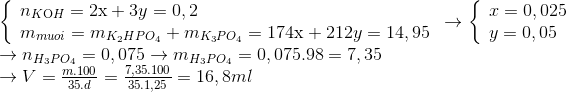
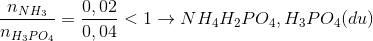
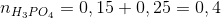 mol => nP2O5 = 0,2 mol
mol => nP2O5 = 0,2 mol