Câu hỏi:
Một hợp chất A có thành phần phần trăm về khối lượng các nguyên tố 52,17% C; 13,05% H; 34,78% O. Hợp chất này nặng gấp 23 lần phân tử hiđrô. Xác định công thức hóa học của hợp chất trên?
Phương pháp giải:
Lời giải chi tiết:
Gọi CTPT A: CxHyOz (x, y, x )
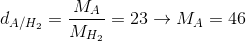
Xét 1 mol hợp chất A
\({m_C} = \frac{{52,17}}{{100}}.46 = 24(g) = > {n_C} = \frac{{24}}{{12}} = 2\left( {mol} \right)\)
\({m_H} = \frac{{13,05}}{{100}}.46 = 6(g) = > {n_H} = \frac{6}{1} = 6(mol)\)
\({m_O} = \frac{{34,78}}{{100}}.46 = 16(g) = > n{}_O = \frac{{16}}{{16}} = 1(mol)\)
Vậy công thức hóa học của A là: C2H6O
Quảng cáo


















