Câu hỏi:
Hoà tan hết 25,2g kim loại M trong dung dịch axit HCl, sau phản ứng thu được 10,08 lít H2 (đktc). Kim loại M là:
- A Zn.
- B Mg.
- C Fe.
- D Al.
Phương pháp giải:
Đổi mol H2.
Viết PTHH xảy ra: \(M + nHCl \to MC{l_n} + \frac{n}{2}{H_2}\)
Tính mol M theo mol H2. Từ đó tìm được mối liên hệ giữa MM và n. Kẻ bảng chạy giá trị của n ta tìm được M
Lời giải chi tiết:
nH2(đktc) = 10,08 : 22,4 = 0,45 (mol)
Giả sử kim loại M có hóa trị n (1 ≤ n ≤ 3)
\(M + nHCl \to MC{l_n} + \frac{n}{2}{H_2}\)
(mol) 0,45
\(\begin{array}{l}{n_{{H_2}}} = \frac{n}{2}{n_M} \Rightarrow {n_M} = \frac{{2{n_{{H_2}}}}}{n} = \frac{{0,9}}{n}\\ \Rightarrow M = \frac{{{m_M}}}{{{n_M}}} = \frac{{25,2}}{{\frac{{0,9}}{n}}} = 28n\end{array}\)
Lập bảng:
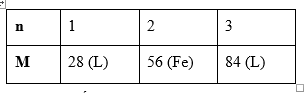
Vậy M là Sắt (Fe)
Đáp án C


















