Câu hỏi:
Cho phương trình hóa học sau: Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O
Hệ số của HNO3 trong phản ứng trên là
- A 28
- B 24
- C 10
- D 16
Phương pháp giải:
Cân bằng phương pháp thăng bằng electron
Lời giải chi tiết:
Bước 1: Xác định sự thay đổi của các nguyên tố trước và sau pư:
\(\mathop {F{e_3}}\limits^{ + 8/3} {O_4} + H\mathop N\limits^{ + 5} {O_3}\buildrel {} \over
\longrightarrow \mathop {Fe}\limits^{ + 3} {(N{O_3})_3} + \mathop N\limits^{ + 2} O + {H_2}O\)
Bước 2,3: Viết quá trình nhường-nhận e và đặt hệ số trước các chất khử và chất oxi hóa thích hợp sao cho tổng số electron nhường bằng số electron nhận.
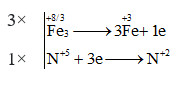
Bước 4: Đặt vào phương trình từ đó tìm được hệ số của chất tham gia phản ứng
\(\mathop {3F{e_3}}\limits^{ + 8/3} {O_4} + 28H\mathop N\limits^{ + 5} {O_3}\buildrel {} \over
\longrightarrow \mathop {9Fe}\limits^{ + 3} {(N{O_3})_3} + \mathop N\limits^{ + 2} O + 14{H_2}O\)
=> Hệ số của các HNO3 là 28
Đáp án A


















