Câu hỏi:
Hòa tan 2,74 gam một kim loại trong nước, thu được 0,448 lít H2 (đktc). Tên kim loại là:
- A Na
- B Ba
- C Ca
- D K
Phương pháp giải:
Gọi kim loại cần tìm là R, hóa trị n (n= 1,2,3)
R + nH2O → R(OH)n + n/2 H2
Ta tính được số mol của kim loại theo ẩn n
Khi đó biện luận MR theo các giá trị n.
Lời giải chi tiết:
Gọi kim loại tan trong nước là R, có hóa trị n với n=1,2, 3
R + nH2O → R(OH)n + n/2 H2
Ta có: nH2= 0,02 mol → nR= 2/n . nH2= 0,04/n (mol)
→ MR= \({{2,74} \over {{{0,04} \over n}}} = 68,5n\)
Xét các trường hợp sau:
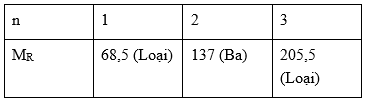
Vậy kim loại cần tìm là Ba.
Đáp án B
Quảng cáo


















