Bài 30: Lưu huỳnhLưu huỳnh là ... Quảng cáo
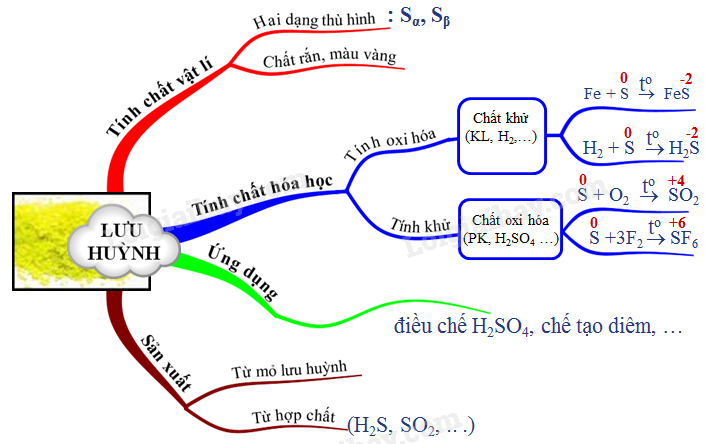
I. VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ - ZS = 16. Cấu hình e: 1s22s22p63s23p4 => S thuộc chu kì 3 nhóm VIA, và có 6 electron lớp ngoài cùng. II. TÍNH CHẤT VẬT LÍ - Lưu huỳnh có 2 dạng thù hình: Lưu huỳnh tà phương và lưu huỳnh đơn tà - Nóng chảy trong khoảng từ 113 đến 119 độ C III. TÍNH CHẤT HÓA HỌC Khảo sát số oxi hóa của S trong một số hợp chất \({{H}_{2}}\overset{-2}{\mathop{S}}\,\) \(\overset{0}{\mathop{S}}\,\) \(\overset{+4}{\mathop{S}}\,{{O}_{2}}\) \(\overset{+6}{\mathop{S}}\,{{O}_{3}}\) => S mang số oxi hóa trung gian nên thể hiện cả tính OXH và Khử khi tham gia phản ứng hóa học. 1. Tác dụng với kim loại và H2 tạo hợp chất sunfua (S2-) Fe + S \(\xrightarrow{t{}^{o}}\) FeS-2 Zn + S \(\xrightarrow{t{}^{o}}\) ZnS-2 Hg + S \(\xrightarrow{{}}\) HgS-2 H2 + S \(\xrightarrow{t{}^{o}}\) H2S-2 2. Tác dụng với phi kim S + O2 \(\xrightarrow{t{}^{o}}\) \(\overset{+4}{\mathop{S}}\,{{O}_{2}}\) S + 3F2 \(\xrightarrow{t{}^{o}}\) \(\overset{+6}{\mathop{S}}\,{{F}_{6}}\) 3. Tác dụng với các hợp chất có tính oxi hóa mạnh - S là chất khử khi tác dụng với hợp chất oxi hóa tạo hợp chất chứa lưu huỳnh trong đó S có số oxi hóa là +4 hoặc +6 S + 2H2SO4 đặc \(\xrightarrow{t{}^{o}}\) \(\overset{+4}{\mathop{3S}}\,{{O}_{2}}\) + 2H2O S + 6HNO3 đặc \(\xrightarrow{t{}^{o}}\) \({{H}_{2}}\overset{+6}{\mathop{S{{O}_{4}}}}\,\) + 6NO2 + 2H2O IV. ỨNG DỤNG - 90% Lưu huỳnh được khai thác để sản xuất H2SO4 - Phần còn lại dùng để lưu hóa cao su, sản xuất tẩy trắng bột giấy, dược phẩm, .... V. TRẠNG THÁI TỰ NHIÊN VÀ SẢN XUẤT LƯU HUỲNH - Trong tự nhiên lưu huỳnh có nhiều ở dạng đơn chất, tạo thành các mỏ lớn. Ngoài ra chúng còn có ở dạng hợp chất như muối sunfat, muối sunfua - Sản xuất lưu huỳnh bằng cách nén nước siêu nóng (170 độ C) vào mỏ làm lưu huỳnh nóng chảy, đẩy lên mặt đất. Sau đó S được tách ra khỏi các tạp chất. Sơ đồ tư duy: Lưu huỳnh
Loigiaihay.com
|




















Danh sách bình luận