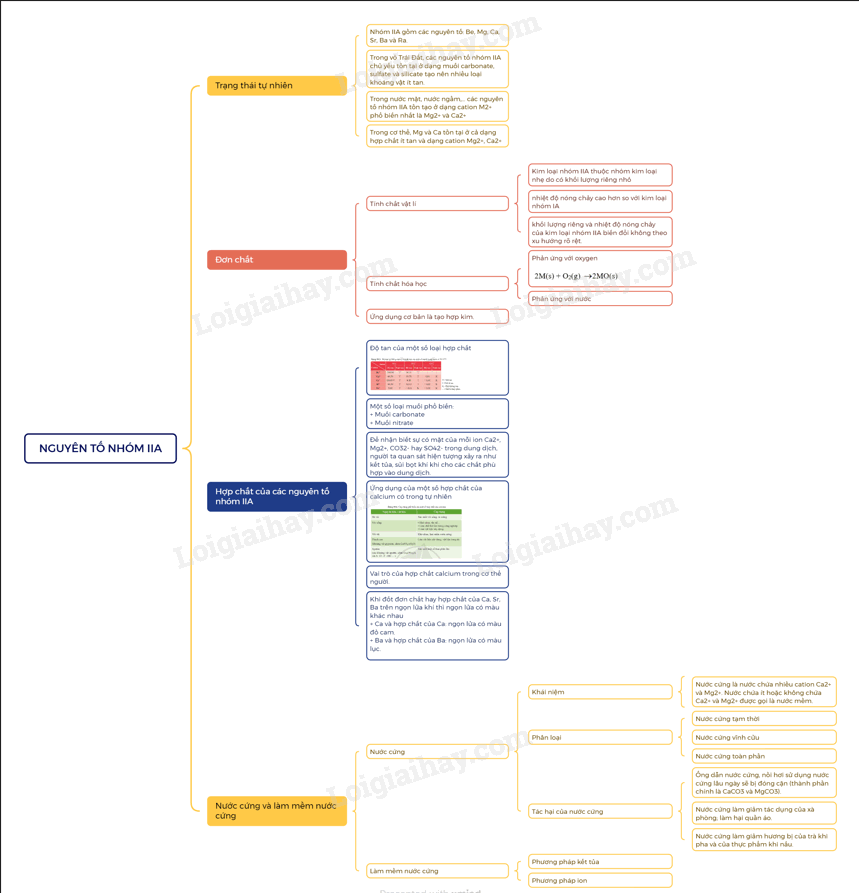
Lý thuyết Nguyên tố nhóm IIA - Hóa 12 Kết nối tri thứcKim loại nhóm IIA là những nguyên tố s, đứng ngay sau nguyên tố kim loại kiềm ở mỗi chu kì. Quảng cáo
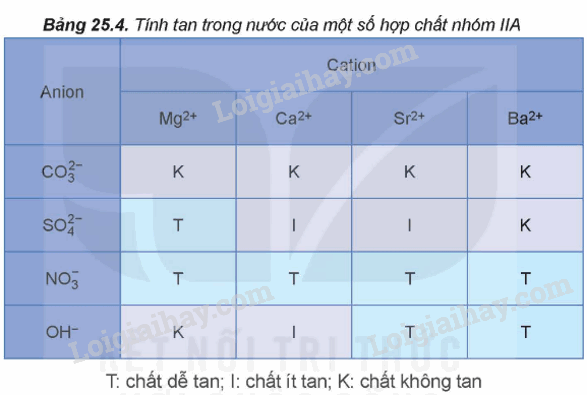
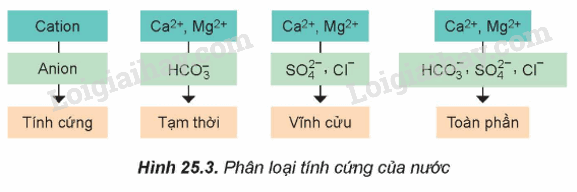
I. Đơn chất nhóm IIA 1. Đặc điểm chung - Kim loại nhóm IIA là những nguyên tố s, đứng ngay sau nguyên tố kim loại kiềm ở mỗi chu kì. - Kim loại nhóm IIA có thế điện cực chuẩn \(E_{{M^{2 + }}/M}^o\)nhỏ nên dễ tách electron hóa trị ra khỏi nguyên tử, thể hiện tính khử mạnh: M \( \to \)M2+ + 2e - Trong hợp chất, nguyên tử nhóm IIA thể hiện số oix hóa đặc trưng là +2. 2. Trạng thái tự nhiên Trong tự nhiên, các nguyên tố nhóm IIA chỉ tồn tại ở dạng hợp chất. Magnesium và calcium là hai nguyên tố phổ biến trên vỏ Trái Đất, có nhiều khoáng vật như MgCO3.CaCO3 (dolomite), CaCO3 (calcite)…. 3. Tính chất vật lí - Kim loại IIA có nhiệt độ nóng chảy cao hơn nhiệt độ nóng chảy của kim loại nhóm IA, nhưng tương đối thấp so với nhiệt độ nóng chảy của các kim loại khác. - Kim loại nhóm IIA đều là kim loại nhẹ, có khối lượng riêng tương đối nhỏ 4. Tính chất hóa học - Tác dụng với oxygen - Khi đốt nóng trong oxygen hoặc trong không khí, các kim loại nhóm IIA đều bốc cháy, tạo ra oxide theo phương trình hóa học tổng quát sau: 2M(s) + O2(g) \( \to \)2MO(s) - Khi cháy, các kim loại nhóm IIA cho ngọn lửa có màu đặc trưng. b) Phản ứng với nước Be không tan trong nước, Mg phản ứng với nước rất chậm ở nhiệt độ thường, phản ứng mạnh hơn khi đun nóng. Ca, Sr, Ba phản ứng mạnh với nước ở nhiệt độ thường. 5. Ứng dụng - Các kim loại nhóm IIA và hợp kim của chúng có nhiều ứng dụng trong thực tế: + Be dùng để chế tạo hợp kim có độ bền cơ học, không bị ăn mòn, khó nóng chảy,… + Mg dùng để chế tạo hợp kim làm vật liệu sản xuất ô tô, máy bay, chi tiết máy,… II. Hợp chất của kim loại nhóm IIA 1. Đặc điểm chung - Tính tan trong nước của một số hợp chất nhóm IIA: - Khi đốt nóng các kim loại nhóm IIA hoặc hợp chất của chúng trong ngọn lửa không màu làm ngọn lửa có màu đặc trưng: Ca2+ màu đỏ cam, Sr2+ màu đỏ son, Ba2+ màu lục. 2. Một số hợp chất quan trọng a) Muối carbonate và nitrate + Tác dụng với acid Ví dụ: MCO3 + 2HCl → MCl2 + CO2 + H2O + Phản ứng nhiệt phân Ví dụ: - Tương tự muối carbonate, các muối nitrate của kim loại nhóm IIA cũng đều bị phân hủy nhiệt tạo thành oxide. b) Nhận biết từng ion riêng rẽ Ca2+, Ba2+, SO42-, CO32- trong dung dịch. 3. Ứng dụng Các nguyên liệu, vật liệu chứa calcium như đá vôi, vôi, nước vôi, thạch cao, quặng apatite, quặng fluorite,… có nhiều ứng dụng trong đời sống và sản xuất. - Một số hợp chất của calcium còn có vai trò quan trọng đối với cơ thể con người như calcium phosphate, hydroxylapatite tham gia cấu tạo xương và răng. III. Nước cứng 1. Khái niệm, phân loại a) Khái niệm - Nước trong tự nhiên như nước mặt (nước sông, suối, ao hồ,…) và nước ngầm thường hòa tan muối của nhiều ion kim loại như Ca2+, Mg2+,… - Nước chứa nhiều ion Ca2+ và Mg2+ được gọi là nước cứng. Nước chứa ít hoặc không chứa các ion Ca2+ và Mg2+ được gọi là nước mềm. b) Phân loại 2. Tác hại của nước cứng - Nồi hơi dễ bị đóng cặn gây tốn nhiên liệu và không an toàn. - Đường ống dẫn nước dễ bị đóng cặn làm giảm lưu lượng nước hoặc tắc đường ống. - Giặt bằng xà phòng sẽ tạo ra muối ít tan bám vào quần áo, xà phòng tạo ít bọt, tốn xà phòng, quần áo mau hỏng. - Nấu ăn bằng nước cứng làm cho thực phẩm lâu chín, giảm mùi vị. 3. Làm mềm nước cứng - Nguyên tắc làm mềm nước cứng là làm giảm nồng độ các cation Ca2+ và Mg2+ trong nước cứng. a) Phương pháp kết tủa b) Phương pháp trao đổi ion. SƠ ĐỒ TƯ DUY
|














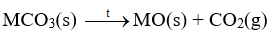







Danh sách bình luận