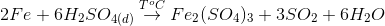30 câu hỏi lý thuyết về tính chất của axit có lời giảiLàm bàiQuảng cáo
Câu hỏi 1 : Oxit tác dụng với axit clohiđric là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Oxit tác dụng được với axit là oxit bazo hoặc oxit lưỡng tính A và B là oxit axit, D là oxit trung tính, C là oxit bazo Đáp án: C Câu hỏi 2 : Nhỏ từ từ dung dịch axit clohiđric vào cốc đựng một mẩu đá vôi cho đến dư axit. Hiện tượng nào sau đây xảy ra ?
Đáp án: D Phương pháp giải: Lời giải chi tiết: CaCO3 + HCl → CaCl2 + CO2 + H2O Đáp án: D Câu hỏi 3 : Khi nhỏ từ từ H2SO4 đậm đặc vào đường chứa trong cốc hiện tượng quan sát được là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án: C Câu hỏi 4 : Muốn pha loãng axit sunfuric đặc ta phải:
Đáp án: D Phương pháp giải: Lời giải chi tiết: Axit sunfuric đặc giống như dầu và nặng hơn trong nước do đó nếu cho nước vào axit, nước sẽ nổi trên bề mặt axit. Khi xảy ra phản ứng hóa học, nước sôi mãnh liệt và bắn tung tóe gây nguy hiểm. Khi cho axit sunfuric vào thì axit sunfuric đặc nặng hơn nước, nếu cho từ từ axit vào nước, nó sẽ chìm xuống đáy nước, sau đó phân bố đều trong toàn bộ dung dịch. Như vậy khi có phản ứng xảy ra, nhiệt lượng sinh ra được phân bố đều trong dung dịch, nhiệt độ sẽ tăng từ từ không làm cho nước sôi lên một cách quá nhanh. Đáp án: D Câu hỏi 5 : Để nhận biết gốc sunfat (= SO4) người ta dùng muối nào sau đây ?
Đáp án: A Phương pháp giải: Lời giải chi tiết: BaSO4 kết tủa trắng Đáp án: A Câu hỏi 6 : KL nào sau dây được dùng để nhận biết cả 3 dd: NaCl, CuCl2, Na2SO4
Đáp án: B Phương pháp giải: Lời giải chi tiết: Ba + 2H2O → Ba(OH)2 + H2 Khi cho Ba vào các dd muối thì Ba phản ứng với nước trước tạo thành dd Ba(OH)2 sau đó dd Ba(OH)2 phản ứng với các muối + dd chỉ xuất hiện bọt khí là NaCl + dd xuất hiện bọt khí và kết tủa màu xanh lơ CuSO4 + Ba(OH)2 → Cu(OH)2↓ + BaSO4 + dd xuất hiện bọt khí và kết tủa trắng là Na2SO4 Na2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH Đáp án B Câu hỏi 7 : CuO tác dụng với dung dịch H2SO4 tạo thành:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Phương trình hóa học: Dung dịch muối có màu xanh Đáp án C Câu hỏi 8 : Dung dịch axit làm quỳ tím :
Đáp án: B Phương pháp giải: Lời giải chi tiết: dung dịch axit làm quỳ đỏ Câu hỏi 9 : Hiện tượng quan sát được khi cho mẩu magie vào ống nghiệm chứa axit HCl dư là:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Khi cho mẩu magie vào ống nghiệm chứa axit HCl dư mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được không màu : Mg + 2HCl → MgCl2 + H2 Dung dịch MgCl2 thu được không có màu Đáp án B Câu hỏi 10 : Khi cho axit tác dụng với bazo thu được:
Đáp án: B Phương pháp giải: Lời giải chi tiết: Axit + bazo → muối và nước Đáp án B Câu hỏi 11 : Chất tác dụng với dung dịch axit sunfuric loãng là
Đáp án: C Phương pháp giải: Các oxit bazơ và các kim loại đứng trước H trong dãy điện hóa sẽ phản ứng được với dung dịch H2SO4 loãng. Lời giải chi tiết: A,B loại vì Ag, Cu là kim loại đứng sau H trong dãy điện hóa C. Thỏa mãn: PTHH: ZnO + H2SO4 → ZnSO4 + H2O D. Loại vì SO2 là oxit axit Đáp án C Câu hỏi 12 : Chất nào sau đây tan trong dung dịch HCl?
Đáp án: A Phương pháp giải: Ghi nhớ tính chất hóa học của axit HCl + làm quỳ tím chuyển sang màu đỏ + tác dụng với bazo, oxit bazo + tác dụng với kim loại đứng trước H trong dãy điện hóa + tác dụng với muối (điều kiện tạo ra muối mới không tan trong axit hoặc axit tạo thành yếu hơn axit phản ứng) Lời giải chi tiết: A. Mg(OH)2 + 2HCl → MgCl2 + H2O B. AgCl không tan trong HCl C. BaSO4 không tan trong HCl D. Cu là kim loại đứng sau H nên không phản ứng được với HCl Đáp án A Câu hỏi 13 : Dung dịch A tác dụng với CuO tạo ra dung dịch có màu xanh lam. A là
Đáp án: C Phương pháp giải: Cần xác định CuO là loại oxit gì và dung dịch nào của Cu có màu xanh lam Lời giải chi tiết: CuO là oxit bazơ => tan trong dung dịch axit H2SO4 tạo muối CuSO4 có màu xanh lam CuO + H2SO4 → CuSO4 + H2O Đáp án C Câu hỏi 14 : Chất nào sau đây tác dụng với axit HCl tạo kết tủa trắng?
Đáp án: C Phương pháp giải: Lời giải chi tiết: Chất kết tủa có chứa gốc Cl là AgCl và PbCl2 Chất tạo kết tủa trắng với HCl là AgNO3 PTHH: AgNO3 + HCl → AgCl↓trắng + HNO3 Đáp án C Câu hỏi 15 : Các kim loại nào sau đây tác dụng được với dung dịch H2SO4 loãng?
Đáp án: C Phương pháp giải: Các kim loại đứng trước H trong dãy hoạt động hóa học của kim loại có phản ứng với dd H2SO4 loãng Lời giải chi tiết: Các kim loại tác dụng được với dung dịch H2SO4 loãng là: Zn, Fe, Al, Mg. Axit không tác dụng với Cu, Ag và Au. Đáp án C Câu hỏi 16 : Chất nào sau đây tác dụng với Fe ở nhiệt độ thường tạo ra khí hiđro là
Đáp án: B Phương pháp giải: Lời giải chi tiết: Axit tác dụng với kim loại tạo muối và giải phóng khí hiđro Fe + 2HCl → FeCl2 + H2↑ Đáp án B Câu hỏi 17 : Tính chất hóa học nào không phải của axit?
Đáp án: C Phương pháp giải: Xem lại tính chất hóa học của axit Lời giải chi tiết: Tính chất hóa học không phải của axit là: Tác dụng với oxit axit. Axit không phản ứng với oxit axit Đáp án C Câu hỏi 18 : Dãy các chất không tác dụng được với dung dịch HCl là:
Đáp án: D Phương pháp giải: Dựa vào tính chất hóa học của axit + Axit tác dụng được với oxit bazơ + Axit tác dụng được với bazơ + Axit tác dụng được với muối (điều kiện: tạo thành muối mới không tan trong axit hoặc axit tạo thành yếu hơn axit phản ứng) + Axit tác dụng với kim loại đứng trước H trong dãy điện hóa học của kim loại Lời giải chi tiết: A. Loại vì Al, Fe có phản ứng. B,C Loại vì cả 3 chất đều phản ứng. D. Thỏa mãn, cả 3 chất đều không phản ứng Đáp án D Câu hỏi 19 : Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là:
Đáp án: A Phương pháp giải: Chọn chất tác dụng được với dd HCl sinh ra khí có khối lượng mol < 29 (g/mol). Lời giải chi tiết: A. Thỏa mãn vì sinh ra khí H2 (M = 2 g/mol) nhẹ hơn không khí. PTHH: Mg + 2HCl → MgCl2 + H2↑ B, C. Loại vì sinh ra khí CO2 (M = 44 g/mol) nặng hơn không khí PTHH: CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O MgCO3 + 2HCl → MgCl2 + CO2↑ + H2O D. Loại vì sinh ra khí SO2 (M = 64 g/mol) nặng hơn không khí PTHH: Na2SO3 + 2HCl → 2NaCl + SO2↑ + H2O Đáp án A Câu hỏi 20 : Dãy chất tác dụng với dung dịch H2SO4 loãng tạo thành dung dịch có màu xanh lam:
Đáp án: D Phương pháp giải: Muối đồng có màu đặc trưng là màu xanh lam ⟹ chọn các chất có phản ứng với dung dịch H2SO4 sinh ra muối đồng. Lời giải chi tiết: A. Loại vì sinh ra MgSO4 không màu. B,C. Loại vì Cu không pư với dd H2SO4. D. Thỏa mãn vì cả 2 chất cùng phản ứng sinh ra muối CuSO4 có màu xanh lam PTHH: CuO + H2SO4 → CuSO4 + H2O Cu(OH)2 + H2SO4 → CuSO4 + 2H2O Đáp án D Câu hỏi 21 : Cho một mẫu giấy quỳ tím vào dung dịch NaOH. Thêm từ từ dung dịch HCl vào cho đến dư ta thấy màu giấy quì:
Đáp án: D Phương pháp giải: Dựa vào sự đổi màu của quỳ tím + Môi trường axit quỳ tím chuyển sang màu xanh + Môi trường trung tính quỳ tím vẫn có màu tím + Môi trường bazơ quỳ tím có màu xanh. Lời giải chi tiết: Cho quỳ tím vào dd NaOH quỳ tím có màu xanh. Thêm từ từ dd HCl đến dư ta thấy quỳ tím chuyển dần sang màu đỏ do có phản ứng: NaOH + HCl → NaCl + H2O Do đó dd thu được chứa NaCl và HCl dư ⟹ có môi trường axit nên làm quỳ tím chuyển sang màu đỏ. Đáp án D Câu hỏi 22 : Chất phản ứng được với dung dịch HCl tạo ra một chất khí có mùi hắc, nặng hơn không khí và làm đục nước vôi trong:
Đáp án: B Phương pháp giải: Xác định được khí mùi hắc, nặng hơn không khí và làm đục nước vôi trong là khí SO2. Từ đó xác định chất phản ứng với HCl sinh ra được khí SO2. Lời giải chi tiết: Khí mùi hắc, nặng hơn không khí và làm đục nước vôi trong là khí SO2. A. Loại vì sinh ra khí H2 ; PTHH: Zn + 2HCl → ZnCl2 + H2↑ B. Thỏa mãn vì sinh ra khí SO2; PTHH: Na2SO3 + 2HCl → 2NaCl + SO2↑ + H2O C. Loại vì sinh ra khí H2S có mùi trứng thối; PTHH: FeS + 2HCl → FeCl2 + H2S↑ D. Loại vì sinh ra CO2 không có mùi; PTHH: Na2CO3 2HCl → NaCl + CO2↑ + H2O Đáp án B Câu hỏi 23 : Dãy các chất không tác dụng được với dung dịch H2SO4 loãng là:
Đáp án: B Phương pháp giải: Ghi nhớ tính chất hóa học của axit: làm quỳ tím chuyển sang màu đỏ, tác dụng với oxit bazo, bazo, kim loại đứng trước H, tác dụng với muối Lời giải chi tiết: Oxit bazo, bazo và một số muối tác dụng được với dung dịch H2SO4 loãng => Đáp án: B vì có Cu đứng sau H2 không tác dụng được với H2SO4 Đáp án B Câu hỏi 24 : Để phân biệt 2 dung dịch HCl và H2SO4 loãng. Ta dùng kim loại
Đáp án: B Phương pháp giải: Lời giải chi tiết: H2SO4 tác dụng với Ba xuất hiện khí và kết tủa trắng còn HCl chỉ xuất hiện khí PTHH: Ba + H2SO4 → BaSO4↓ + H2↑ Ba + 2HCl → BaCl2 + H2↑ Đáp án B Câu hỏi 25 : Dãy gồm các kim loại tác dụng được với dung dịch H2SO4 loãng là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Các kim loại đứng trước H2 mới phản ứng được với H2SO4 loãng A, B loại vì Cu đứng sau H2 D loại vì Ag đứng sau H2 Đáp án C Câu hỏi 26 : Cặp chất nào sau đây tác dụng với nhau sinh ra chất khí cháy trong không khí với ngọn lửa màu xanh?
Đáp án: A Phương pháp giải: Lời giải chi tiết: A đúng vì Zn + HCl → ZnCl2 + H2. H2 cháy dưới ngọn lửa màu xanh B sai vì phản ứng không tạo ra khí C sai vì phản ứng không tạo ra khí D sai vì phản ứng không tạo ra khí Đáp án A Câu hỏi 27 : Muốn nhận biết dung dịch Na2SO4 người ta dùng chất nào dưới đây làm thuốc thử?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Để nhận biết Na2SO4 người ta dùng Ba(OH) 2 làm thuốc thử vì tạo kết tủa trắng BaSO4 Đáp án D Câu hỏi 28 : Khi cho kim loại Fe tác dụng với axit H2SO4 đặc, nóng, dư không tạo thành sản phẩm nào trong các sản phẩm sau đây?
Đáp án: A Phương pháp giải: Lời giải chi tiết:
→ pư không tạo FeSO4 Đáp án A Câu hỏi 29 : Trong công nghiệp, sản xuất axitsunfuric qua mấy công đoạn
Đáp án: C Phương pháp giải: Lời giải chi tiết: Sản xuất axit sunfuric gồm 3 giai đoạn: Giai đoạn 1: Đốt lưu huỳnh cháy trong không khí S + O2 \(\xrightarrow{{{t^0}}}\) SO2 Giai đoạn 2: sản xuất SO3 bằng cách oxi hóa SO2 2SO2 + O2 \(\xrightarrow[{{{450}^0}C}]{{{V_2}{O_5}}}\) 2SO3 Giai đoạn 3: Cho SO3 tác dụng với nước để điều chế H2SO4 SO3 + H2O → H2SO4 Đáp án C Câu hỏi 30 : Cho các dãy chất dưới đây, dãy chất nào tác dụng được với dung dịch axit sunfuric loãng?
Đáp án: C Phương pháp giải: Dựa vào tính chất hóa học của axit H2SO4 loãng + Tác dụng với oxit bazo, bazo + Tác dụng với kim loại đứng trước H trong dãy điện hóa + Tác dụng với muối Lời giải chi tiết: A. Loại Cu và CO không phản ứng B. Loại CO2 không phản ứng C. Thỏa mãn D. Loại CO2 không phản ứng Đáp án C Quảng cáo
|