30 bài tập về liên kết cộng hóa trị có lời giải (phần 2)Làm bàiQuảng cáo
Câu hỏi 1 : Định nghĩa nào sau đây đúng với liên kết kết cộng hóa trị?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Câu hỏi 2 : Hãy cho biết những phân tử nào sau đây có sự phân cực trong liên kết?
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án B Sự phân cực trong liên kết chỉ xảy ra khi liên kết giữa các chất có độ âm điện chênh lệch nhau nhiều I2 , F2 , O2 liên kết giữa 2 chất có cùng độ âm điện nên sẽ không có sự phân cực Câu hỏi 3 : Liên kết trong phân tử nào dưới đây không phải là liên kết cộng hóa trị?
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Na2O : liên kết ion ( hình thành giữa kim loại mạnh và phi kim manh ) Câu hỏi 4 : Hoàn thành nội dung sau: “ Trong hợp chất cộng hóa trị, hóa trị của một nguyên tố được xác định bằng…….của nguyên tử nguyê tố đó trong phân tử”
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 5 : Cho các liên kết sau: H−O, N−H, N−F, N−O. Liên kết nào là liên kết phân cực mạnh nhất
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Độ âm điện của các chất : H : 2,2 , N : 3,04 , O : 3,44 , F : 3,98 Hiệu độ âm điện càng lớn thì càng phân cực : H – O : hiệu độ âm điện lớn nhất ( 1,24 ) Câu hỏi 6 : Cho các hợp chất sau: MgCl2, Na2O, NCl3, HCl, KCl. Hai hợp chất nào sau đây có liên kết cộng hóa trị?
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Hiệu độ âm điện nhỏ hơn 1,7 là liên kết cộng hóa trị Liên kết ion chỉ xảy ra ở các kim loại mạnh với phi kim mạnh Câu hỏi 7 : Xung quanh nguyên tử Bo ( Z = 5) trong phân tử BF3 có bao nhiêu electron?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Bo ( Z = 5) : 1s22s22p1 : cho đi 3 e để đạt cấu hình bền vững F ( Z= 9 ) : 1s22s22p5 : nhận 1 e để đạt cấu hình bền vững => BF3 : 1 nguyên tử Bo đã cho đi 3 e để 3 nguyên tử F đạt cấu hình bền vững ( mỗi 1 F nhận 1 e ) => Xung quanh Bo có 8 e ( bao gồm 2 e cũ và 6 e từ liên kết với F ) Câu hỏi 8 : Trong phân tử NH4Cl có bao nhiêu liên kết CHT?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Trong phân tử NH4Cl có tồn tại 3 kiểu liên kết : ion giữa NH4+ và Cl- cộng hoá trị có cực giữa N và H trong NH3 ( 3 liên kết với 3 H ) cộng hoá trị theo kiểu cho - nhận giữa NH3 và H thứ 4 Câu hỏi 9 : Liên kết hóa học giữa các nguyên tử trong phân tử H2O là liên kết:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Hiệu độ âm điện nằm trong khoảng từ 0,4 đến 1,7 là liên kết cộng hóa trị phân cực Câu hỏi 10 : Phát biểu nào sau đây sai khi nói về liên kết trong phân tử HCl
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Clo có độ âm điện lớn hơn nhiều so với hidro nên cặp e bị clo hút lệch về phía Clo Câu hỏi 11 : Phân tử nào sau đây có liên kết cộng hóa trị phân cực mạnh?
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D Clo có độ âm điện lớn hơn nhiều so với hidro nên cặp e bị clo hút lệch về phía Clo Câu hỏi 12 : Liên kết cộng hóa trị là:
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C ĐN: Liên kết cộng hoá trị là liên kết được tạo nên giữa 2 nguyên tử bằng 1 hay nhiều cặp electron Câu hỏi 13 : Nguyên tử X có cấu hình electron 1s22s2p63s23p3. Công thức phân tử hợp chất khí của X với hiđro là:
Đáp án: D Phương pháp giải: Lời giải chi tiết: Đáp án D 1s22s2p63s23p3 : có 5 e lớp ngoài cùng => cần nhận 3 electron để đạt cấu hình bão hòa 1s22s2p63s23p3 : có tổng 15 e => là P ð Hợp chất với Hidro là : PH3 Câu hỏi 14 : Liên kết cộng hóa trị là liên kết
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án B Câu hỏi 15 : Cho các phát biểu sau: (a) Liên kết trong phân tử HCl, H2O là liên kết cộng hóa trị có cực. (b) Trong phân tử CH4, nguyên tố C có cộng hóa trị là 4. (c) Dãy sắp xếp thứ tự tăng dần độ phân cực liên kết trong phân tử: H2O, H2S, Na2O, K2O (biết ZO = 8; ZS = 16). (d) Trong phân tử C2H2 có một liên kết ba. Phát biểu không đúng là
Đáp án: B Phương pháp giải: Lời giải chi tiết: (c) Sai vì: + Độ âm điện O > S => χO – χH > χS – χH => H-O phân cực hơn H-S + Độ âm điện Na > K => χO – χNa < χO – χK => Na-O kém phân cực hơn K-O Đáp án B Câu hỏi 16 : Trong số các chất sau: HF, CaO, CH4, N2, Số lượng các chất có liên kết cộng hóa trị và liên kết ion lần lượt là
Đáp án: B Phương pháp giải: Lời giải chi tiết: Chất có liên kết cộng hóa trị: HF, CH4, N2 Chất có liên kết ion: CaO Đáp án B Câu hỏi 17 : Trong phân tử sẽ có liên kết cộng hoá trị phân cực nếu cặp electron chung...
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án B Câu hỏi 18 : Liên kết hóa học giữa các nguyên tử trong phân tử HCl thuộc loại liên kết
Đáp án: C Phương pháp giải: Lời giải chi tiết: Đáp án C Câu hỏi 19 : Liên kết cộng hóa trị trong phân tử HCl có đặc điểm
Đáp án: D Phương pháp giải: Trong hợp chất cộng hóa trị, các nguyên tử có xu hướng nhận hoặc nhường e để đạt cấu hình bền vững của khí hiếm. Lời giải chi tiết: Cấu hình e của 1H: 1s1 =>H có xu hướng nhận thêm 1e để đạt cấu hình bền của He (1s2) Cấu hình e của 17Cl: 1s22s22p63s23p5 =>Cl có xu hướng nhận thêm 1e để đạt cấu hình bền của Ar (1s22s22p63s23p6) Như vậy H và Cl góp chung 1e để đạt cấu hình bền
Như vậy liên kết H-Cl có một cặp e chung, là liên kết đơn, phân cực về phía Cl (do Cl có độ âm điện lớn hơn H). Đáp án D Câu hỏi 20 : Kiểu liên kết tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung được gọi là
Đáp án: A Phương pháp giải: Lời giải chi tiết: Đáp án A Câu hỏi 21 : Liên kết hóa học trong phân tử Br2 thuộc loại liên kết
Đáp án: D Phương pháp giải: Liên kết giữa 2 nguyên tử cùng loại là liên kết cộng hóa trị không cực. Lời giải chi tiết: Liên kết giữa 2 nguyên tử cùng loại là liên kết cộng hóa trị không cực. Đáp án D Câu hỏi 22 : Trong phân tử N2, số cặp electron dùng chung là (cho 7N)
Đáp án: C Phương pháp giải: Viết cấu hình e của 7N từ đó dự đoán sự nhường hoặc nhận e để đạt được cấu hình của khí hiếm. Lời giải chi tiết: Cấu hình e của 7N là 1s22s22p3 => N thiếu 3 e để đạt được cấu hình bền của khí hiếm Ne 1s22s22p6 => Trong phân tử N2, mỗi nguyên tử N góp chung 3e để mỗi nguyên tử đạt cấu hình bền => Số cặp e dùng chung là 3 Đáp án C Câu hỏi 23 : Chọn câu đúng nhất về liên kết cộng hoá trị. Liên kết cộng hoá trị là liên kết:
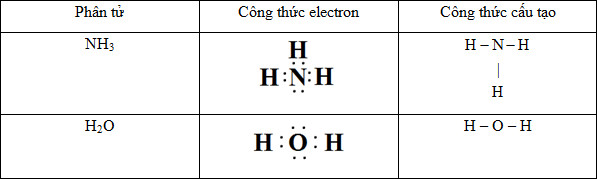
Đáp án: B Phương pháp giải: Lời giải chi tiết: Đáp án B Câu hỏi 24 : Viết công thức e và công thức cấu tạo của H2O, NH3. Phương pháp giải: Viết công thức electron và công thức cấu tạo của phân tử dựa vào quy tắc bát tử. Lời giải chi tiết:
Câu hỏi 25 : Chất nào sau đây có liên kết cộng hóa trị không cực?
Đáp án: C Phương pháp giải: Định nghĩa về liên kết cộng hóa trị phân cực và không phân cực - Liên kết cộng hóa trị: tạo nên bằng 1 hoặc nhiều cặp electron chung - Liên kết cộng hóa trị phân cực: cặp e chung bị lệch về phía nguyên tử có độ âm điện lớn hơn - Liên kết cộng hóa trị không phân cực: cặp e chung không bị lệch bề nguyên tử nào Lời giải chi tiết: Ta thấy O2 có 2 nguyên tử O cùng độ âm điện => tạo được liên kết cộng hóa trị không phân cực Đáp án C Câu hỏi 26 : Chọn câu đúng nhất về liên kết cộng hóa trị. Liên kết cộng hóa trị là liên kết
Đáp án: D Phương pháp giải: Dựa vào khái niệm về liên kết cộng hóa trị Lời giải chi tiết: Liên kết cộng hóa trị là liên kết được tạo thành giữa 2 nguyên tử bằng một hay nhiều cặp electron chung. Đáp án D Câu hỏi 27 : Chọn phát biểu sai trong các câu sau.
Đáp án: D Phương pháp giải: Dựa vào khái niệm các loại liên kết hóa học, đặc điểm của từng loại liên kết hóa học. Lời giải chi tiết: - Liên kết cộng hóa trị là liên kết được tạo thành giữa 2 nguyên tử bằng một hay nhiều cặp electron chung (hai nguyên tử đó có thể giống hoặc khác nhau về tính chất hóa học) → A đúng (ví dụ: CO2); B đúng (ví dụ: Cl2, O2, CO) - Liên kết ion là liên kết hóa học được hình thành bằng lực hút tĩnh điện giữa các ion mang điện tích trái dấu (1 nguyên tử nhường electron tạo thành cation, 1 nguyên tử nhận electron tạo thành anion → hai nguyên tử đó có tính chất hóa học trái ngược nhau) → C đúng. - Liên kết ion là được hình thành giữa một kim loại điển hình (IA) và một phi kim điển hình (VIIA). → D sai. Đáp án D Câu hỏi 28 : Tuỳ thuộc vào số cặp electron dùng chung tham gia tạo thành liên kết cộng hóa trị giữa 2 nguyên tử mà liên kết được gọi là
Đáp án: C Phương pháp giải: Dựa vào cách viết công thức electron và sự quy ước: 1 đôi electron = 1 liên kết “–”. Lời giải chi tiết: - Trong liên kết cộng hóa trị, tùy vào số cặp electron dùng chung mà liên kết tạo thành là liên kết đơn (1 cặp electron dùng chung), liên kết đôi (2 cặp electron dùng chung), liên kết ba (3 cặp electron dùng chung). - Liên kết đơn = liên kết σ; liên kết đôi = 1 liên kết σ + 1 liên kết π Đáp án C Câu hỏi 29 : Liên kết hóa học trong phân tử F2, Cl2, O2 đều là:
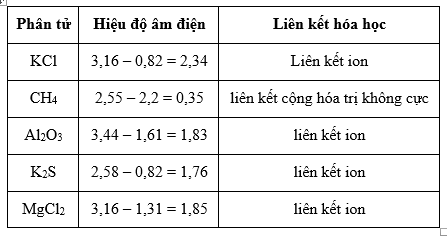
Đáp án: C Phương pháp giải: Dựa vào đặc điểm của liên kết cộng hóa trị. Lời giải chi tiết: Liên kết giữa hai nguyên tử giống nhau có hiệu độ âm điện bằng 0 ® liên kết cộng hóa trị không cực Đáp án C Câu hỏi 30 : Cho các chất KCl, CH4, Al2O3, K2S, MgCl2. Số chất có liên kết cộng hóa trị không cực là (độ âm điện của K: 0,82; Al: 1,61; S: 2,58; Cl: 3,16; O: 3,44; Mg: 1,31; H: 2,2; C: 2,55)
Đáp án: A Phương pháp giải: Tính hiệu độ âm điện ∆ + 0 ≤ ∆ < 0,4: liên kết cộng hóa trị không cực + 0,4 ≤ ∆ < 1,7: liên kết cộng hóa trị có cực. + ∆ ≥ 1,7: liên kết ion. Lời giải chi tiết:
Đáp án A Quảng cáo
|