Câu hỏi:
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M → Mn+ + ne
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học:
+ Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
+ Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Điều kiện xảy ra sự ăn mòn điện hóa học là:
+ Các điện cực phải khác nhau về bản chất, có thể là cặp 2 kim loại khác nhau hoặc cặp kim loại với phi kim,…
+ Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn.
+ Các điện cực cùng tiếp xúc với một dung dịch chất điện li.
Một sinh viên thực hiện thí nghiệm sau:
Thí nghiệm 1:
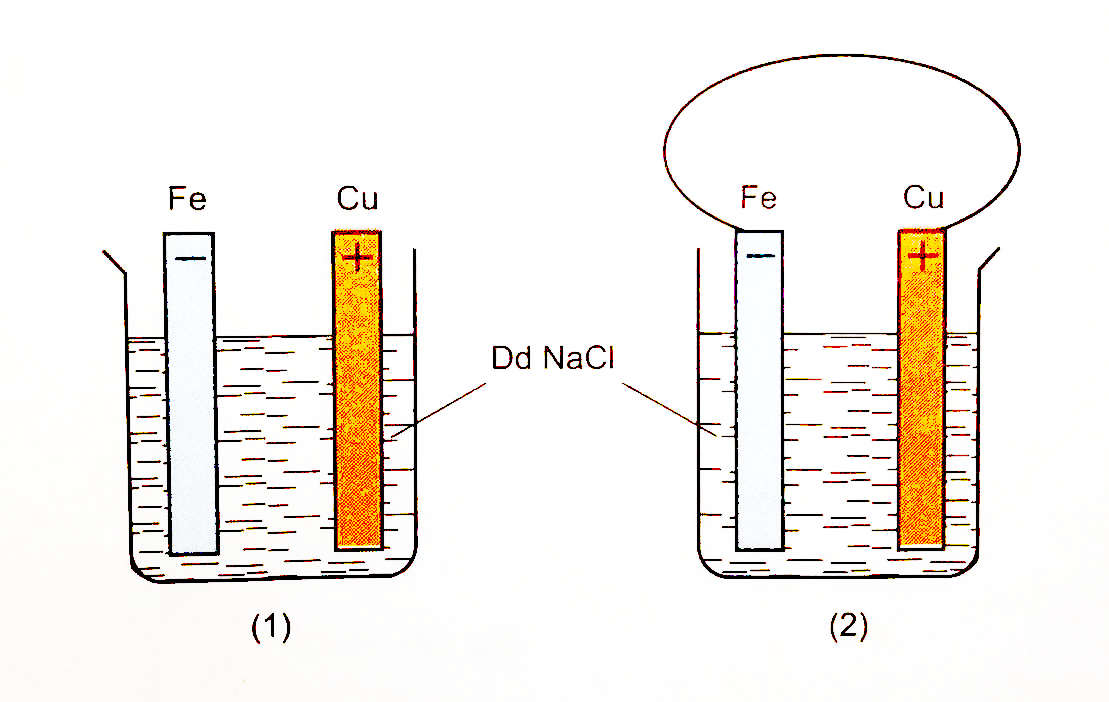
- Rót các thể tích NaCl đậm đặc bằng nhau vào 2 cốc thủy tinh.
- Cắm một lá sắt và một lá đồng vào mỗi cốc.
- Nhỏ vào mỗi cốc 5 - 7 giọt dung dịch kali ferixianua K3[Fe(CN)6] (là thuốc thử nhận biết ion Fe2+ vì thuốc thử phản ứng với muối sắt(II) tạo kết tủa màu xanh là sắt(II) ferixianua Fe3[Fe(CN)6]2).
- Nối lá Fe và lá Cu trong cốc (2) bằng một dây dẫn.
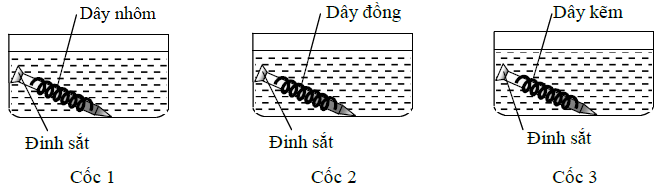
Thí nghiệm 2: Tiến hành thí nghiệm như hình vẽ sau (3 cốc đều chứa dung dịch NaCl đậm đặc có cùng thể tích và nồng độ mol):
Câu 1:
Trong Thí nghiệm 1, hiện tượng quan sát được là
- A cốc (1) xuất hiện kết tủa xanh, cốc (2) không hiện tượng.
- B cốc (1) và cốc (2) đều xuất hiện kết tủa xanh.
- C cốc (1) không hiện tượng, cốc (2) xuất hiện kết tủa xanh.
- D cốc (1) và cốc (2) đều không có hiện tượng gì.
Phương pháp giải:
- Điều kiện xảy ra sự ăn mòn điện hóa học là:
+ Các điện cực phải khác nhau về bản chất, có thể là cặp 2 kim loại khác nhau hoặc cặp kim loại với phi kim,…
+ Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn.
+ Các điện cực cùng tiếp xúc với một dung dịch chất điện li.
- Trong pin điện, chất có tính khử mạnh hơn đóng vai trò anot, chất có tính khử yếu hơn đóng vai trò là catot:
+ Tại anot xảy ra quá trình oxi hóa.
+ Tại catot xảy ra quá trình khử.
Lời giải chi tiết:
*Cốc (1): Không có sự ăn mòn điện hóa do 2 thanh kim loại không tiếp xúc trực tiếp/gián tiếp qua dây dẫn.
⟹ Cốc (1) không có hiện tượng.
*Cốc (2): Có sự ăn mòn điện hóa do thỏa mãn cả 3 điều kiện xảy ra hiện tượng ăn mòn điện hóa:
+ Có 2 điện cực Fe và Cu.
+ 2 điện cực tiếp xúc gián tiếp với nhau qua dây dẫn.
+ 2 điện cực cùng tiếp xúc với dung dịch chất điện li là NaCl.
Tính khử của Fe mạnh hơn Cu nên Fe đóng vai trò anot (-) và bị ăn mòn: Fe → Fe2+ + 2e.
⟹ Cốc (2) xuất hiện kết tủa xanh.
Chọn C.
Câu 2:
Trong Thí nghiệm 1, để hiện tượng xảy tương tự ta có thể thay thanh đồng bằng thanh kim loại nào sau đây?
- A Mg.
- B Ni.
- C Al.
- D Zn.
Phương pháp giải:
Trong pin điện hóa, kim loại đóng vai trò anot (kim loại có tính khử mạnh hơn) bị ăn mòn.
Lời giải chi tiết:
Ta có thể thay kim loại Cu bằng kim loại Ni. Vì Fe có tính khử mạnh hơn Ni nên đóng vai trò anot (-) và bị ăn mòn điện hóa.
Chọn B.
Câu 3:
Trong Thí nghiệm 2, đinh sắt trong cốc nào được bảo vệ?
- A Cốc 2.
- B Cốc 3.
- C Cốc 1.
- D Cốc 1 và cốc 3.
Phương pháp giải:
Trong pin điện hóa, kim loại đóng vai trò anot (kim loại có tính khử mạnh hơn) bị ăn mòn.
Lời giải chi tiết:
So sánh về tính khử: Al > Zn > Fe > Cu.
Trong pin điện hóa, kim loại đóng vai trò anot (kim loại có tính khử mạnh hơn) bị ăn mòn.
⟹ Đinh sắt được bảo vệ khi được quấn xung quanh bởi một kim loại có tính khử mạnh hơn.
⟹ Cốc 1 và cốc 3 đinh sắt được bảo vệ.
Chọn D.


















