Câu hỏi:
Hòa tan hoàn toàn m gam Al vào dung dịch loãng chứa 0,2 mol H2SO4, thu được khí H2 và dung dịch X. Cho từ từ dung dịch NaOH 2M vào X, kết quả thí nghiệm được ghi ở bảng sau:
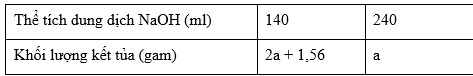
Giá trị của m và a lần lượt là
- A 5,4 và 1,56.
- B 5,4 và 4,68.
- C 2,7 và 4,68.
- D 2,7 và 1,56.
Phương pháp giải:
\(Al{\rm{ }} + {\rm{ }}\mathop {{H_2}S{O_4}}\limits_{0,2\,mol} \buildrel {} \over
\longrightarrow dd\,X\left\{ \matrix{
A{l_2}{(S{O_4})_3}:x \hfill \cr
{H_2}S{O_4}:y \hfill \cr} \right. + {H_2}\)
+ BT SO42-: 3x + y = 0,2 (1)
Khi cho NaOH vào dd X xảy ra theo thứ tự:
H+ + OH- → H2O
Al3+ + 3OH-→ Al(OH)3↓
Al(OH)3 + OH- → AlO2- + 2H2O
+ Nếu như kết tủa đạt max: nNaOH = 3nAl3+ + nH+ = 6x + 2y = 0,4 mol
Vậy với trường hợp nNaOH = 0,28 mol kết tủa chưa tạo cực đại; trường hợp nNaOH = 0,48 mol kết tủa tạo cực đại rồi tan 1 phần
Lời giải chi tiết:
\(Al{\rm{ }} + {\rm{ }}\mathop {{H_2}S{O_4}}\limits_{0,2\,mol} \buildrel {} \over
\longrightarrow dd\,X\left\{ \matrix{
A{l_2}{(S{O_4})_3}:x \hfill \cr
{H_2}S{O_4}:y \hfill \cr} \right. + {H_2}\)
+ BT SO42-: 3x + y = 0,2 (1)
Khi cho NaOH vào dd X xảy ra theo thứ tự:
H+ + OH- → H2O
Al3+ + 3OH-→ Al(OH)3↓
Al(OH)3 + OH- → AlO2- + 2H2O
+ Nếu như kết tủa đạt max: nNaOH = 3nAl3+ + nH+ = 6x + 2y = 0,4 mol
Vậy đồ thị 1 điểm bên trái và 1 điểm bên phải
+ Xét điểm 0,28 mol: \(\left\{ \matrix{Al{(OH)_3}:{{2a + 1,56} \over {78}} \hfill \cr A{l^{3 + }} \hfill \cr} \right. \Rightarrow {{2a + 1,56}\over {78}}.3 + 2y = 0,28\,(2)\)
+ Xét đểm 0,48 mol \(\left\{ \matrix{Al{(OH)_3}:{a \over {78}} \hfill \cr Al{O_2}^ - :(2x - {a \over {78}}) \hfill \cr} \right. \Rightarrow 3{a \over {78}} + 4(2x - {a \over {78}}) + 2y = 0,48\,(3)\)
\(\buildrel {(1)\,(2)\,(3)} \over
\longrightarrow \left\{ \matrix{
x = 0,05 \hfill \cr
y = 0,05 \hfill \cr
a = 1,56 \hfill \cr} \right. \Rightarrow m = 2x.27 = 2,7\,gam\)
Đáp án D


















