Câu hỏi:
Hỗn hợp X gồm Ba, BaO, Al2O3. Hoà tan hết m gam hỗn hợp X vào nước dư thu được dung dịch Y và a mol H2. Rót từ từ dung dịch H2SO4 vào dung dịch Y ta có đồ thị biểu diễn số mol kết tủa vào số mol H2SO4 như sau:
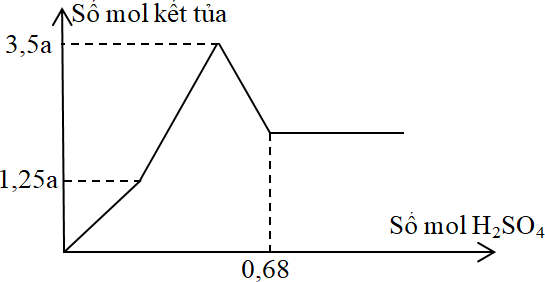
Hấp thụ 3a mol CO2 vào dung dịch Y thu được m1 gam kết tủa. Giá trị của m1 là
- A 51,08
- B 50,24
- C 52,18
- D 48,68
Phương pháp giải:
Lời giải chi tiết:
Do đoạn 1 kết tủa tăng chậm sau đó tăng nhanh ở đoạn 2 nên suy ra dung dịch Y chứa:
Ba2+ (x mol), OH- (y mol) và AlO2- (z mol)
BTĐT có: 2x = y + z (1)
+ Đoạn 1:
H+ + OH- → H2O
Ba2+ + SO42- → BaSO4
Tại điểm cuối đoạn 1:
=> nH+ = nOH- = y mol => nH2SO4 = 0,5y (mol)
=> n kết tủa = nBaSO4 = nH2SO4 => 1,25a = 0,5y => a = 0,4y (2)
+ Đoạn 2:
H+ + AlO2- + H2O → Al(OH)3
Ba2+ + SO42- → BaSO4
Tại điểm cuối đoạn 2 thì Al(OH)3 và BaSO4 đều max
=> n kết tủa = nBaSO4 max + nAl(OH)3 max => 3,5a = x + z (3)
+ Đoạn 3:
3H+ + Al(OH)3 → Al3+ + 3H2O
Cuối đoạn 3 thì Al(OH)3 bị hòa tan hết: nH+ = nOH- + 4nAlO2- => 0,68.2 = y + 4z (4)
Giải (1) (2) (3) (4) được: x = 0,32; y = 0,4; z = 0,24; a = 0,16
Vậy dung dịch Y chứa: Ba2+ (0,32 mol), OH- (0,4 mol) và AlO2- (0,24 mol)
Khi dẫn 0,48 mol CO2 vào dung dịch Y thu được:
Al(OH)3 (0,24 mol)
BaCO3: u mol
Ba(HCO3)2: v mol
Giải hệ: nBa2+ = u + v = 0,32 và nCO2 = u + 2v = 0,48 được u = v = 0,16
=> m kết tủa = mAl(OH)3 + mBaCO3 = 0,24.78 + 0,16.197 = 50,24 gam
Đáp án B


















