Cho hỗn hợp bột X gồm Al, Fe2O3, Fe3O4 (có cùng số mol). Đem nung 41,9 gam hỗn hợp X trong điều kiện không có không khí thu được hỗn hợp Y. Hòa tan Y trong dung dịch H2SO4 đặc, nóng, dư thu được V lít khí SO2 (là sản phẩm khử duy nhất ở đktc). Giá trị V là
-
A.
5,60 lít.
-
B.
4,48 lít.
-
C.
8,96 lít.
-
D.
11,20 lít
+) Sử dung pp quy đổi và bảo toàn e: 3.nAl + 3.nFe = 2.nO + 2.nSO2
Gọi ${{n}_{Al}}={{n}_{F{{\text{e}}_{2}}{{O}_{3}}}}={{n}_{F{{\text{e}}_{3}}{{O}_{4}}}}=a\,mol$
=> mhh X = 27a + 160a + 232a = 41,9 => a = 0,1 mol
=> quy hỗn hợp X về Al (0,1 mol), Fe (0,1.2 + 0,1.3 = 0,5 mol) và O (0,1.3 + 0,1.4 = 0,7 mol)
Xét toàn bộ quá trình ta có:
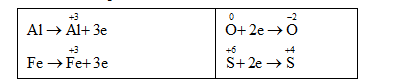
Bảo toàn e: 3.nAl + 3.nFe = 2.nO + 2.nSO2
=> nSO2 = (3.0,1 + 3.0,5 – 2.0,7) : 2 = 0,2 mol
=> V = 0,2.22,4 = 4,48 lít
Đáp án : B

Các bài tập cùng chuyên đề


















Danh sách bình luận