Một nhà máy muốn xác định độ cứng tổng và nồng độ ion Ca²⁺ của mẫu nước khoáng. Trong Phần A, kỹ sư chuẩn độ 50 cm³ nước khoáng với ethylenediaminetetraacetic acid (EDTA) 0,01 M, mất 18,5 mL EDTA để chuyển màu đỏ rượu sang xanh da trời. Trong Phần B, kỹ sư thêm NaOH để loại Mg²⁺, sau đó chuẩn độ 50 cm³ nước khoáng với EDTA 0,01 M, mất 12,4 mL để chuyển sang màu xanh da trời. Hãy tính Nồng độ Mg²⁺ (ppm) trong nước. Biết ppm số mg chất tan trong 1 L dung dịch và phương trình chuẩn độ như sau:
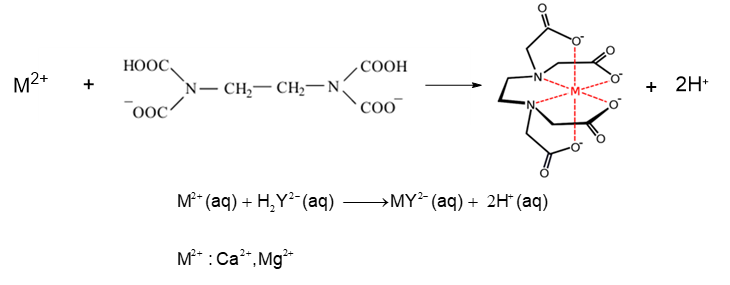
Tính nồng độ EDTA sau đó tính nồng độ Mg2+.
n EDTA trong phần 1 = 18,5.0,01 = 0,185 mmol.
n EDTA trong phần 2 = 12,4.0,01 = 0,124 mmol => n Ca2+ = 0,124 mmol => n Mg2+ = 0,185 – 0,124 = 0,061 mmol.
Đổi 50 cm3 = 0,05L.
Nồng độ Mg2+ là: 0,061.24 : 0,05 = 29,28 ppm ≈ 29ppm.
Đáp án 29





















Danh sách bình luận